Clear Sky Science · ar
تحديد المشهد المناعي المتغير بدقة خلوية واحدة في نقائل الرئة غير صغيرة الخلايا إلى الدماغ وارتباطه باستجابات ضعيفة لمثبطات نقاط التفتيش المناعية
انتشار السرطان إلى الدماغ ولماذا يفشل العلاج في كثير من الأحيان
عند انتقال سرطان الرئة إلى الدماغ، بات بإمكان الأطباء استخدام أدوية قوية تطلق الجهاز المناعي، تُعرف بمثبطات نقاط التفتيش المناعية. ومع ذلك، لا يزال العديد من المرضى الذين يتلقون هذه الأدوية يشهدون نمو أورامهم الدماغية أو عودتها، حتى عندما تستجيب أورام الرئة. تطرح هذه الدراسة سؤالاً مباشراً لكنه محوري: ما الاختلاف في الخلايا المناعية داخل نقائل الدماغ مقارنة بتلك في الورم الأصلي بالرئة، وكيف يمكن لتلك الاختلافات أن تفسر لماذا يفشل العلاج المناعي الحديث في كثير من الأحيان في الدماغ؟
فحص كل خلية مناعية على حدة
لمعالجة هذه المشكلة، استخدم الباحثون تسلسل الرنا أحادي الخلية، تقنية تقرأ أي الجينات نشطة في عشرات الآلاف من الخلايا الفردية. جمعوا الخلايا المناعية من أورام الرئة ومن نقائل الدماغ لدى أشخاص مصابين بسرطان الرئة غير صغير الخلايا، الشكل الأكثر شيوعاً من سرطان الرئة. من خلال توصيف أكثر من مئة ألف خلية، بنوا خريطة عالية الدقة للمشهد المناعي في كل موقع. أتاح لهم ذلك تحديد عائلات مميزة من خلايا T، والخلايا التغصنية، والوحيدات، والبلعمات، وخلايا B، والخلايا البلازمية، ورصد أي أنواع الخلايا كانت وفيرة أو نادرة في الدماغ مقارنة بالرئة.
خلايا T المتجهة نحو الإجهاد وفقدان الذاكرة المناعية
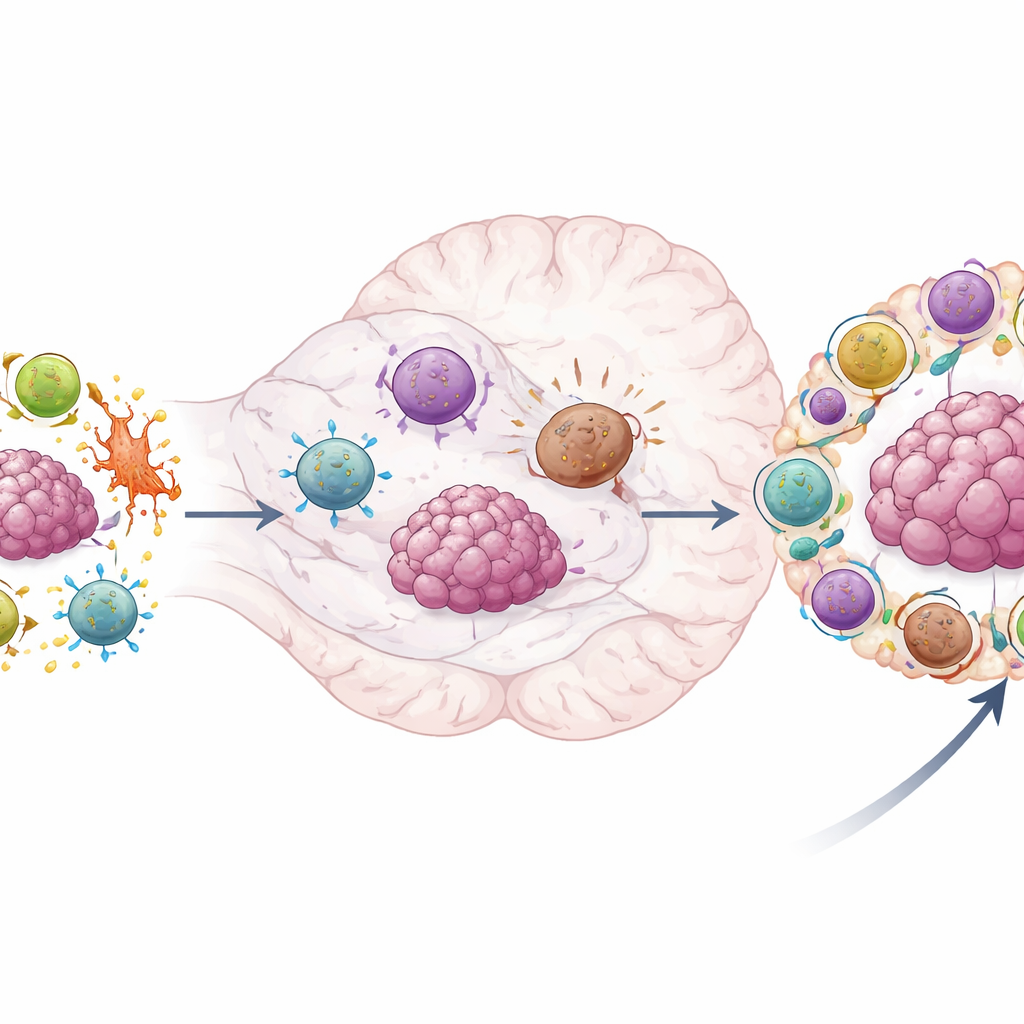
وجد الفريق أن نقائل الدماغ مليئة بخلايا T تُظهر علامات إجهاد خلوي شديد. هذه الخلايا شغّلت مستويات عالية من جينات تُنتج بروتين صدمة حرارية يسمى HSP70، وهو علامة كلاسيكية للخلايا تحت الضغط. كانت خلايا T المساعدة وخلايا T القاتلة ذات هذا النمط المجهد أكثر شيوعاً في آفات الدماغ مقارنة بالأورام الأساسية في الرئة. وعلى الرغم من أن بعض هذه الخلايا لا تزال تحمل سمات تنشيط أو هجوم، إلا أنها أيضاً أظهرت علامات الإرهاق Dysfonction وضعف الأداء. عند تحليل المؤلفين لمجاميع بيانات سريرية واسعة لمرضى عولجوا بمثبطات نقاط التفتيش، كان الأشخاص الذين كانت أورامهم تحمل تواقيع أعلى من هذه الخلايا T ذات HSP70 العالية يميلون إلى تجربة تقدم أسرع في المرض.
وبالمثل، نُقِصت عدة أنواع من خلايا T التي تعمل عادة كذراع «الذاكرة» طويلة الأمد للجهاز المناعي في نقائل الدماغ. كانت خلايا T المساعدة ذات الطابع الذاكري المركزي وخلايا T القاتلة المقيمة في الأنسجة — وكلاهما قادر على البقاء والاستجابة بسرعة للسرطان — أكثر شيوعاً في أورام الرئة وكانت مرتبطة بنتائج أفضل بعد العلاج المناعي. في الدماغ، حلت هذه أحواض الذاكرة الواقيه محلها خلايا T متداولة عالية التكاثر أظهرت ضغوطاً أيضية وكانت مرتبطة باستجابات علاجية أسوأ. معاً، يرسم هذا صورة نقائل دماغية كبيئة يفقد فيها الرقابة المناعية المتينة وعالية الجودة وتستبدل بخلايا T متعبة، مُجهدة، وأقل فعالية.
الخلايا الداعمة التي تساعد أو تعرقل الهجوم المناعي
لا تتوقف القصة عند خلايا T. فحص المؤلفون أيضاً أنواع خلايا مناعية أخرى تشكل بيئة الورم. في الأورام الأساسية بالرئة، وجدوا خلايا تغصنية وفيرة من نوع متخصص في عرض المواد الغريبة لخلايا T، تعمل فعلياً كمعلمين يدربون خلايا T على التعرف على السرطان ومكافحته. كانت هذه الخلايا أندر بكثير في نقائل الدماغ، ووجودها في أورام الرئة ارتبط ببقاء أفضل عند استخدام علاج نقاط التفتيش. انقسمت الخلايا الوحيدة والبلعمات أيضاً إلى فصائل مفيدة وضارة. أظهرت مجموعة وحيدات في أورام الرئة علامات التهاب نشط ودعم للهجوم المناعي، في حين عرضت مجموعة وحيدات أخرى، متسربة في الدماغ، تغيرات في استخدام الطاقة تشير إلى دور مكبوت للمناعة. وبالمثل، تراكمت فئة من البلعمات الموسومة بجزيء يدعى PLTP في نقائل الدماغ وكانت مرتبطة بنتائج أسوأ، بينما ارتبطت مجموعة بلعمات أخرى في أورام الرئة باستجابات أكثر ملاءمة.
بناء بصمة جينية للتنبؤ باستجابة العلاج
من خلال دمج اكتشافاتهم أحادية الخلية مع بيانات التعبير الجيني الكلي من مجموعات مرضى أكبر، استخلص الباحثون «بصمة مناعية مستمدة من نقائل الدماغ» مكونة من سبعة جينات، أطلقوا عليها BMIS. تلتقط هذه البصمة التوازن بين خلايا T المجهدة والبلعمات الكابحة من جهة، والبرامج المناعية الأكثر فعالية من جهة أخرى. عندما طبقوا BMIS على مجموعات مستقلة من مرضى بسرطان الرئة وسرطان المثانة النقيلي الذين يتلقون مثبطات نقاط التفتيش، أدلت درجات BMIS الأعلى باستمرار بأن هؤلاء المرضى لديهم بقاء أسوأ ومعدلات استجابة أقل. ومن اللافت أن BMIS أضاف قوة تنبؤية تتجاوز عبء الطفرات الورمية المستخدم عادةً، ما يشير إلى أن فهم حالة البيئة المناعية يمكن أن يكمل المؤشرات الحيوية المستندة إلى الحمض النووي.
ما يعنيه هذا للمرضى والعلاجات المستقبلية
للقارئ العام، الخلاصة أن نقائل الدماغ من سرطان الرئة ليست مجرد أورام عادية في موقع جديد؛ بل تقع في حي مناعي متغير جوهرياً. المدافعون الرئيسيون — خلايا الذاكرة T والخلايا التغصنية العارضة للمستضدات — مُنهَكون، بينما تهيمن خلايا T المجهدة، والوحيدات المُعاد تشكيلها أيضياً، والبلعمات الكابحة. يساعد هذا النظام المناعي المنحرف في تفسير سبب قدرة عقاقير نقاط التفتيش الحديثة على السيطرة على المرض في الرئة لكنها تفشل في الدماغ. من خلال تحديد أنواع الخلايا والبرامج الجينية المحددة، وترجمتها إلى درجة جينية عملية، تمهد هذه الدراسة الطريق لتحسين التنبؤ بمن سيستفيد من العلاج المناعي ولتصميم علاجات جديدة تهدف إلى استعادة حضور مناعي صحي وفعال في الدماغ.
الاستشهاد: Bai, M., Yin, T., Li, X. et al. Identification of altered immune landscape at single-cell resolution in NSCLC brain metastasis and its association with poor immune checkpoint inhibitor responses. Nat Commun 17, 2370 (2026). https://doi.org/10.1038/s41467-026-70715-6
الكلمات المفتاحية: سرطان الرئة غير صغير الخلايا, نقائل الدماغ, البيئة المناعية للورم, مقاومة العلاج المناعي, تسلسل الرنا أحادي الخلية