Clear Sky Science · ar
Frazzled/DCC يوجّه دمج السلف المكانية لضمان تجدد معوي مستقر
كيف يجددَ الجهاز الهضمي نفسه بهدوء
يومياً، تتلف الخلايا المبطنة للأمعاء وتحتاج إلى استبدال، ومع ذلك يحافظ العضو على شكله وحجمه بدقة مدهشة. تكشف هذه الدراسة، باستخدام ذبابة الفاكهة كنموذج، عن نظام توجيه خفي يخبر الخلايا المعوية الوليدة بالضبط إلى أين تذهب لسد الفجوات الصغيرة في البطانة. فهم هذا «التحكم في حركة الخلايا» لا يوضح فقط كيف تحافظ الأعضاء الصحية على نفسها، بل يسلّط الضوء أيضاً على كيف يمكن أن تُستغل إشارات التوجيه المماثلة أثناء انتشار السرطان.
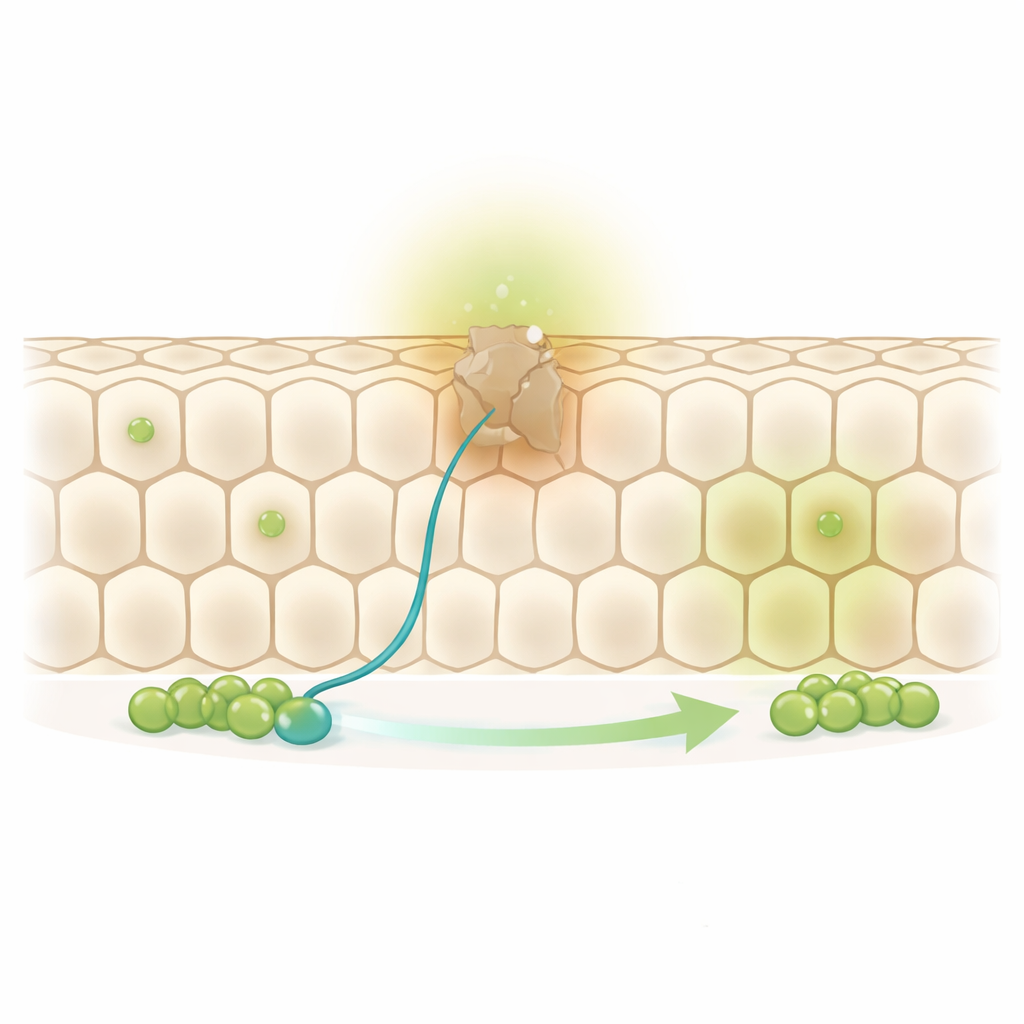
بنية شبيهة بالخلايا النحلية في حركة مستمرة
سطح أمعاء ذبابة الفاكهة مغطى بطبقة واحدة من الخلايا الامتصاصية الكبيرة المرتبة مثل خليّة نحلة. في قاعدة هذا الصف تجلس خلايا جذعية متناثرة وبناتها المباشِرات، المسماة السلفيات. عندما تبلغ خلية امتصاصية قديمة نهاية عمرها، تنقسم خلية جذعية وتستبدل ابنتها السلفية الجارة المتعبة في نهاية المطاف. مع ذلك، لاحظ المؤلفون أن نحو ثلث الخلايا في هذا النمط العسلي ليس لديها خلية جذعية أو سلفية مباشرة بجانبها. هذا أثار لغزاً: كيف تُجدد هذه الخلايا «الخارجة عن المتناول» دون أن تترك ثقوباً في الحاجز؟
خلايا جديدة في حالة حركة
من خلال تتبّع أحداث الاستبدال الفردية على مدار أسبوع، وجد الباحثون أن هذه الخلايا النائية تُجدَّد بنفس تواتر تلك الموجودة بجانب خلية جذعية مباشرة. وهذا يوحي بأن السلفيات يجب أن تتحرك. بالفعل، لاحظ الفريق أن السلفيات تطيل نتوءات طويلة ورفيعة—شعوريات خلوية—أبعد وأكثر تكراراً من الخلايا الجذعية نفسها. هذه النتوءات ليست عشوائية: في الظروف الطبيعية تشير أساساً نحو الجيران الأقدم غير المستبدَلين بدلاً من نحو الذين تم تجديدهم حديثاً، مما يشير إلى سلوك نشط للبحث والإنقاذ موجّه نحو الخلايا الأكثر حاجة للاستبدال.
إشارة توجيه عصبية أعيد توظيفها للأمعاء
لفهم كيفية توجيه هذه النتوءات، لجأ المؤلفون إلى عائلة جزيئات معروفة جيداً من توصيلات الدماغ: النترينات ومستقبلاتها Frazzled/DCC وUnc-5. في الجهاز العصبي تعمل النترينات كمنارات بعيدة المدى تجذب أو تردم ألياف الأعصاب النامية. في أمعاء الذبابة أظهر الفريق أن مستقبلات Frazzled/DCC وUnc-5 توجد تحديداً على السلفيات، ومركّزة في نتوءاتها. الخلايا الامتصاصية المتعبة، بدورها، تبدأ في إنتاج وإطلاق نتْرِين يُدعى Netrin-B. عندما زاد الباحثون Netrin-B في خلايا مختارة، أطالت السلفيات نتوءاتها ووجّهتها نحو المصدر، ثم هاجرت لتشغل تلك البقعة. وعندما حجَبوا Netrin-B أو عطّلوا Frazzled، قصرَت النتوءات، ولم تعد الخلايا النائية تُستبدل بكفاءة، وماتت الذبابات في عمر مبكر، مما يؤكد مدى أهمية هذا التوجيه لصحة الأمعاء.
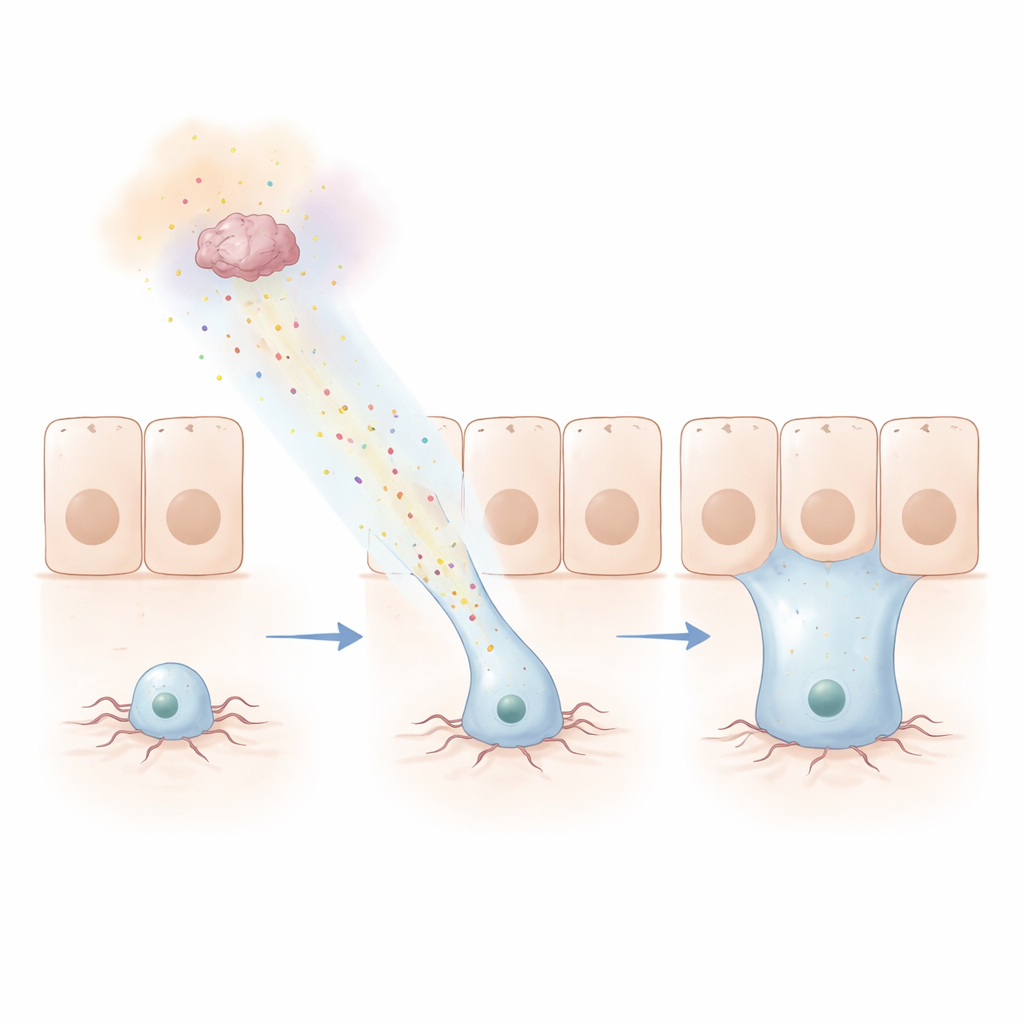
اتباع أثر كيميائي
لاستكشاف مدى وصول هذه الإشارة، بنى الفريق اختباراً مبتكراً سمّاه «هاملين»، نسبة إلى صفّار حلب. جعلوا حلقة من الخلايا عند تقاطع مناطق الأمعاء تفرز النترينات، مع وسم السلفيات بعلامة فلورية على مسافة. على مدى أيام، هاجرت السلفيات حتى عشرات الميكرومترات نحو المصدر، حتى عابِرةً حدوداً حادة إلى طبقة نسيجية مختلفة واندماج هناك. النسخ البشرية من النترينات ومستقبل DCC استطاعت أن تحلّ محل نظيراتها في الذبابة وتوجّه هذه الحركات أيضاً، مما يبيّن حفظ الآلية على نطاق عميق. الآلية نفسها العاملة على تحريك الخلايا في أماكن أخرى من الجسم كانت مطلوبة هنا: عندما أُزيلت مكوّنات أساسية، فشلت النتوءات والتجدد بعيد المدى.
لماذا هذا مهم للصحة والمرض
بعبارة مبسطة، تكشف هذه الدراسة أن الأمعاء لا تعتمد فقط على ضغط الانقسام المحلي للخلايا لتجديد بطانتها. بدلاً من ذلك، ترسل الخلايا المحتضرة إشارة كيميائية «استغاثة»، Netrin-B، التي تجذب سلفيات محددة مزوّدة بمستقبلات Frazzled/DCC. تطيل هذه السلفيات شعورياتها على طول التدرج، تزحف نحو الخلية المسنة، وتندمج في مكانها للحفاظ على سلامة الحاجز. وبما أن نظام النترين–DCC نفسه نشط في الثدييات وقد رُبط بغزو السرطان وانتشاره، فإن نتائج الذبابة تقدم دعماً آلياً ملموساً لاعتبار هذه الجزيئات سيفاً ذا حدين: ضرورية لإصلاح منظم في الأنسجة الصحية، لكن قد تكون خطيرة عندما تُسيء الأورام تنظيمها وتتعلم التحرك والاستعمار في أعضاء جديدة.
الاستشهاد: Zipper, L., Ramon-Cañellas, P., Akkas-Gazzoni, F. et al. Frazzled/DCC directs spatial progenitor integration ensuring steady-state intestinal turnover. Nat Commun 17, 2491 (2026). https://doi.org/10.1038/s41467-026-70704-9
الكلمات المفتاحية: خلايا جذعية معوية, هجرة الخلايا, إشارة نتْرِين, التوازن النسيجي, انبثاث السرطان