Clear Sky Science · ar
الانتقالات البنائية في التجميع التدريجي لجزئيات نواة البروتيازوم
كيف تتخلص الخلايا من النفايات الجزيئية
داخل كل خليةٍ من خلايانا، يجب تكسير البروتينات المستهلكة والتالفة قبل أن تتراكم كقمامة. تقوم آلة جزيئية عملاقة تُسمى البروتيازوم بمعظم أعمال التنظيف هذه، وهي بالفعل هدف لأدوية مضادة للسرطان. تستعرض هذه الدراسة ما يحدث خلف الكواليس عندما تُبنى النواة المُحفِّزة للبروتيازوم خطوة بخطوة في خلايا الخميرة، كاشفةً عن اختصارات وفحوصات أمان غير متوقعة تساعد في ضمان أن تعمل الآلة النهائية بدقة وفقط عندما تكون جاهزة.
بناء برميل يمزق البروتينات
الجانب الفاعل من البروتيازوم هو نواة على شكل برميل مكوّنة من حلقات متراكبة من وحدات فرعية بروتينية. يحتوي هذا البرميل مواقع القطع المخفية التي تقطع البروتينات الأخرى إلى قطع صغيرة. وبما أن تشغيل هذه القواطع مبكراً سيكون خطيراً، فإن الخلايا تُجمّع البرميل على شكل سلسلة من الوسطاء الجزئيين. ركز المؤلفون على النسخ المبكرة من النواة، المعروفة بالمجمعات السالفة، والتي تكون عادة نادرة وعابرة. من خلال إبطاء إحدى آخر خطوات التجميع قليلاً، تمكنوا من التقاط وتنقية هذه الأشكال المبكرة من الخميرة وتصويرها باستخدام المجهر الإلكتروني بالتبريد عالي الدقة، الذي يجمد الجزيئات أثناء العمل ويكشف عن أشكالها ثلاثية الأبعاد.
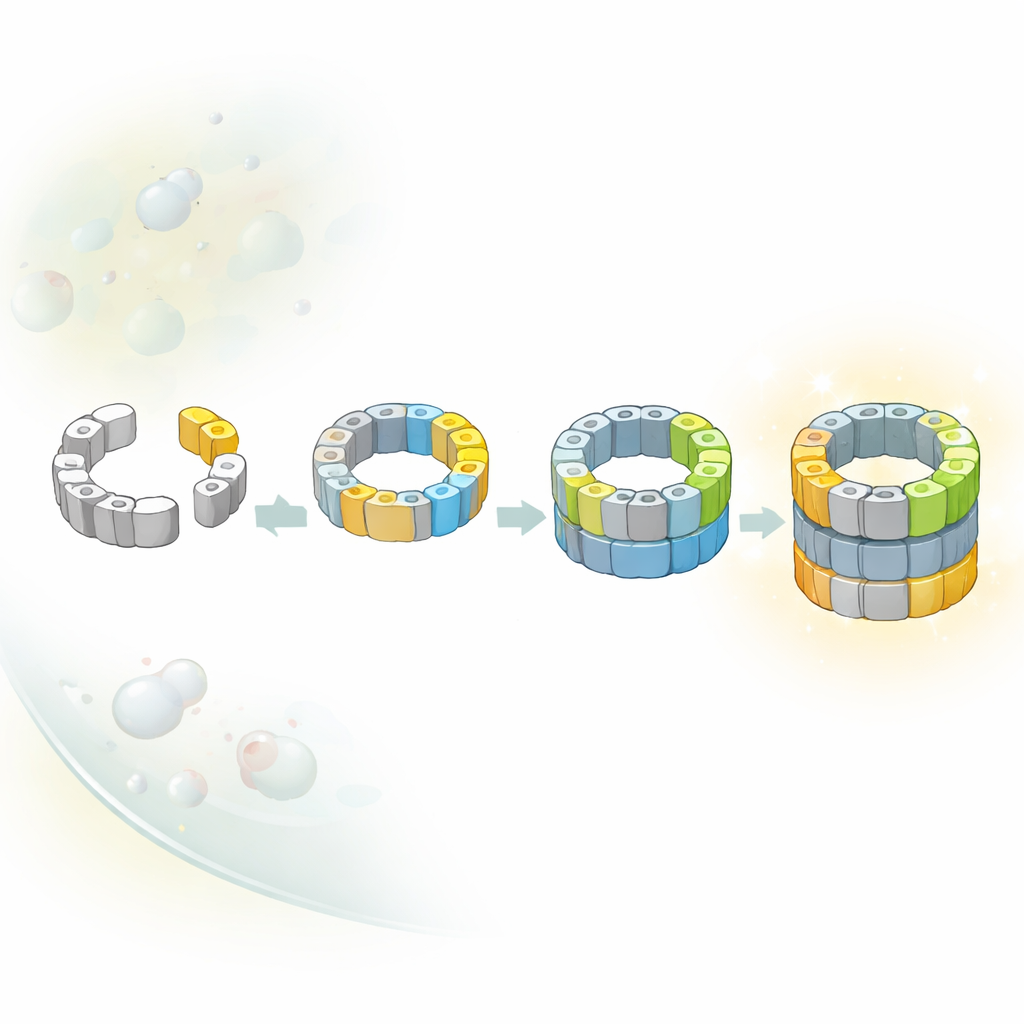
طرق متعددة تؤدي إلى نفس النواة
تميل الرسوم التوضيحية التقليدية في الكتب إلى الإيحاء بأن الآلات المعقدة داخل الخلايا تُبنى على طول مسار واحد ثابت. هنا، اكتشف الباحثون أن الأمر ليس كذلك بالنسبة لنواة البروتيازوم. حدّدوا عدة وسطاء متميّزين يختلفون في أي الوحدات التحفيزية انضمت إلى البرميل نصف المُنجَز. من خلال الجمع بين لقطات هيكلية وحيل جينية تُشغّل أو تُطفئ وحدات فرعية فردية، أظهروا أن مسارين بديلين على الأقل يؤديان من نصف برميل مبكر إلى برميل يكاد يكتمل. في أحد المسارين، تصل وحدة فرعية معينة تُسمى β5 أولاً؛ وفي مسار آخر، يمكن لوحدة فرعية مختلفة، β1، أن تنضم في وقت أبكر. من المحتمل أن يتوقف التوازن بين هذين الطريقين على أي اللبنات البنائية تكون أكثر توفراً في البيئة المزدحمة داخل الخلية.
من أجزاء مترهلة إلى حجرة قطع مُغلقة
تكشف البُنى أيضاً كيف تُهيأ مواقع القطع في البروتيازوم بعناية مع تقدم التجميع. في الوسائط المبكرة، تكون مناطق الحلقات المحيطة بالبقايا القطعية المدفونة مترهلة وضعيفة التنظيم، والمراكز التحفيزية ما تزال محجوبة بواسطة مقاطع قصيرة تسمى «بروبيبتايد». مع انضمام وحدات فرعية إضافية حول الحلقة، تتبنى هذه الحلقات تدريجياً أشكالاً أكثر تحديداً تُقَرن الأحماض الأمينية الحاسمة اللازمة للتفعيل الذاتي. فقط عندما تلتقي نصفا البرميل أخيراً، مكتملة الحلقة المزدوجة، فإن هذه الحلقات تقفل بالكامل في ترتيبها النشط وتؤدي إلى إزالة المقاطع المانعة. هذا الربط بين الهندسة والكيمياء يساعد على ضمان أن تظهر قدرة القطع القوية فقط داخل حجرة محكمة الإغلاق، مما يحمي بقية الخلية.
المساعدون «الشابرون» يوجّهون ثم يتركون المهمة
أثناء العملية، تقوم بروتينات مساعدة متخصصة تُسمى الشابرونات بمرافقة البرميل الجاري تجميعه ومنع التوليفات الخاطئة. تبدأ شابرونة واحدة، Ump1، في حالة غير مُنظمة إلى حد كبير لكنها تطوي تدريجياً مع إحاطة المزيد من الوحدات الفرعية بها، فتُحاصر في النهاية في التجويف المركزي ثم تُدمر بمجرد أن يصبح البرميل فعالاً. زوج آخر من الشابرونات، Pba1–Pba2، يمسك بسطح الحلقة الخارجية بذكاء بطريقتين. حلقة مرنة من Pba1 تَسْتَقر بين وحدتي حلقة خارجية كفاصل، مباعدة إياهما قليلاً ومنع الإغلاق المبكر. وفي الوقت نفسه، يساعد الطرف الخلفي لإحدى الوحدات الخارجية (α1) في وضع المقاطع المجاورة بحيث يمكن عند المرحلة النهائية تحرير الشابرونات وإغلاق الحلقة بشكل صحيح. عندما حذف الباحثون ذيل α1، توقف التجميع في حالة متأخرة وكادت تكتمل لكنها احتفظت بشابروناتها بعناد، مؤكدة أن هذه المنطقة الصغيرة تعمل كجزء من مفتاح إطلاق.
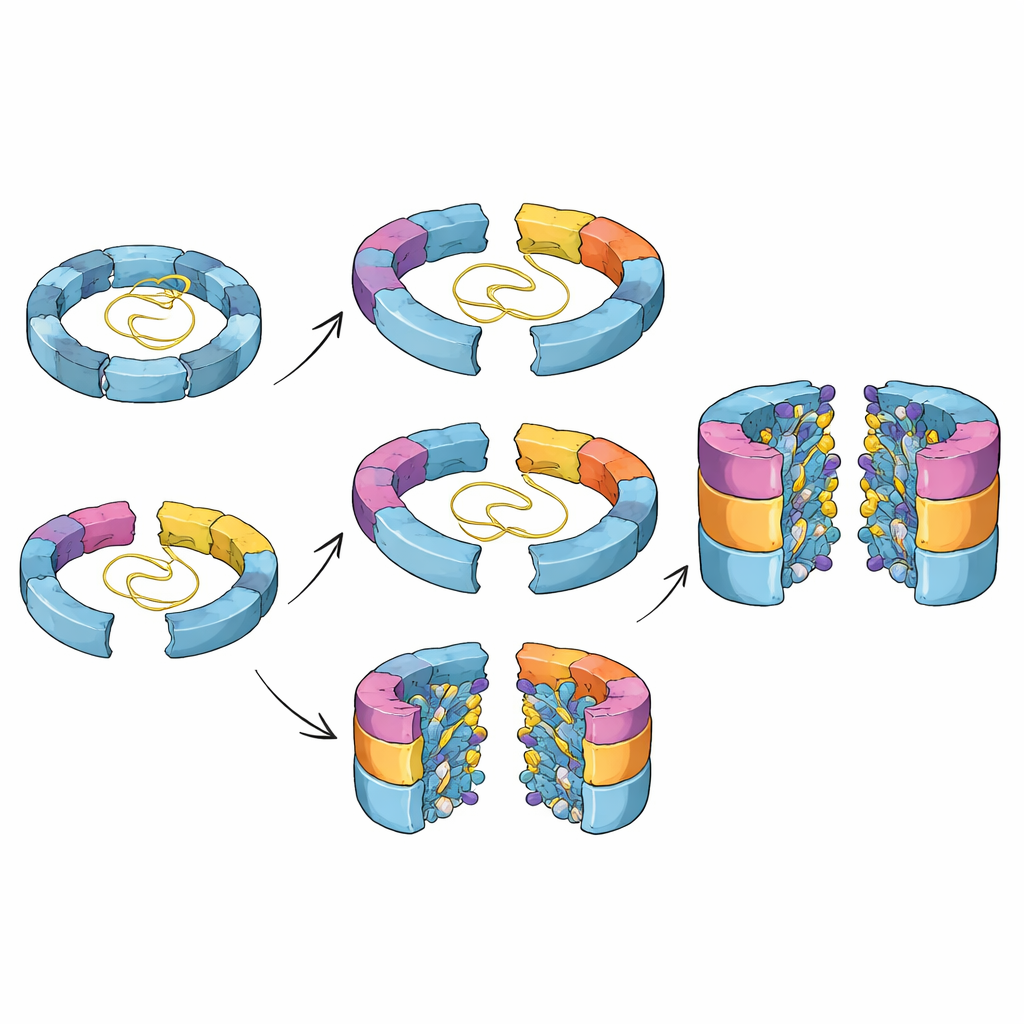
لماذا تهم هذه الخطوات الخفية
سواءً معاً، ترسم هذه النتائج صورة مفصّلة لكيفية تنسيق الخلايا لتجميع آلة تقطيع بروتينية خطرة لكنها أساسية. تُظهر الدراسة أن نواة البروتيازوم يمكن بناؤها بأكثر من طريق واحد، وأن مواقعها النشطة تُنحت تدريجياً في مواضعها، وأن البروتينات المساعدة لا تثبت الوسطاء الأوائل فحسب بل تُبرمج أيضاً في دائرة زمنية تضمن مغادرتها في اللحظة المناسبة. يساعد فهم هذه الخطوات الخفية في تفسير كيف يمكن لتغيرات جينية صغيرة في عوامل التجميع أن تساهم في المرض، وقد يساعد تصميم أدوية تضبط نشاط البروتيازوم في السرطان أو اضطرابات المناعة أو التنكّس العصبي عن طريق استهداف بنائه بدل شكله النهائي.
الاستشهاد: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
الكلمات المفتاحية: تجميع البروتيازوم, تحلل البروتينات, البروتينات المساعدة الجزيئية, المجهر الإلكتروني بالتبريد, مراقبة جودة الخلايا