Clear Sky Science · ar
سورورين تغلق بوابة خروج الحمض النووي لكوهيسين للحفاظ على تلاصق الأختين الكروماتيديتين
الحفاظ على الكروموسومات المنسوخة معًا بأمان
في كل مرة تنقسم فيها خلية، يجب أن تنسخ حمضها النووي ثم تنقل مجموعة مكتملة إلى كل خليةٍ ابنة. إذا تباعدت تلك النسخ قبل الأوان، فقد يؤدي ذلك إلى كسر الكروموسومات، وفوضى جينية، وأمراض بما في ذلك السرطان. تكشف هذه الدراسة كيف أن قطعة بروتينية صغيرة تُدعى ذيل سورورين تعمل كقفل مادي على مشبك حلقي الشكل يُمسك النسختين الشقيقتين من الحمض النووي معًا، موضحة كيف تحافظ الخلايا على اقتران الكروموسومات حتى اللحظة الدقيقة للانفصال.
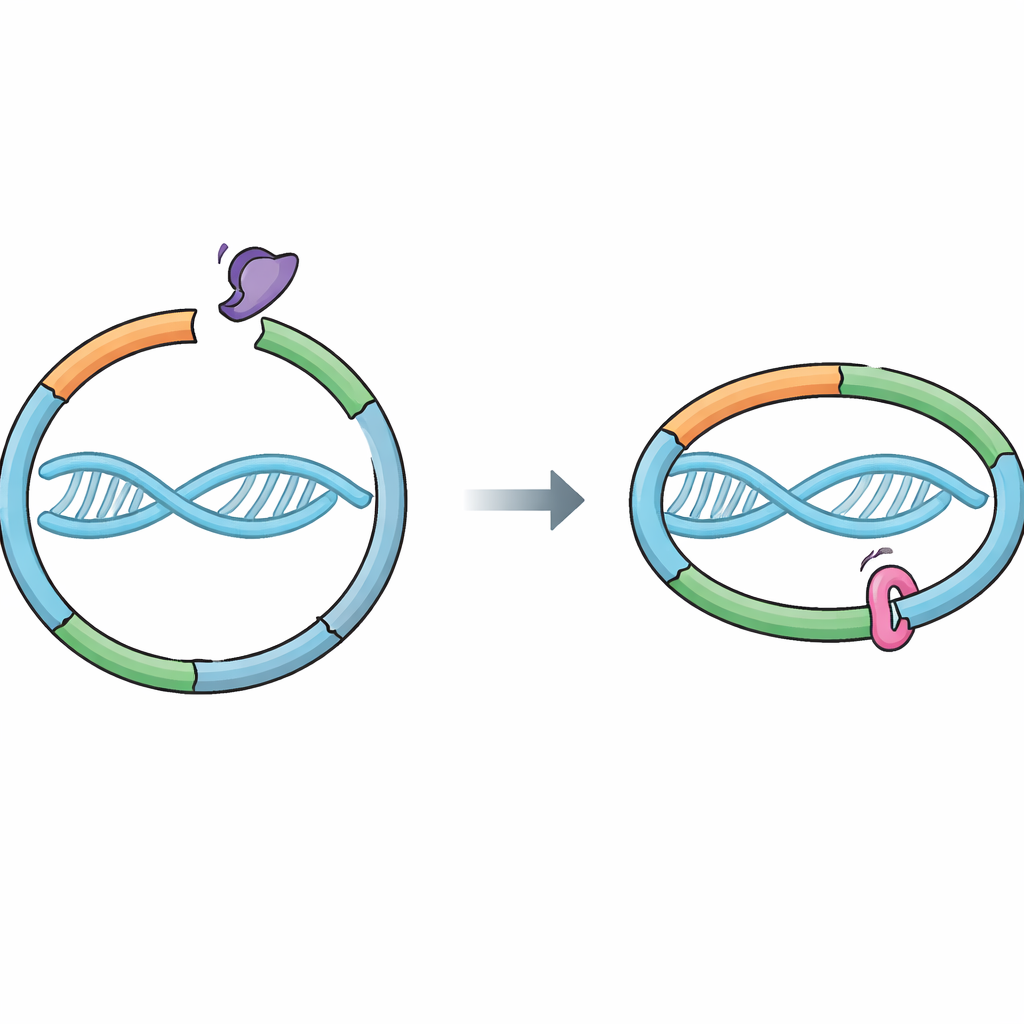
حلقة جزيئية تحرس جيناتنا
تعتمد الخلايا على ماكينة بروتينية تُسمى الكوهيسين لربط الكروموسومات المنسوخة حديثًا معًا. يشكل الكوهيسين حلقة تحيط بالحمض النووي، رابطًا بين الخيطين الشقيقين الناتجين عن تكرار الحمض النووي. يجب أن تكون هذه الرابطة قوية بما يكفي لتحمل كل الاندفاعات أثناء انقسام الخلية، لكنها قابلة للفتح في الوقت المناسب حتى ينفصل الشقيقان بنظافة. يساعد بروتين مساعد يُدعى وابل (Wapl) على فتح «بوابة خروج» محددة في الحلقة حيث يلتقي جزآن من الكوهيسين، RAD21 وSMC3. فتح هذه البوابة يسمح للحمض النووي بالانزلاق للخارج ولكوهيسين بالسقوط. حتى الآن، كان يُعتقد أن سورورين يحافظ على التلاصق بالأساس عن طريق حجب شريك وابل المسمى Pds5، لكن كان من غير الواضح ما إذا كان سورورين يلامس حلقة الكوهيسين مباشرة أيضًا.
ذيل صغير بقوة تثبيت كبيرة
ركز الباحثون على نهاية سورورين المتطرفة — آخر 30 حمضًا أمينيًا، المسماة المنطقة الطرفية C (CTR). عن طريق تقطيع سورورين إلى أجزاء واختبارها في خلايا بشرية، وجدوا أن هذه المنطقة الطرفية الصغيرة ضرورية وكافية للحفاظ على اقتران الكروموسومات الشقيقة. عندما رُسّب الـCTR صناعيًا عند السنتروميرات، المواقع المركزية حيث تبقى الشقيقات ملتصقات لأطول وقت، استعاد ذلك التلاصق تقريبًا بالكامل في خلايا تفتقر إلى سورورين الكامل. وعلى النقيض، عندما تم تثبيت الـCTR على طول الكروماتين، لم يعد بالإمكان إزالة الكوهيسين بكفاءة، وفشلت الكروموسومات في الانكماش وفك التشابك بشكل صحيح. أظهرت هذه الخلايا كروموسومات انقسامية طويلة وضبابية، وجسور DNA بين الشقيقات المنفصلات، وأخطاء في التوزيع — مشكلات تشبه بشكل لافت ما يحدث عند إزالة وابل نفسه.
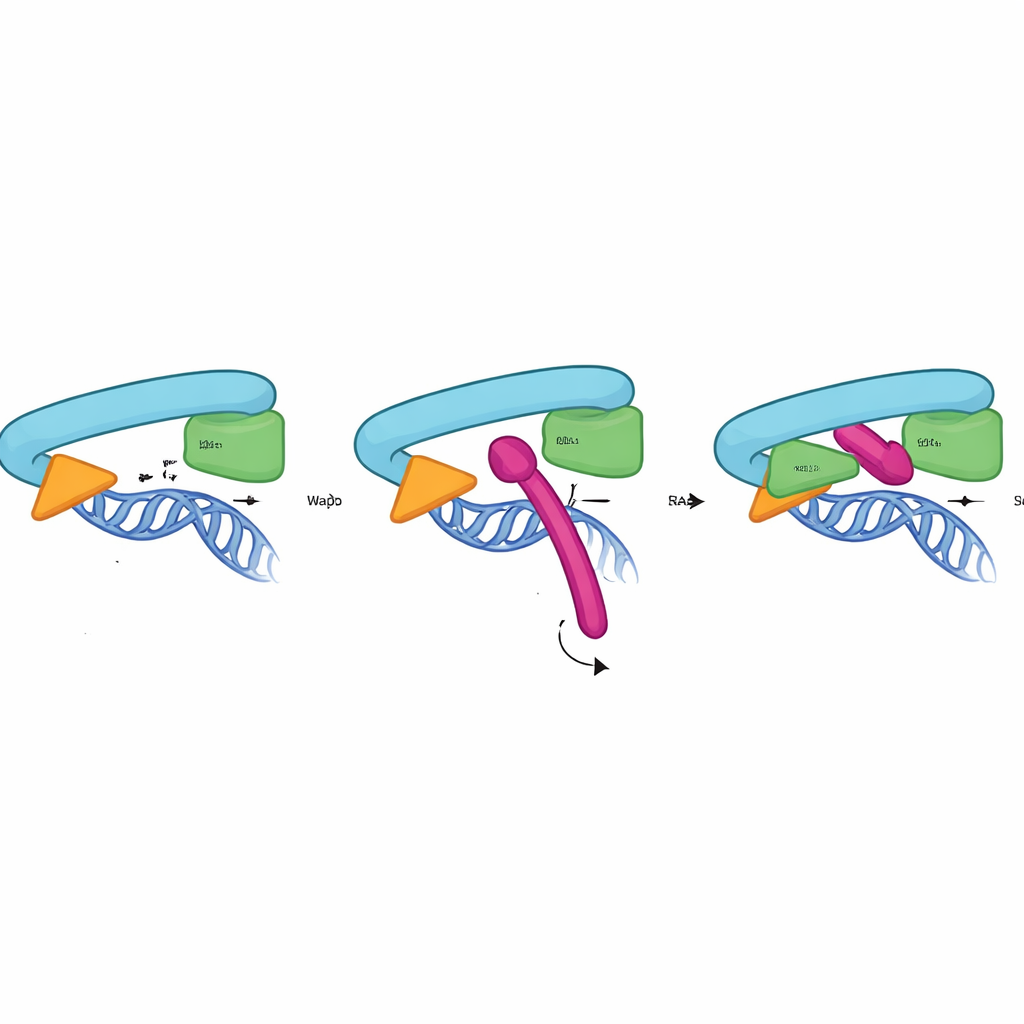
كيف يمسك قفل سورورين الحلقة
لفهم كيفية عمل الـCTR على المستوى الذري، جمع الباحثون بين اختبارات بيوكيميائية، وتغيرات جينية (ميوتانجنسيس)، وتنبؤات بنية بواسطة AlphaFold3. أظهروا أن الـCTR يرتبط مباشرة وبشكل محدد بالواجهة بين RAD21 ومنطقة الرأس في SMC3 — الموقع ذاته الذي يشكل بوابة خروج الحمض النووي. لا يتطلب هذا التفاعل وجود Pds5 أو وحدة SA2 ويحدث فقط على الكوهيسين المتصل بالكروماين، ويبلغ ذروته في الطور الذي يجب فيه الحفاظ على التلاصق بثبات. يقترح النموذج البنيوي أن لولبة قصيرة داخل الـCTR تستقر في جيب تشكله RAD21 وSMC3، مستخدمة مجموعة من البقايا المحافظة الدهنية والسالبة الشحنة للتشبث. كان تعديل بضعة نقاط اتصال فقط في سورورين أو RAD21 أو SMC3 كافياً لإبطال الارتباط والتسبب في انفصال الشقيقات قبل الأوان، مما يؤكد أن هذه الواجهة تعمل كقفل مادي للبوابة.
مفتاح إطلاق مُوقّت لفصل الكروموسومات
يجب على الخلايا أيضًا تحرير الكوهيسين في الوقت المناسب. اكتشف الفريق أن سورورين يحمل موقع تحكم قريبًا، حمض أميني واحد (S145) يُضاف إليه مجموعة فوسفات بواسطة كيناز الانقسام الميتوزي أوروورا B. يكسر هذا التعديل بشكل خاص قبضة سورورين على Pds5، مما يسمح لإعادة تدخل وابل والمساعدة في إزالة الكوهيسين من أذرع الكروموسومات، لكنه يترك تلامس الـCTR مع بوابة RAD21–SMC3 سليمًا إلى حد كبير. عند السنتروميرات، يقوم عامل آخر، Sgo1، بتجنيد فسفاتاز يزيل هذه الفوسفات، محافظًا على ارتباط سورورين–Pds5 وقفل البوابة بقوة حتى القطع النهائي لـRAD21 في الطور الانفصالي. أظهرت الاختبارات الجينية أنه عندما يُزال وابل، تختفي عيوب التلاصق الناتجة عن تعطيل تفاعل الـCTR–البوابة، مما يبرز أن المهمة الأساسية لسورورين هي حماية بوابة الخروج تحديدًا من الفتح الذي يقوده وابل.
ما يعنيه هذا لاستقرار الجينوم والمرض
معًا، تعيد هذه النتائج صياغة سورورين بوصفه حارسًا ذا وظيفتين: يتنافس مع وابل على الوصول إلى Pds5 ويغلق مباشرة بوابة خروج الحمض النووي للكوهيسين عبر الـCTR الصغير الخاص به. يضمن هذا التحكم المزدوج أن التلاصق قوي حيث يلزم، لا سيما عند السنتروميرات، ومع ذلك يمكن تقشيره عن أذرع الكروموسومات في أوائل الانقسام الخيطي للسماح بالانكماش وفك التشابك المناسبين. ونظرًا لأن الطفرات في الكوهيسين ومنظميه شائعة في اضطرابات التطور والسرطانات، فإن سطح التلامس المرسوم بدقة بين سورورين وRAD21 وSMC3 يسلط الضوء على نقطة ضعف جديدة حيث يمكن للتغيرات الصغيرة أن تزعزع الكروموسومات — وعلى هدف محتمل لعلاجات مستقبلية تسعى إلى ضبط مدى إحكام احتفاظنا بمادةنا الجينية.
الاستشهاد: Chen, Q., Yuan, X., Shi, M. et al. Sororin locks the DNA-exit gate of cohesin to preserve sister-chromatid cohesion. Nat Commun 17, 2284 (2026). https://doi.org/10.1038/s41467-026-70484-2
الكلمات المفتاحية: تماسك الكروماتيد الشقيق, مركب الكوهيسين, سورورين, انقسام الكروموسومات, استقرار الجينوم