Clear Sky Science · ar
طفرة مُمْرِضة في بروتين تاو تُحدِث خللاً في مسار التحلل الذاتي والليزوزوم يقيّد تدهور تاو في نموذج لجلطة الدماغ الجبهي الصدغي التنكسي
عندما تتأخّر طواقم التنظيف في الدماغ
لماذا يصاب بعض الأشخاص بمشكلات مدمرة في الذاكرة والسلوك قبل بلوغهم سنًّا متأخّرة؟ يتناول هذا البحث السؤال عبر التركيز على بروتين دماغي واحد، تاو، وعلى “مراكز إعادة التدوير” الخلوية الصغيرة التي عادةً ما تُبقيه تحت السيطرة. من خلال مراقبة خلايا عصبية بشرية حية بمجاهر فائقة الدقة، يبيّن الباحثون كيف تُعيق طفرة ممرضة في تاو نظام التخلص من النفايات الخلوي، وكيف أن تحفيز هذا النظام بجزيء صغير يمكن أن يساعد في تنظيف الفوضى. قد تشير نتائجهم إلى استراتيجيات علاجية جديدة لأشكال معيّنة من الخرف.
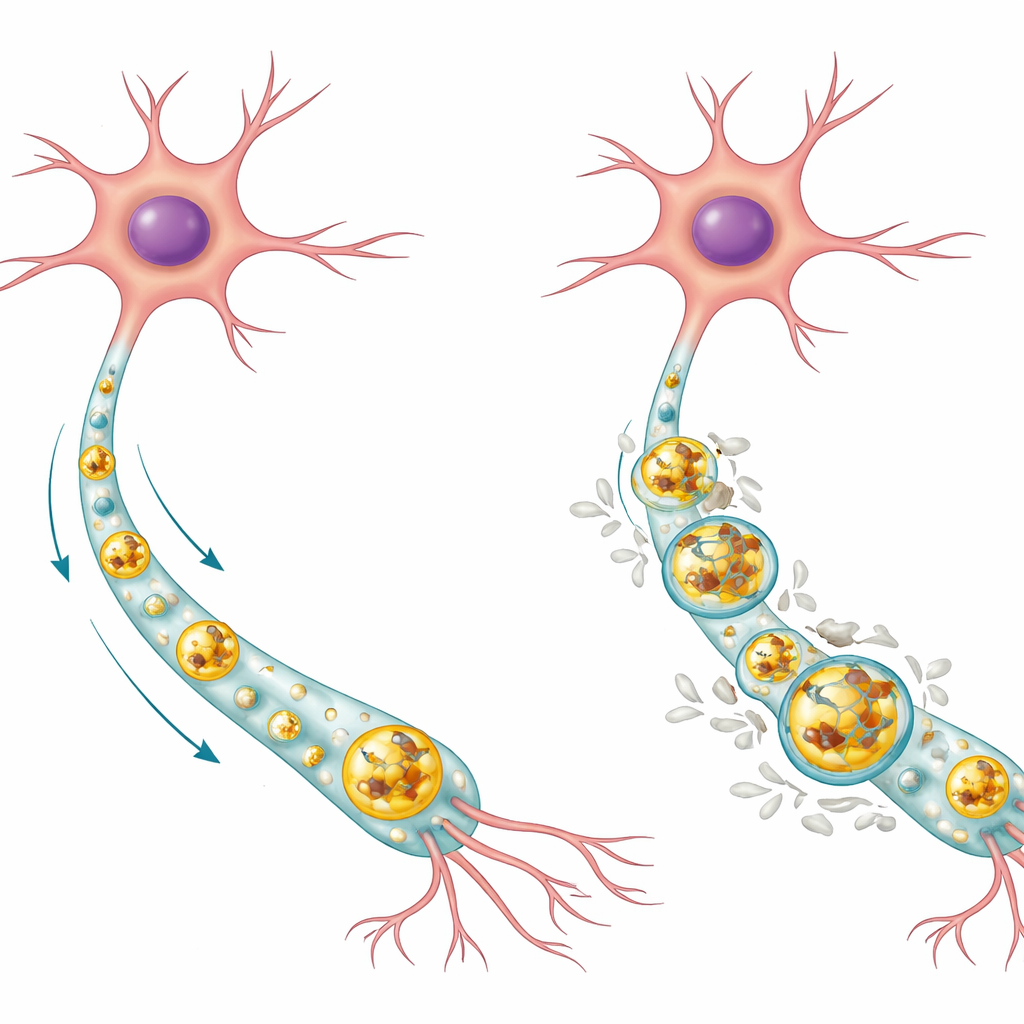
كيف تَتخلص خلايا الدماغ عادةً من القمامة
الخلايا العصبية خلايا طويلة العمر لا يمكنها ببساطة الانقسام لتخفيف المواد التالفة، لذا تعتمد بدرجة كبيرة على أنظمة تنظيف داخلية. أحد المسارات الرئيسية هو مسار التحلل الذاتي–الليزوزومي. في هذه العملية تُحاط البروتينات غير المرغوب فيها والأجزاء البالية بأكياس غشائية تُدعى الحويصلات الذاتية (autophagosomes)، التي تندمج بعد ذلك مع مقصورات مملوءة بالإنزيمات تُعرف بالليزوزومات، حيث يُكسّر الحمولة ويعاد تدويرها. في الخلايا العصبية البشرية السليمة، وجد المؤلفون أن بروتين تاو الطبيعي يميل إلى التراكم داخل المركز الحمضي لليزوزومات حيث يمكن تحلّله، بينما الشكل المفسفر من تاو (تعديل كيميائي مرتبط بالمرض) يجلس أكثر على غشاء الليزوزوم الخارجي. كانت معظم الليزوزومات في الخلايا السليمة خالية من تاو تمامًا، مما يشير إلى أن هذا النظام عادةً ما يحافظ على مستويات تاو منخفضة ومراقبة بشكل جيّد.
ما الذي يخطئ في شكل وراثي من الخرف
ركّز الفريق على طفرة في جين MAPT تُسمى p.R406W، والتي تسبب شكلاً موروثًا من الخَرَف الجبهي الصدغي ويمكن أن تحاكي فقدان الذاكرة الشبيه بمرض ألزهايمر. باستخدام تكنولوجيا الخلايا الجذعية، أعادوا برمجة خلايا جلد المرضى إلى خلايا جذعية متعددة القدرات مستحثة ثم إلى أعداد كبيرة من الخلايا العصبية البشرية التي حملت الطفرة أو التي عُدّلت جينيًا إلى الحالة الطبيعية. في الخلايا العصبية الطافرة، كانت مستويات تاو الكلي وتاو المفسفر أعلى بكثير، ليس لأن الخلايا أنتجت مزيدًا من تاو، بل لأنها قلّلت من كفاءتها في التخلص منه. كشفت التصوير الفائق الدقة أن تقريبًا كل الليزوزومات في الخلايا الطافرة كانت محشوة بتاو وبخاصة بتاو المفسفر الذي يغلف غشاء الليزوزوم. هذا التراكم دلّ على أن المسار الرئيسي للتخلص من البروتينات داخل الخلية كان مسدودًا.
مراكز إعادة التدوير المسدودة وحركة بطيئة
عند فحص آلية إعادة التدوير عن كثب، لاحظ الباحثون أن الليزوزومات في الخلايا الطافرة كانت أكثر عددًا، وأكبر حجمًا، وتميل إلى التمركز بعيدًا عن جسم الخلية. أظهر التصوير الحي بأصباغ فلورية أن هذه الليزوزومات تحرّك ببطء وتقطع مسافات أقصر على طول الألياف العصبية، على الرغم من أن مسارات الميكروتوبول الأساسية بدت طبيعية. احتوت الخلايا الطافرة أيضًا على المزيد من الحويصلات الذاتية، وزيادة في بروتين المُرشِّح للحمل p62، وقطرات دهنية إضافية—علامات على أن المواد كانت تُوسم للتخلص لكنها لم تُكسَّر بالكامل. باستخدام مُبلِغ حساس للـ pH، وجدوا أن الحويصلات الذاتية في الخلايا الطافرة غالبًا ما تفشل في الاندماج بشكل صحيح مع الليزوزومات، مما يؤدي إلى تراكم حويصلات إعادة تدوير «نصف مكتملة» وعيوب واسعة في تنظيف الخلايا، ليس فقط لتاو بل لحمولة أخرى أيضًا.
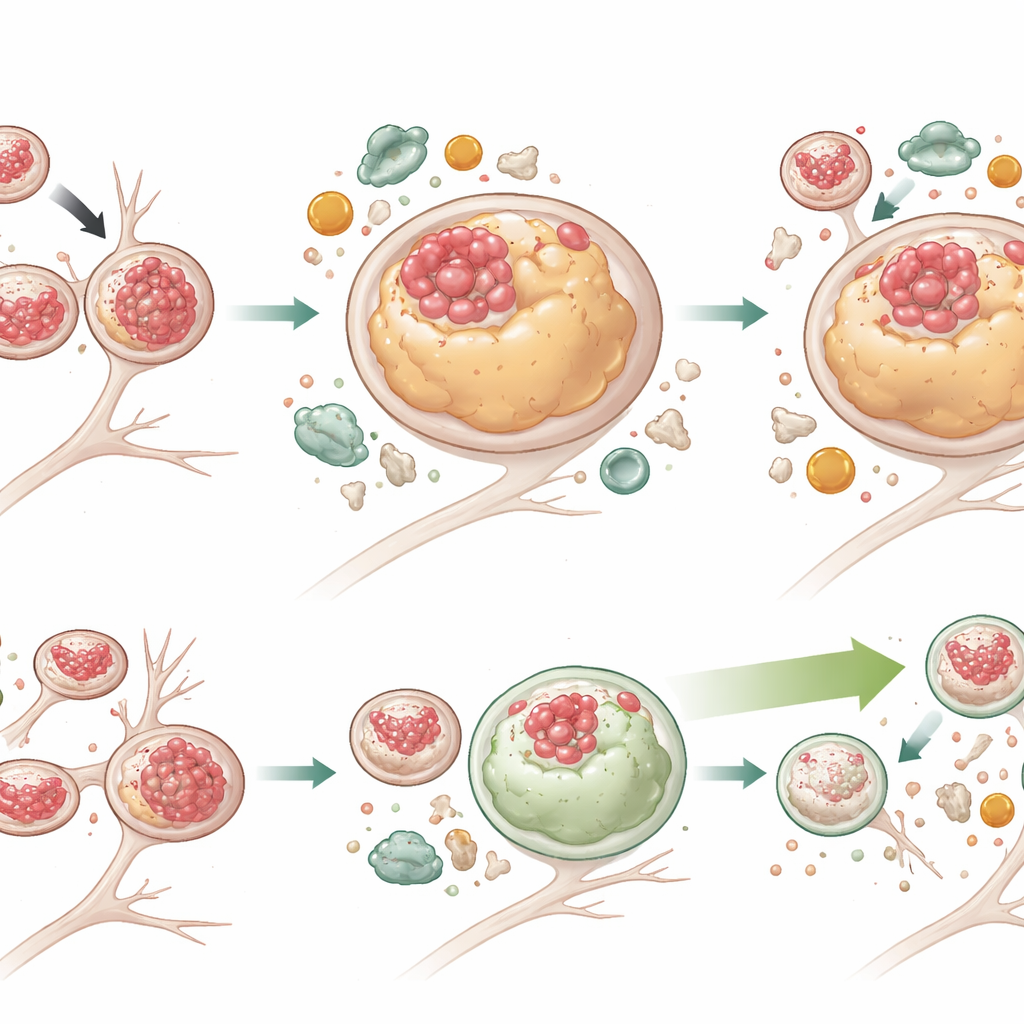
تعزيز التنظيف الخلوي من دون إصلاح الاختناق المروري
لاختبار ما إذا كان تعزيز التحلل الذاتي يمكن أن يتغلب على هذه المشكلات، عالج الفريق الخلايا العصبية بالمركب الصغير G2‑567، وهو جزيء أظهر سابقًا أنه يحفّز نظام التحلل الذاتي–الليزوزومي. بعد أسبوعين من العلاج، انخفضت مستويات تاو الكلي وتاو المفسفر في الخلايا الطافرة بشكل ملحوظ، وعادت العديد من الليزوزومات لتكون خالية من تاو مرة أخرى. كما تقلصت أحجام الليزوزومات لتقترب من الطبيعي. ازدادت علامات التحلل الذاتي النشط، بينما انخفض p62—مؤشر على توقف التحلل—في الخلايا الطافرة، مما يدل على تكسير حمولة أكثر فاعلية. من المثير للاهتمام أن G2‑567 لم يصحّح كل العيوب: فقد ظلّت الليزوزومات في الخلايا الطافرة تميل للتمركز بعيدًا عن جسم الخلية وتتحرّك ببطء، وبقي بروتين مرسال (JIP3) المرتبط بنقل الليزوزوم مرتفعًا. هذا يوحي بأن وظيفة الحركة والوظيفة التحللية لليزوزومات يمكن فصلهما جزئيًا، وأن تحسين التحلل وحده قد يكون كافيًا لتقليل تراكم تاو السام.
ما معنى هذا لعلاجات الخرف المستقبلية
لغير المتخصصين، الخلاصة الأساسية هي أنه في هذا النموذج الوراثي للخَرَف الجبهي الصدغي المشكلة ليست فقط أن تاو يصبح شاذًا؛ بل أن نظام إعادة التدوير في الخلايا العصبية لا يواكب الحمولة. تُعطّل طفرة تاو p.R406W مباشرةً عدة خطوات في مسار التحلل الذاتي–الليزوزوم، مما يسبب تراكم تاو—وخاصة شكله المفسفر—على وعلى داخل الليزوزومات، إلى جانب مواد أخرى غير مهضومة. عن طريق دفع آلة التنظيف الخلوية دوائيًا للعمل بجدّ أكثر، استطاع الباحثون خفض مستويات تاو وتطبيع حجم الليزوزومات، رغم استمرار عيوب النقل. تعزز هذه النتائج الفكرة القائلة بأن الأدوية المصمّمة لرفع مستوى التحلل الذاتي ووظيفة الليزوزوم بأمان قد تساعد في استعادة توازن البروتينات في الخرف المرتبط بتاو وربما في حالات أكثر شيوعًا مثل مرض ألزهايمر.
الاستشهاد: Mirfakhar, F.S., Marsh, J.A., Sato, C. et al. A pathogenic Tau mutation drives autophagy-lysosome dysfunction that limits Tau degradation in a model of frontotemporal dementia. Nat Commun 17, 2699 (2026). https://doi.org/10.1038/s41467-026-70473-5
الكلمات المفتاحية: بروتين تاو, التحلل الذاتي (الأتوفاجي), خلل في الليزوزوم, الخَرَف الجبهي الصدغي, التنكس العصبي