Clear Sky Science · ar
تحدد قابلية السطح للماء والصلابة سداد البروتين على الجسيمات النانوية المأخوذة فمياً لعلاج التهاب القولون
تحويل الحبوب إلى علاجات أذكى
غالبًا ما يتناول الأشخاص المصابون بأمراض الأمعاء الالتهابية مثل التهاب القولون أدوية مضادة للالتهاب قوية، ومع ذلك يضيع جزء كبير من كل جرعة أو يسبب آثارًا جانبية في أجزاء أخرى من الجسم. تستكشف هذه الدراسة طريقة جديدة لجعل الأدوية الفموية تتصرف مثل صواريخ موجهة: عبر تصميم جسيمات دقيقة حاملة للدواء تستقطب بروتينات الأمعاء الذاتية كنظام استهداف طبيعي، مما يساعد الأدوية على التوجه نحو خلايا الجهاز المناعي التي تقود الالتهاب المعوي.
كيف يكسو القناة الهضمية الجسيمات النانوية
عندما يدخل أي جسيم نانوي الجسم، يُغطَّى بسرعة بطبقة رقيقة من البروتينات، مكوّنًا ما يسميه العلماء «سداد البروتين». في الأمعاء المريضة، يبدو هذا السداد مختلفًا تمامًا عن السداد في الأنسجة السليمة لأن مزيج البروتينات المحلي قد تغيّر. سبق للمؤلفين أن وجدوا أن التهاب القولون يسبب سدادًا معويًا خاصًا يوجه الجسيمات بدرجة ما نحو خلايا مناعية تُسمى البالعات الكبيرة، التي تساهم في إشعال الالتهاب وحله. هنا، سعى الباحثون إلى تشكيل ذلك السداد عمدًا عبر تعديل ميزتين أساسيتين للجسيمات الحاملة للدواء — طردها للماء (كراهية الماء) وصلابتها — لتحويل تأثير بسيط ناتج عن المرض إلى استراتيجية استهداف فعّالة.
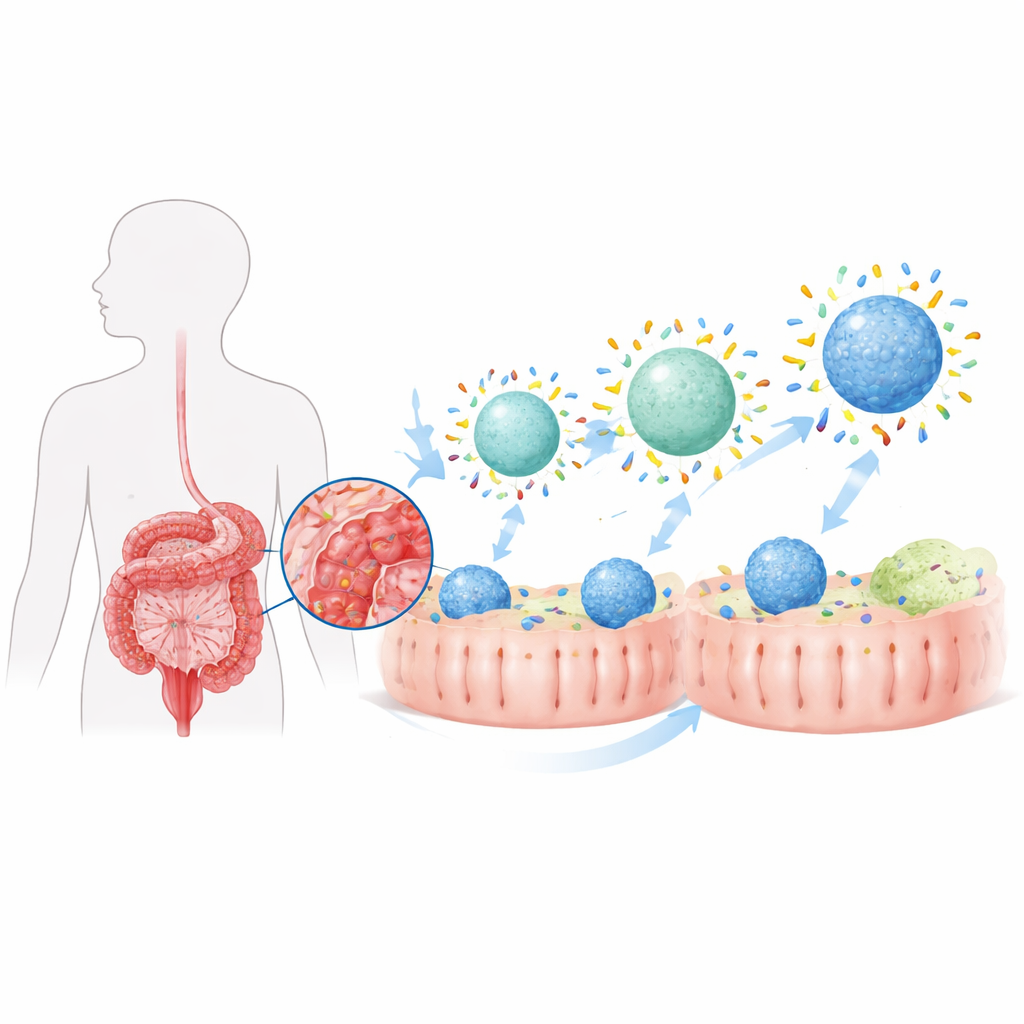
جعل الجسيمات أكثر جاذبية للبروتينات
بنى الفريق جسيمات نانوية قائمة على الدهون تشبه الفقاعات الدهنية الصغيرة وضبطوا مدى محبة أو كراهية أسطحها للماء بإضافة كميات مختلفة من طلاء بوليمري شائع. الجسيمات ذات الأسطح الأكثر كراهية للماء ربطت كمية أكبر بكثير من بروتينات الأمعاء عند تعرضها لسوائل التهاب القولون، سواء في الحيوانات أو في أنابيب الاختبار. عندما حُملت هذه الجسيمات «المناهضة للماء» بالستيرويد بوديزونيد وأعطيت فمويًا لجرذان مصابة بالتهاب القولون، سلّمت كمية دواء أكبر بكثير إلى بالعات القولون مقارنة بالإصدارات الأكثر محبة للماء. نتيجة لذلك، استعادت الحيوانات المعالجة وزنًا أكبر، وأظهرت تقصيرًا أقل في القولون وتلفًا نسيجيًا أقل، وانخفضت مستويات جزيئات الالتهاب في الأمعاء. ومع ذلك، على الرغم من تحسن الالتهاب، لم يعد الوضع إلى حالة صحية كاملة، ما يشير إلى أن زيادة كمية بروتينات السداد وحدها لم تكن كافية.
تصلب الجسيمات لاختيار شركاء أفضل
لدفع الفكرة أبعد، أبقى الباحثون الأسطح مناهضة للماء لكن غيّروا البنية الداخلية لجعل الجسيمات لينة أو متوسطة أو صلبة بملء نواتها بكريات بلاستيكية بأحجام مختلفة. بقيت الثلاثة تلتقط كميات إجمالية مماثلة من بروتينات الأمعاء، لكن تركيبة البروتينات تغيرت. شكّلت الجسيمات الأكثر صلابة سدادًا غنيًا بشكل خاص ببروتينات يمكنها الارتباط بمستقبلات على البالعات الكبيرة أو حمل مغذيات صغيرة تمتصها تلك الخلايا. أحد هذه البروتينات، S100A8، وفير في الأمعاء الملتهبة ويمكنه الاندماج مع مستقبلات خاصة بالبالعات الكبيرة. أدى حجب S100A8 على السداد إلى تقليل امتصاص البالعات الكبيرة للجسيمات الصلبة بشكل حاد، مما كشف عنه كمكوّن استهدافي رئيسي تختاره صلابة الجسيم.
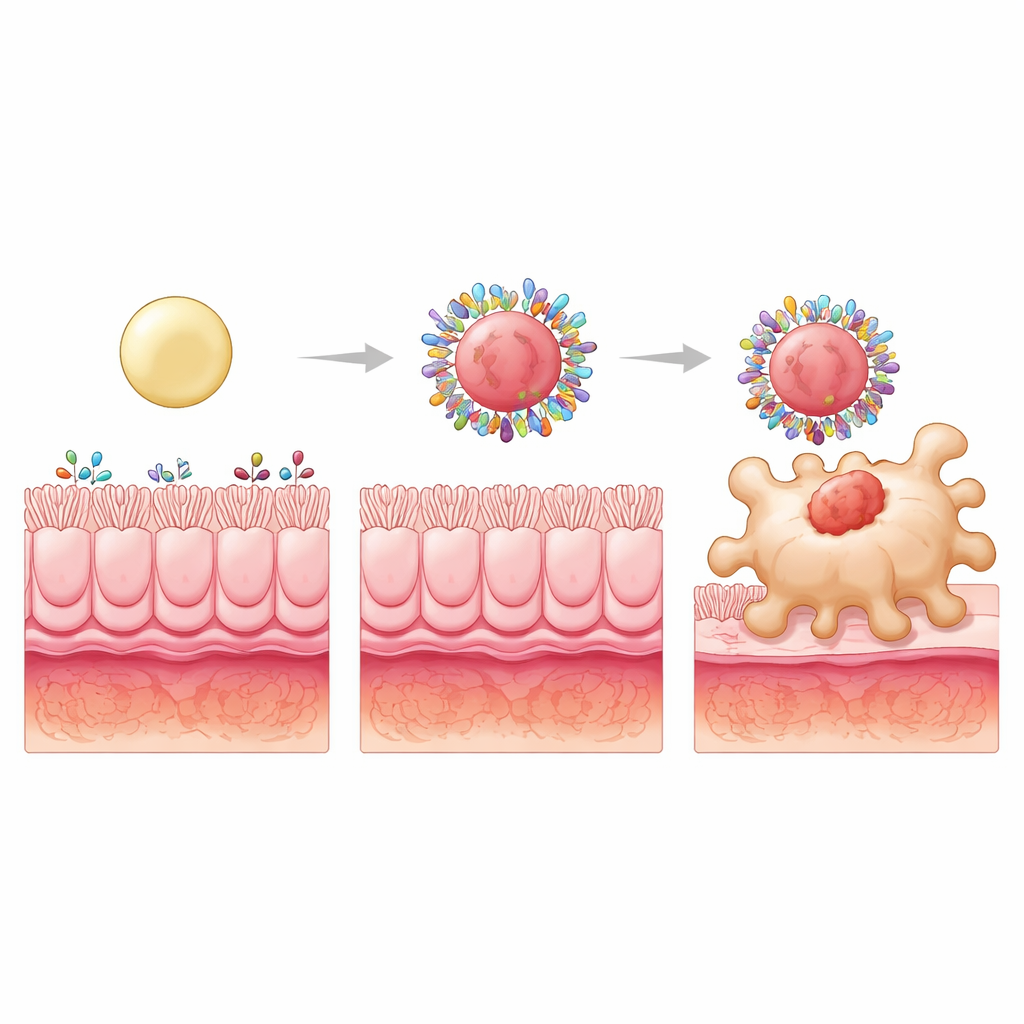
من استهداف أفضل إلى شفاء أفضل
عندما حُشي البوديزونيد داخل هذه الجسيمات عالية الكراهية للماء والعالية الصلابة وأُعطيت فمويًا لجرذان مصابة بالتهاب القولون، كانت الفوائد ملحوظة. لم تقلل التركيبة الصلبة الضرر المعوي والإجهاد التأكسدي فحسب، بل عادت أيضًا بمستويات عدة إشارات التهابية إلى تلك المرصودة في الحيوانات السليمة. أعادت توازنًا صحيًا أكبر بين أنواع البالعات «المهاجمة» و«المهدئة» وعزَّزت الخلايا التائية المنظمة التي تساعد في كبح الاستجابات المناعية. ومن المهم أن هذه المكاسب اعتمدت على بيئة البروتين المتغيرة بالمرض في التهاب القولون؛ فالتصميم نفسه لم يُظهر استهدافًا مميزًا في الجرذان السليمة، مما يؤكد أن السداد هو حليف ديناميكي ومحدد بالمرض.
لماذا يهم هذا للأدوية المستقبلية
تُظهر هذه الدراسة أننا قادرون على توجيه بروتينات الجسم نفسها لتعمل كـ«علمات» ذكية ومتجددة ذاتيًا على حوامل الأدوية الفموية ببساطة عن طريق ضبط خواص السطح والخصائص الميكانيكية للحوامل. من خلال زيادة التقاط البروتين أولًا عبر أسطح مناهضة للماء ثم استخدام الصلابة لتفضيل بروتينات موجهة نحو البالعات مثل S100A8، أنشأ الباحثون جسيمات نانوية تبحث طبيعيًا عن الخلايا المناعية التي تقود التهاب القولون وتوصِل العلاج حيث يلزم أكثر. يمكن تكييف نفس منطق التصميم — التلاعب بكيفية شعور الجسيمات وتصرفها على سطح الأمعاء — لأنواع عديدة من الأدوية النانوية والأمراض، مقدمًا مسارًا جديدًا وأكثر دقة للعلاج الموجه دون إضافة جزيئات استهداف صناعية.
الاستشهاد: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
الكلمات المفتاحية: توصيل الدواء بالجسيمات النانوية, أمراض الأمعاء الالتهابية, سداد البروتين, الطب النانوي الفموي, استهداف البالعات الكبيرة