Clear Sky Science · ar
خريطة تفاعلات على مستوى الجنس عبر نسخ متباينة من NS4B تكشف عن دور محفوظ لعملية UFMylation في تكاثر الأورثوفلافيفيروس
لماذا تهمنا هذه الدراسة الفيروسية
تنتشر فيروسات مثل الضنك وزيكا وغرب النيل إلى مناطق جديدة وقد تتسبب في أشياء تتراوح بين الحمى إلى التهابات الدماغ وعيوب الولادة. ومع ذلك ما زلنا نفتقر إلى علاجات واسعة وموثوقة. تستكشف هذه الدراسة كيف يساعد تعاون خفي بين هذه الفيروسات ونظام وسم خلوي غير معروف جيداً يُدعى UFMylation الممرضات على التكاثر. من خلال رسم خريطة هذه العلاقة عبر العديد من الفيروسات ذات الصلة، يكشف المؤلفون عن نقطة ضعف مشتركة يمكن استغلالها لتطوير أدوية مضادة للفيروسات في المستقبل.
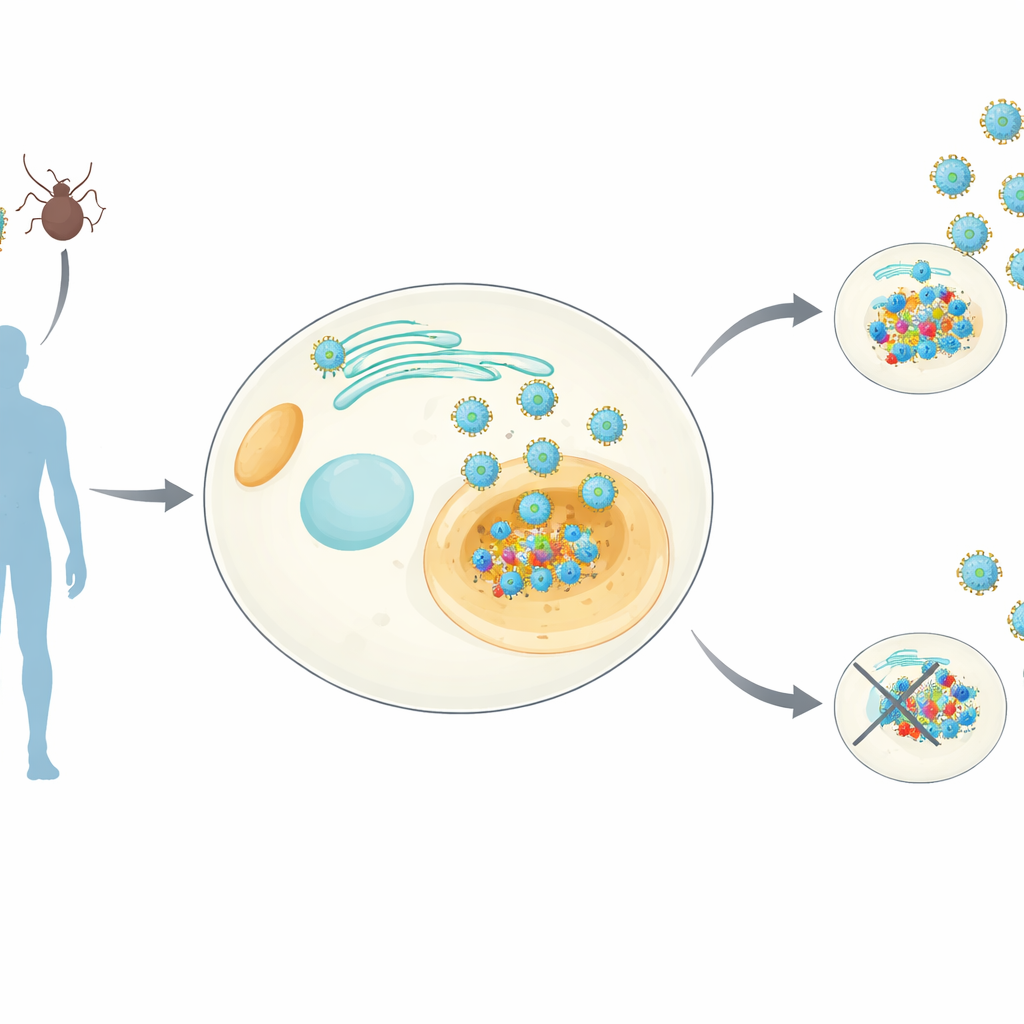
تتبع صديق فيروسي أساسي
تنتمي الأورثوفلافيفيروسات — المجموعة التي تشمل الضنك وزيكا وحمى الصفراء وغيرها — إلى فيروسات تحمل بروتينًا صغيرًا يدعى NS4B يندمج في الأغشية داخل خلايانا. من المعروف أن NS4B ضروري لتكاثر الفيروس، لكن مهامه الدقيقة ظلت غامضة. أنشأ الباحثون سلالات خلايا بشرية تعبر باستمرار عن NS4B من ثمانية أورثوفلافيفيروسات مختلفة. ثم استخدموا تقنيات قياس طيفي حساسة لسحب NS4B مع أي بروتينات بشرية ترتبط به، وبالتوازي قيَّموا كيف يغير تعبير NS4B تركيبة البروتينات الكلية في الخلية. أنتج ذلك «أطلس تفاعلات» على مستوى الجنس — الذي أسموه NS4Bome — يُظهر الأهداف الخلوية المشتركة والخاصة بكل فيروس.
حيل مشتركة وخدع مخصصة
أظهر الأطلس وجود 538 بروتينًا بشريًا تتفاعل مع NS4B وأكثر من 500 يتغير مقدارها عند وجود NS4B. يتركز العديد منها في مسارات تدير إنتاج الطاقة في الميتوكوندريا، تشكيل الأغشية الداخلية وحركة البروتينات والدهون المصنوعة حديثًا. كانت بعض التفاعلات مشتركة بين معظم الفيروسات، مما يوحي بحيل محفوظة تطوريًا تستخدمها جميع الأورثوفلافيفيروسات. بينما ظهرت أخرى في أنواع أو سلالات معينة فقط، مما قد يفسر لماذا يفضّل بعض الفيروسات البعوض على القراد، أو تُسبب أمراضًا دماغية بدلًا من الحمى النزفية. تُحوّل هذه النظرة المنظمة مجموعة مبعثرة من دراسات سابقة جزئية إلى خريطة متماسكة لكيفية إعادة هذه الفيروسات توصيل سلك الخلية.
حليف مفاجئ: نظام UFMylation
من بين العديد من الشركاء الذين ارتبطت بهم NS4B، برز واحد: UBA5، إنزيم البداية لمسار UFMylation. UFMylation هو نظام خلوي يربط وسمًا بروتينيًا صغيرًا، UFM1، بأهداف مختارة، مؤثرًا في عمليات مثل مراقبة جودة البروتين والاستجابات للضغط الخلوي. باستخدام تدخل RNA والتقاطعات الجينية المعتمدة على CRISPR، أظهر الفريق أن الخلايا التي تفتقر إلى UBA5 أو غير قادرة على إجراء UFMylation تقل فيها قدرة تكاثر زيكا والفيروسات ذات الصلة بشكل كبير. إعادة إدخال UBA5 الطبيعي أعادت نمو الفيروس، بينما الأشكال الطافرة التي لم تعد قادرة على دفع UFMylation لم تفعل ذلك، مثبتة أن نشاط الوسم نفسه حاسم للعدوى.
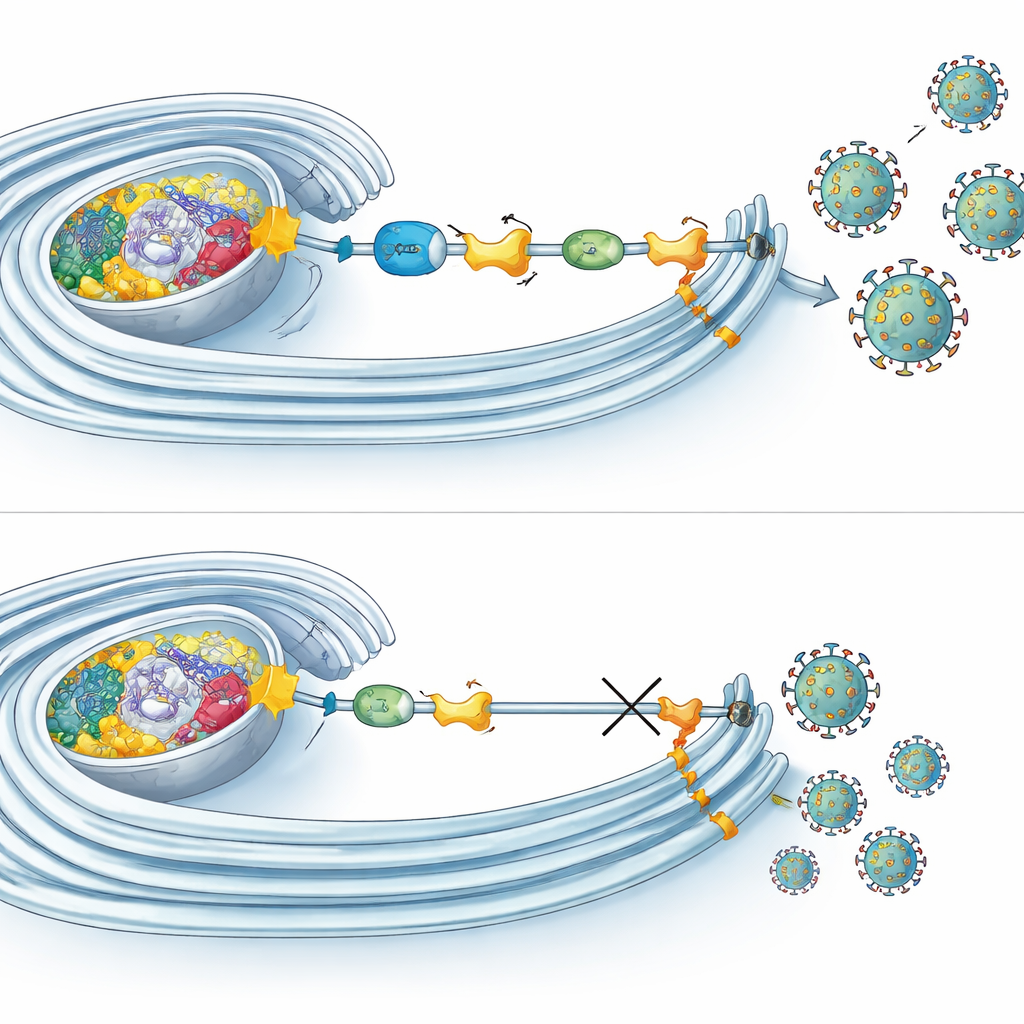
كيف يدعم الوسم مصانع الفيروس
كشفت تجارب المجهرية والتحليل الكيميائي الحيوي أن مكونات متعددة من نظام UFMylation تتجمع في الأماكن نفسها التي يُنسخ فيها الحمض النووي الريبي الفيروسي داخل أغشية مُعاد تشكيلها. هناك، ترتبط ليس فقط مع NS4B بل أيضًا مع بروتينات فيروسية أخرى تبني آلية التكاثر. من المثير أن حجب UFMylation لم يوقف دخول الفيروس أو إنتاج الحمض النووي الريبي أو تخليق البروتينات. بدلاً من ذلك، أضعف بشكل أساسي المراحل المتأخرة من الدورة، مثل تجميع أو إفراز الجسيمات المعدية. وفي الوقت نفسه، تبين أن UFMylation يؤثر على كيفية تنفس الميتوكوندريا: عندما تعطَّل المسار، أظهرت الخلايا استهلاكًا منخفضًا للأكسجين وأشكالًا متغيرة للميتوكوندريا. بالمقابل، في المراحل المبكرة من عدوى زيكا، ارتفع التنفس الميتوكوندري، مما يشير إلى أن الفيروسات قد تستغل UFMylation لتعزيز إنتاج الطاقة في الخلية عندما تكون في أمس الحاجة إليها.
اختبار دواء في خلايا وأسماك صغيرة
بعد ذلك توجه المؤلفون إلى مركب صغير الجزيء، DKM 2‑93، الذي يثبط الموقع النشط في UBA5. في خلايا بشرية مزروعة، خفّض هذا المثبط إنتاج فيروس زيكا بحوالي عشر مرات عند جرعات تركت الخلايا بصحة جيدة إلى حد كبير، وأظهر نشاطًا عبر أنواع خلايا متعددة. لرؤية ما إذا كانت هذه الاستراتيجية تعمل في كائن حي، استخدموا نموذج سمك الزебرا للعدوى بزيكا، والذي يحاكي سمات رئيسية من المرض في الدماغ النامي. أدى معالجة الأجنة المصابة بـ DKM 2‑93 أثناء تطور المخ المبكر إلى خفض مستويات الحمض النووي الريبي الفيروسي بشكل ملحوظ وتقليل نسبة الأسماك التي أظهرت تشوّهات شديدة، مشيرةً إلى فائدة مضادة للفيروسات حقيقية في الجسم الحي.
ماذا يعني هذا للعلاجات المستقبلية
عن طريق بناء خريطة شاملة لكيفية تفاعل NS4B من العديد من الأورثوفلافيفيروسات مع البروتينات البشرية، تبرز هذه الدراسة UFMylation كمسار مساعد محفوظ تعتمد عليه هذه الفيروسات لإنتاج جزيئات معدية. ولأن نفس النظام الخلوي يبدو أنه يدعم الضنك وزيكا وغرب النيل وغيرهم، قد تعمل الأدوية التي تُضعف UFMylation بصورة انتقائية كمضادات فيروسات واسعة النطاق، بدلاً من استهداف فيروس واحد في كل مرة. وعلى الرغم من الحاجة لمزيد من العمل لفهم بالضبط أي البروتينات تُوسَم ولضمان السلامة، تحدد النتائج هدفًا واعدًا معتمدًا على العائل قد يساعد يومًا ما في تخفيف اندلاع عدة أمراض منقولة بواسطة البعوض والقراد باتباع نهج علاجي واحد.
الاستشهاد: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
الكلمات المفتاحية: فيروس زيكا, حمى الضنك, تفاعلات العائل–الفيروس, UFMylation, مضادات فيروسات واسعة النطاق