Clear Sky Science · ar
تنشيط متزامن للخلايا العصبية الأستيل كولينيرية في المخطط يؤدي إلى إفراز محلي للسيروتونين
لماذا تهم هذه الاكتشافات الكيميائية في الدماغ
العادات والدافعية والسلوكيات القهرية كلها تعتمد على منطقة دماغية صغيرة لكنها حيوية تُسمى المخطط. رسالتان معروفَتان في الدماغ، الدوبامين والسيروتونين، تساعدان في ضبط هذه المنطقة، وتسعى العديد من الأدوية النفسية إلى تعديل توازنهما. تكشف هذه الدراسة عن خط تواصل مخفي سابقًا: فصيلة خاصة من الخلايا العصبية التي تفرز الأستيل كولين يمكنها أن تتصل مباشرة بألياف السيروتونين وتدفعها لإفراز المزيد من السيروتونين، لكن ذلك يحدث فقط في جزء محدد من المخطط. قد يساعد هذا الرابط الجديد في تفسير سبب تداخل اضطرابات مثل الوسواس القهري ومرض باركنسون مع تغيّرات معقدة في عدة ناقلات عصبية في وقت واحد.
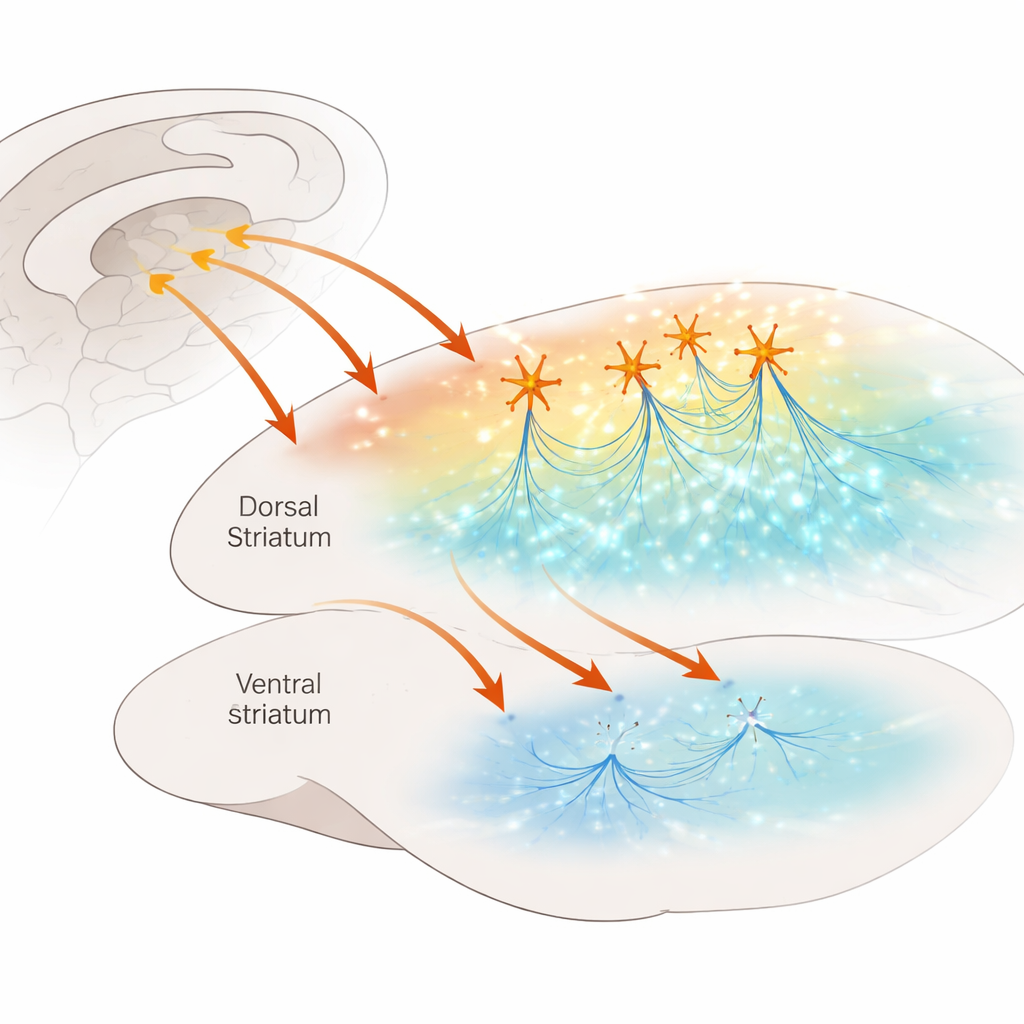
تقاطع مزدحم في الدماغ
يعمل المخطط الظهري كمحور اتخاذ قرار، يساعدنا على التحول بين الأفعال الموجهة نحو هدف والعادات التلقائية. يتلقى مدخلاً كثيفًا من القشرة ويُغمر بمعدِّلات عصبية مثل الدوبامين والسيروتونين، التي تضبط كيفية معالجة الإشارات. ضمن هذا المحور توجد مجموعة قليلة لكن قوية من الخلايا العصبية الداخلية الأستيل كولينيرية—خلايا تفرز الأستيل كولين وتطلق إشارات بانتظام مثل ميترو نوم صغير. أظهرت أعمال سابقة أنه عندما تطلق هذه الخلايا معًا، يمكنها زيادة إطلاق الدوبامين بقوة عبر العمل على مستقبلات النيكوتين الأستيل كولينية الموجودة على ألياف الدوبامين. أما ما إذا كان هناك طريق مختصر مشابه للسيروتونين فكان غير معلوم، رغم أن السيروتونين مركزي للمزاج والتعلم وتأثيرات الأدوية المستخدمة في علاج الوسواس القهري والاكتئاب.
مراقبة إنارة السيروتونين في الزمن الحقيقي
لمعالجة هذا السؤال، استخدم الباحثون فئرانًا مزودة بمستشعر فلوري يلمع أكثر عندما يوجد السيروتونين. حقنوا فيروسًا يحمل هذا المستشعر في المخطط، أعدّوا شرائح رقيقة من الدماغ، ثم استخدموا مجهر ثنائي الفوتون لمراقبة إشارات السيروتونين أثناء تحفيز النسيج. أدى التحفيز الكهربائي داخل المخطط الظهري إلى ومضات واضحة من نشاط المستشعر تتلاشى ببطء. عندما طبّق الفريق دواءً يعيق مستقبلات النيكوتين الأستيل كولينية، تقلصت هذه الومضات وأصبحت أكثر محلية، مما يشير إلى أن الأستيل كولين عبر هذه المستقبلات يساعد على زيادة إفراز السيروتونين ونشره على مساحة أوسع. والمثير أن إجراء نفس التجربة في المخطط البطني—منطقة مجاورة ذات توصيل سيروتونيني أكثر كثافة—لم يظهر مساهمة نيكوتينية، كاشفًا أن هذا الحوار المتبادل محدد إقليميًا.
إثارة السيروتونين بضوء موجه
لكشف ما إذا كان الأستيل كولين من الخلايا الداخلية الأستيل كولينيرية وحده قادرًا على دفع إفراز السيروتونين، لجأ المؤلفون إلى البصريات الوراثية (أوبتوغينيتيكس). عدّلوا هذه الخلايا لتستجيب لومضات قصيرة من الضوء الأزرق أو الأصفر ونشطوها بتزامن بينما استمروا في مراقبة المستشعر السيروتونيني. كانت مليون جزء من الثانية الواحدة (ميلي ثانية واحدة) من الضوء كافية لإثارة إشارة سيروتونين قوية في المخطط الظهري، ذات مسار زمني مشابه للمكوِّن الحساس للنيكوتين في الاستجابة المستحثة كهربائيًا. أدى حجب مستقبلات النيكوتين إلى إلغاء هذه الإشارة تقريبًا، حتى عندما تم كبت المدخلات الكيميائية والمستقبلات الأخرى في الشريحة دوائيًا. أظهرت هذه المجموعة من التحفيز الدقيق وحجب المستقبلات أن الأستيل كولين يعمل مباشرة على مستقبلات النيكوتين على طول ألياف السيروتونين لتحفيز إفراز السيروتونين المحلي، بدلًا من الاعتماد على طرق غير مباشرة عبر أنواع خلايا أخرى أو محاور الدوبامين.
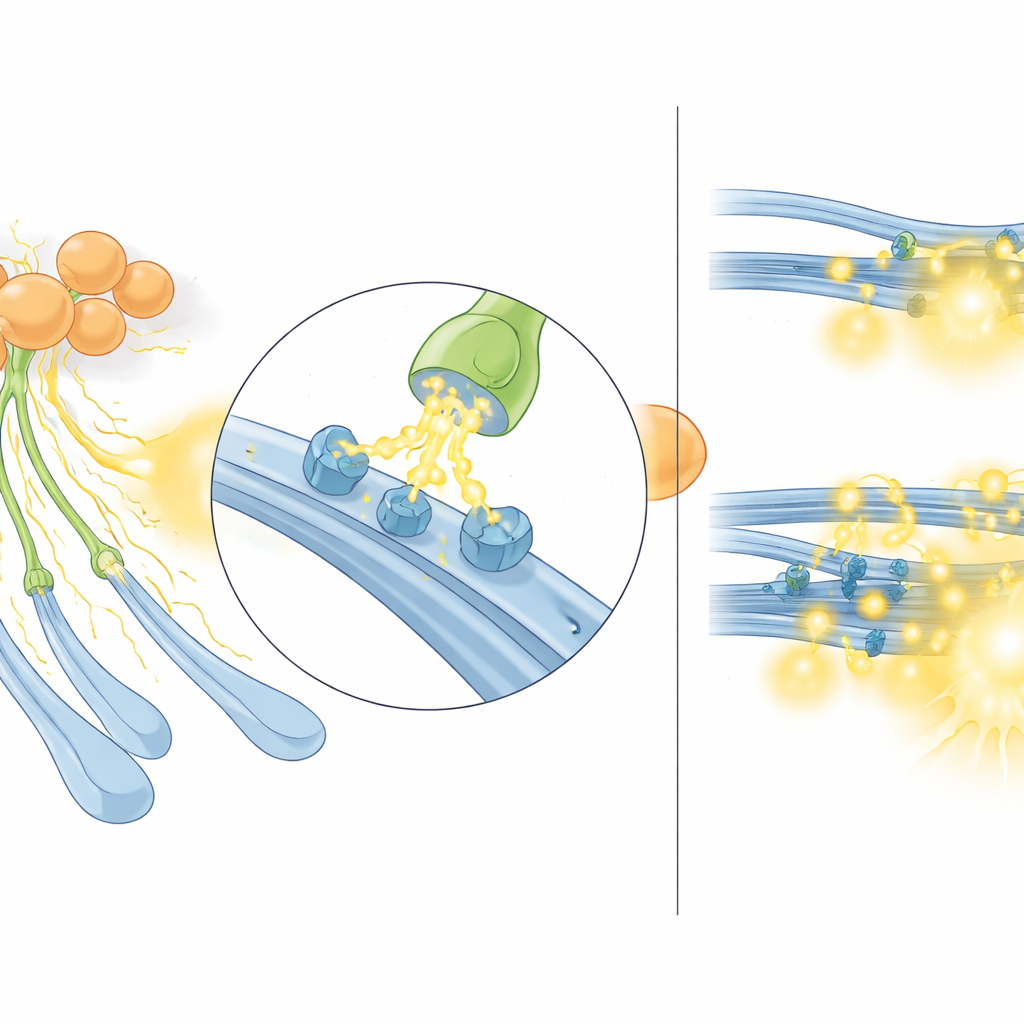
عندما يسخن النظام أكثر من اللازم
سأل الفريق بعد ذلك ماذا يحدث في حالة مرضية ذات صلة حيث يكون إشارات الأستيل كولين قوية بشكل غير طبيعي. استخدموا فئرانًا مُعدَّلة جينياً تفتقر إلى جين Sapap3، وهو نموذج راسخ يُظهر تمشيطًا مفرطًا وسلوكيات شبيهة بالوسواس القهري، وقد أُظهر سابقًا أنها تملك خلايا داخلية أستيل كولينيرية أكثر نشاطًا وإفرازًا أعظم للأستيل كولين. في هذه الفئران، أنتج التحفيز الكهربائي للمخطط الظهري إشارات مستشعر سيروتونين أكبر من تلك في الحيوانات الطبيعية. والأهم أن هذا الاختلاف اختفى عندما حُجبت مستقبلات النيكوتين، مما يعني أن الجزء المعتمد على الأستيل كولين فقط من إفراز السيروتونين كان هو الذي تعاظم. وظهرت نمطية مماثلة للدوبامين. بعبارة أخرى، في هذه الحالة الفائقة الأستيل كولين، تضخم الخلايا الداخلية الأستيل كولينيرية مكون النيكوتين من إفراز أحادي الأمين بشكل غير متناسب، مما يسمح فعليًا للأستيل كولين "باختطاف" ألياف السيروتونين كمسار رئيسي لإخراج السيروتونين.
تداعيات أوسع على اضطرابات الدماغ
تكشف هذه النتائج عن حوار مضبوط بدقة ومحدد إقليميًا بين الأستيل كولين والسيروتونين في المخطط الظهري. في الأدمغة السليمة، قد تؤدي دفعات متزامنة من نشاط الخلايا الداخلية الأستيل كولينيرية—مثل تلك الناتجة عن أحداث مفاجئة ومهمة سلوكيًا—إلى توسيع وتقوية إشارات السيروتونين مؤقتًا، مُشكّلةً كيفية تعلم الأفعال أو قمعها. في الحالات المرضية حيث يكون الأستيل كولين مرتفعًا باستمرار، كما في فئران Sapap3 وربما في حالات مثل الوسواس القهري أو مرض باركنسون، قد يتضخم نفس الآلية، مساهِمة في أنماط غير طبيعية لإشارات السيروتونين والدوبامين. إن فهم هذا الرابط الخفي يقدم طريقة جديدة للتفكير بكيفية تفاعل عدة معدِّلات عصبية في السلوك الطبيعي والمرض، وقد يشير في نهاية المطاف إلى علاجات تستهدف تداخلهما الديناميكي بدقة أكبر بدل معاملة كل ناقل على حدة.
الاستشهاد: Matityahu, L., Hobel, Z.B., Berkowitz, N. et al. Synchronous activation of striatal cholinergic interneurons induces local serotonin release. Nat Commun 17, 2278 (2026). https://doi.org/10.1038/s41467-026-70359-6
الكلمات المفتاحية: سيروتونين المخطط, الخلايا العصبية الداخلية الأستيل كولينيرية, مستقبلات النيكوتين للأستيل كولين, اضطراب الوسواس القهري, العقد القاعدية