Clear Sky Science · ar
التحكم في وظيفة الليزوزوم بواسطة بروتين تنشيط الجي تي بيازات TBC1D9B وشريكه الواصل TMEM55B
كيف تحافظ مراكز إعادة التدوير الخلوية على التوازن
داخل كل خلية منا توجد أكياس صغيرة تسمى الليزوزومات تعمل كمراكز لإعادة التدوير ومحاور تحكم للنمو. عندما تعمل بشكل جيد، تُفكك الأجزاء المتهالكة وتُعاد استخدام مكوناتها؛ وعندما تفشل، تتراكم النفايات وقد تظهر أمراض، بما في ذلك الاضطرابات العصبية التنكسية والسرطان. تكشف هذه الدراسة كيف يساعد بروتينان غير معروفين كثيراً على تبديل الليزوزومات بين حالة تجوال داعمة للنمو وحالة متكتلة مخصصة لإزالة النفايات، ما يسلط الضوء على كيفية تكيّف الخلايا مع الوفرة والجوع.
نقل مراكز إعادة التدوير داخل الخلية
الليزوزومات ليست ثابتة في مكانها. إنها تسير على مسارات داخلية، تُجر إلى الخارج بواسطة مجموعة من المحركات الجزيئية وتُسحب إلى الداخل بواسطة مجموعة أخرى. لموقعها داخل الخلية أهمية: عندما تكون المغذيات متاحة بكثرة، تنتشر الليزوزومات نحو مناطق الخلية الخارجية وتدعم إشارات النمو؛ وعندما يكون الطعام نادراً، تتراجع إلى المركز، تصبح أكثر حموضة، وتزيد من كفاءة تحلل المواد الخلوية. كان معروفاً أن بروتين صغير يشبه المفتاح يُدعى ARL8 يدفع الليزوزومات إلى الخارج، لكن حتى الآن لم يُحدد نظام فرملة مخصص لكبحه. افترض المؤلفون أن مثل هذه الفرملة ستكون حاسمة لتمكين الخلايا من التحول بسرعة إلى وضع الحفظ أثناء الجوع.
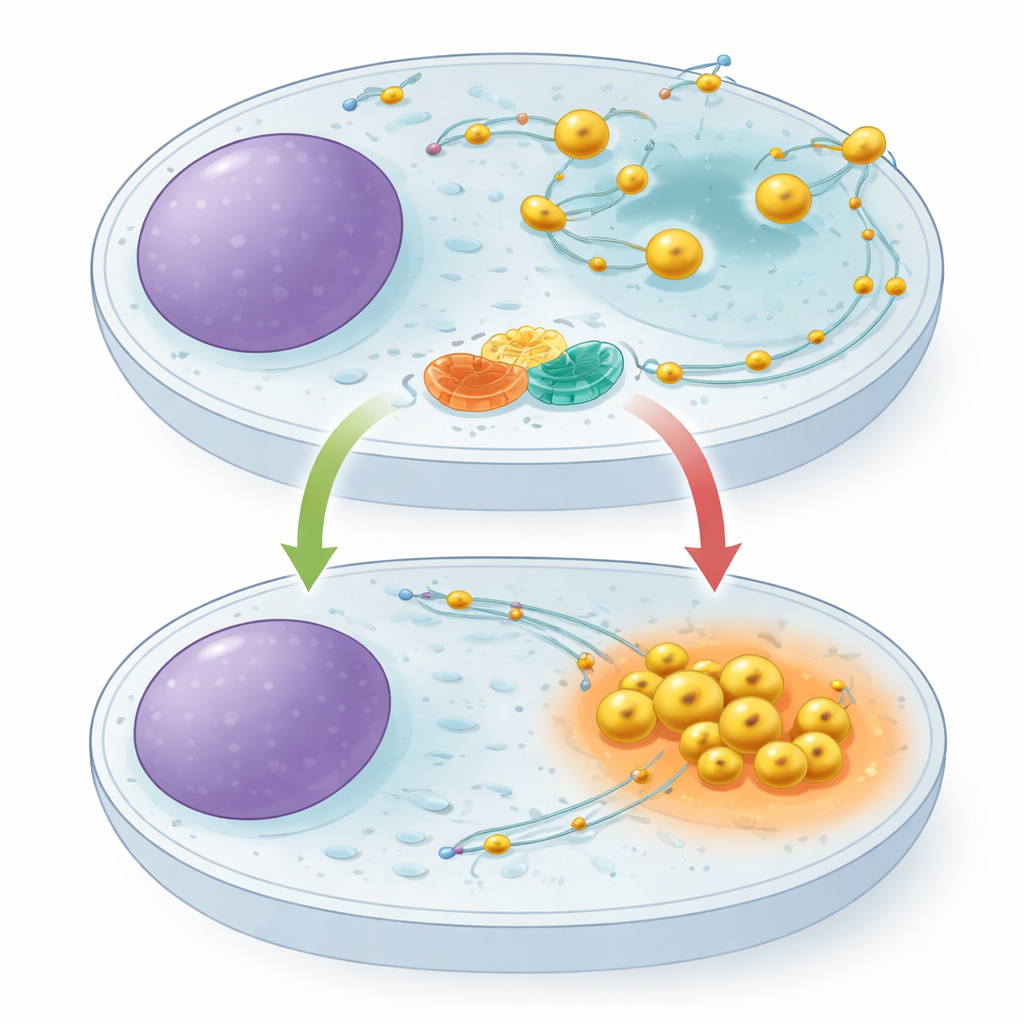
شراكة جزيئية على سطح الليزوزوم
باستخدام تقنيات صيد البروتينات والقياس الطيفي الكتلي، اكتشف الباحثون أن بروتيناً اسمه TBC1D9B يرتبط ببروتين غشائي لليزوزوم يُدعى TMEM55B. يجلس TMEM55B عبر الغلاف الخارجي لليزوزوم، بينما يكون TBC1D9B قابل الذوبان إلى حد كبير ويمكنه الالتحام بالغشاء. أظهر الفريق أن هذين البروتينين يشكلان معقداً مباشراً: يلتصق TBC1D9B المطهر بالجزء المكشوف من TMEM55B في أنابيب الاختبار، وتستخرج النسخ المعلّمة من البروتينين بعضها البعض من مستخلصات الخلايا. كشفت خرائط دقيقة لمقاطع البروتين أن عدة مناطق من TBC1D9B تتلامس مع TMEM55B، مما يضع TBC1D9B على سطح الليزوزوم دون أن يحجب الجزء المسؤول عن نشاطه التحفيزي.
عندما تفشل الفرملة، تتوحش الليزوزومات
لاكتشاف ما يقوم به هذا التعاون، استخدم المؤلفون تعديل CRISPR لإزالة TMEM55B أو TBC1D9B من الخلايا البشرية. في كلتا الحالتين، لم تعد الليزوزومات تتجمع قرب النواة بل تفرّقَت نحو حافة الخلية وتحركت أسرع على طول مساراتها، مما يحاكي حالة الخلايا في وضع التغذية المستمر. أعادت إعادة إدخال TBC1D9B الطبيعي توطينها بشكل صحيح، لكن نسخة تفتقر إلى القدرة التحفيزية لم تفعل ذلك، مما يشير إلى أن نشاطها الإنزيمي ضروري. عند تجويع الخلايا، سحبت الخلايا الضابطة الليزوزومات إلى الداخل وعززت قوتها الهاضمة، كما أظهرته زيادة نشاط الإنزيمات الأساسية وتحسين تحلل الحمولة الاختبارية. فشلت الخلايا التي تفتقد TMEM55B أو TBC1D9B في القيام بذلك: بقيت ليزوزوماتها طرفية وكان استجابتها التحليلية للجوع مُضعفة. كما تضررت البلعمة الذاتية، العملية التي تلتهم فيها الخلايا مكوناتها التالفة، مع معالجة أقل كفاءة لمؤشر البلعمة الذاتية وتراكم بروتين المرافق p62.
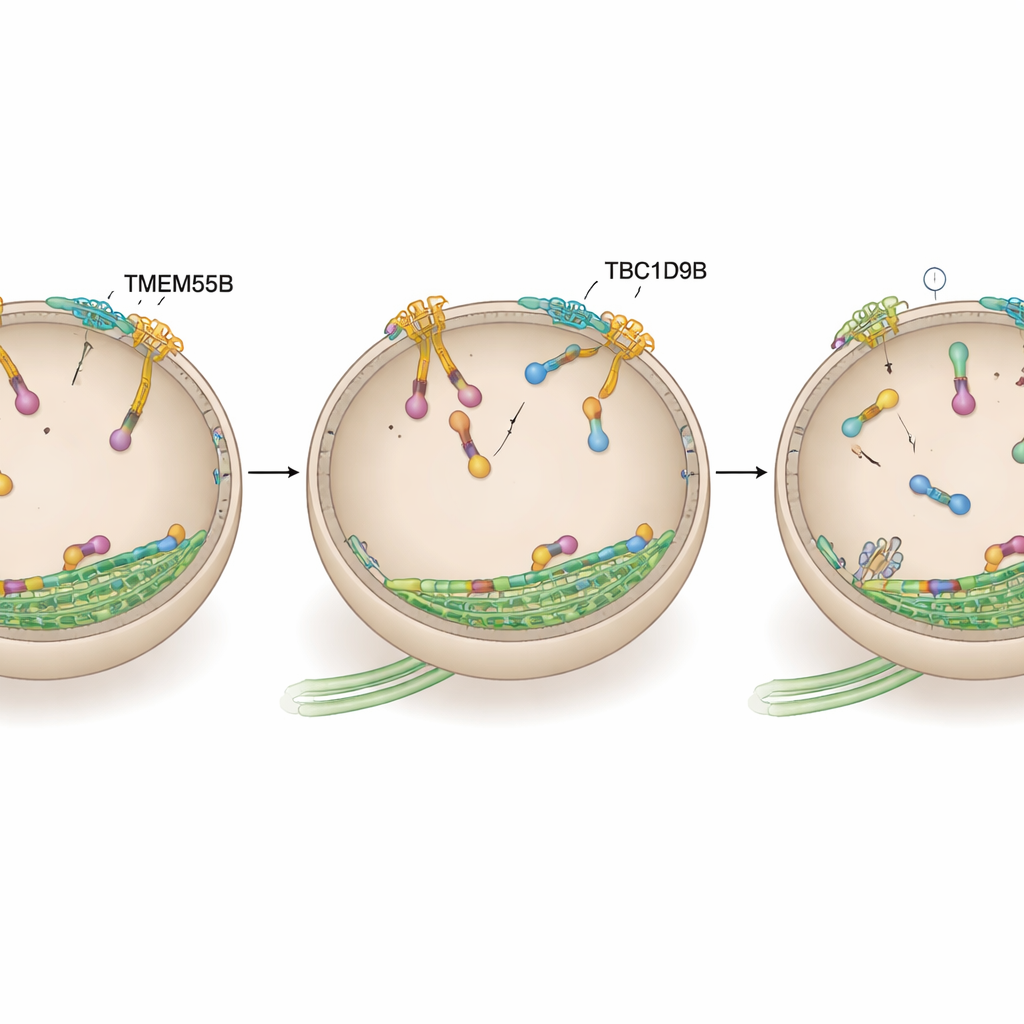
إيقاف محرك الليزوزوم
سأل الفريق بعد ذلك ما إذا كان TBC1D9B يمارس تأثيره عن طريق العمل مباشرة على ARL8، مفتاح تشغيل المحرك الخارجي. باستخدام وسم التقارب في الخلايا العصبية البشرية واختبارات الارتباط في خطوط خلوية وبروتينات منظفة، أظهروا أن TBC1D9B يرتبط انتقائياً بالشكل النشط المحمّل بالجيو تي بي (GTP) من متغير ARL8B، لكنه لا يرتبط بالشكل غير النشط أو بالنسخة القريبة ARL8A. تنبأ النمذجة الهيكلية بأن بقايا رئيسية في TBC1D9B تلامس جيب الجيو تي بي في ARL8B. في اختبارات كيميائية حيوية، سرّع TBC1D9B تحلل الجيو تي بي المرتبط بـ ARL8B، محولاً بذلك البروتين من حالة "تشغيل" إلى حالة "إيقاف"؛ ولم يعد بالإمكان ذلك من قِبل نسخة طفورية من TBC1D9B تفتقد هذه البقايا. تماشياً مع ذلك، أظهرت الخلايا التي تفتقد TMEM55B أو TBC1D9B زيادة في ARL8B على الليزوزومات، بينما أدى إفراط التعبير عن TBC1D9B إلى سحب الليزوزومات نحو المركز، شبيهاً بخفض نشاط ARL8B.
مقبض ضبط جديد لصيانة الخلية
أخيراً، اختبر المؤلفون ما إذا كانت هذه الفرملة على ARL8B تفسر التغيرات الخلوية المرصودة عند فقدان TBC1D9B. عند نقص ARL8B، بقيت الليزوزومات متجمعة قرب النواة بغض النظر عن وجود TMEM55B أو TBC1D9B، وتم تجاوز العيوب في البلعمة الذاتية الناجمة عن فقدان TBC1D9B إلى حد كبير. تدعم البيانات مجتمعة نموذجاً يفيد بأن TMEM55B يجند TBC1D9B إلى الليزوزومات حيث يثبط ARL8B ويسمح لليزوزومات بالتحول من حالة متناثرة داعمة للنمو إلى حالة مركزية مكرّسة للهضم. للمختصين غير المتخصصين، يعني ذلك أن الدراسة كشفت مقبض ضبط مهم تستخدمه الخلايا لتحديد متى تعيد التدوير بشكل أكثر نشاطاً، وهي عملية لها آثار على اضطرابات تراكم النفايات في الدماغ والأيض والسرطان.
الاستشهاد: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
الكلمات المفتاحية: الليزوزومات, البلعمة الذاتية, إشارة خلوية, نقل العضيات, الاضطرابات العصبية التنكسية