Clear Sky Science · ar
تنشيط NF-κB في الخلايا النجميّة يعيق شفاء الجروح بعد إصابة الدماغ الرضحية في ذكور الفئران
لماذا لا تلتئم رضوض الدماغ دائمًا بشكل نظيف
عندما يتلقى شخص ضربة على الرأس، فإن الضرر الظاهر على السطح هو جزء فقط من القصة. في أعماق الدماغ يحدث استجابة شفاء معقّدة يمكن أن تحدد ما إذا كان الشخص سيتعافى جيدًا أم ستظهر له مشاكل دائمة في التفكير أو المزاج أو الحركة. تكشف هذه الدراسة في ذكور الفئران كيف يمكن لمسار ضغط حيوي داخل خلايا الدعم المسماة الخلايا النجمية أن يحول استجابة شفاء طبيعية إلى استجابة تزيد الضرر بعد إصابة الدماغ الرضحية.
المستجيبون الأوائل الخفيون في الدماغ
الخلايا النجمية على شكل نجمة تحيط بالخلايا العصبية والأوعية الدموية، وتساعد في الحفاظ على استقرار البيئة الداخلية للدماغ. بعد إصابة في الرأس، تغير شكلها وسلوكها بسرعة، وتشكل حاجزًا حول المنطقة المتضررة وتساهم في إعادة بناء النسيج. ركز الباحثون على مفتاح جزيئي داخل هذه الخلايا يسمى NF-κB، المعروف بدوره في تنظيم الالتهاب في أنسجة متعددة. تساءلوا عما إذا كان هذا المفتاح بعد إصابة مغلقة في الرأس تشبه الارتجاجات والكدمات الشائعة لدى البشر يساعد أو يضُر قدرة الدماغ على الشفاء.
مفتاح الضغط الذي ينشط بعد الصدمة
من خلال تحليل نشاط الجينات في نسيج دماغ الفئران بعد الإصابة، وجد الفريق ارتفاعًا في الجينات المرتبطة بالالتهاب وإشارات NF-κB، خصوصًا بين اليوم الثالث والسابع بعد الصدمة، عندما تتسارع الأضرار الثانوية. باستخدام فئران مزوّدة بمؤشرات تقريرية، أظهروا أن تنشيط NF-κB لم يكن منتشرًا في الدماغ بأكمله بل تركز حول موقع التأثير. هناك، كان نشطًا بشكل خاص في الخلايا البلعمية الصغيرة (حرس الجهاز المناعي في الدماغ) وفي الخلايا النجمية التي تشكل حافة الجرح. أوحت هذه التوقيتات والمواقع بأن NF-κB في الخلايا النجمية قد يكون منظّمًا حاسمًا لكيفية تنظيم الدماغ لندبته وضبط استجابته المناعية.
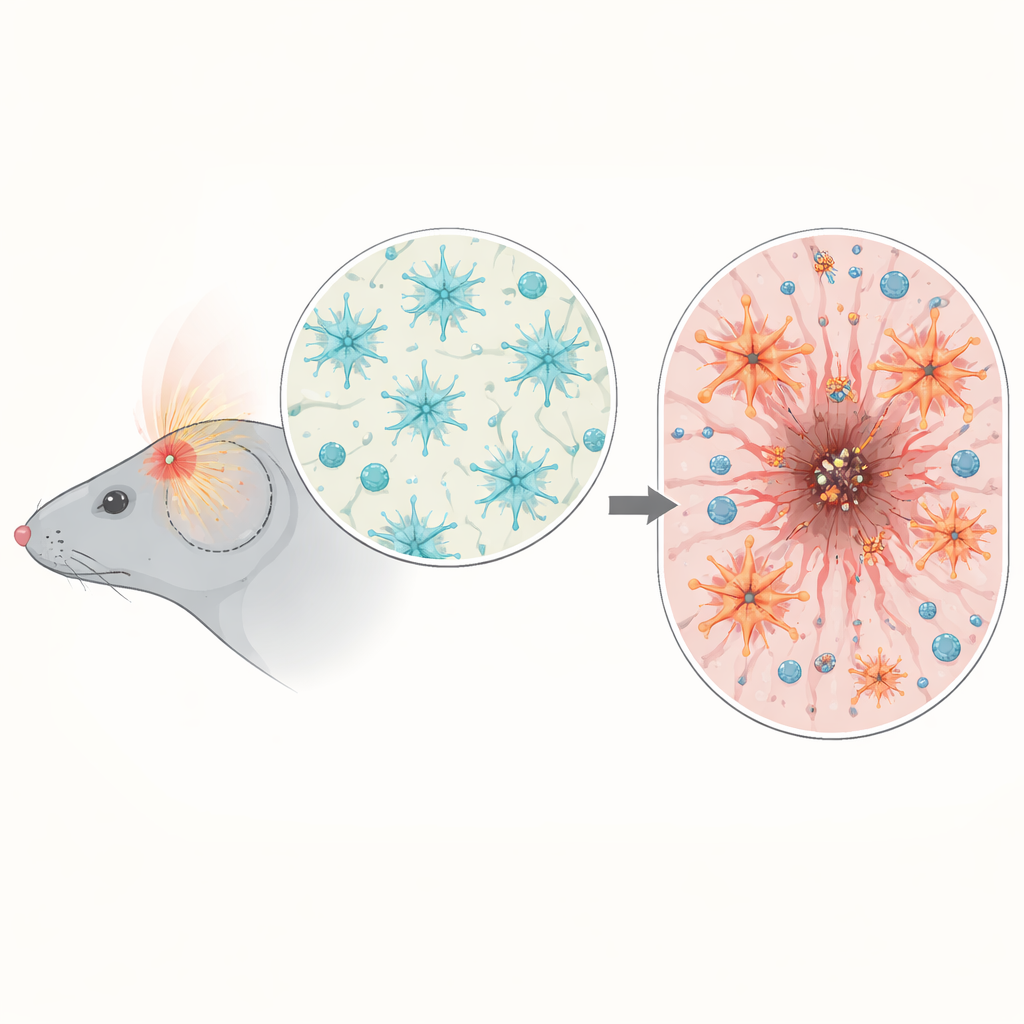
تشديد نشاط الخلايا النجمية إلى حد مفرط
لاختبار السببية، هندس العلماء فئرانًا تجعل NF-κB في الخلايا النجمية إما معزَّزًا صناعيًا أو مكبوحًا، ولكن فقط بعد اكتمال نمو الدماغ. عندما تعرضت هذه الفئران لصدمة في الرأس، فقدت الفئران ذات NF-κB المفرط النشاط في الخلايا النجمية وزنًا أكبر، وأظهرت درجات عصبية مبكرة أسوأ، وكانت لديها آفات دماغية أكبر وأكثر دوامًا في مقاطع الأنسجة وصور الرنين المغناطيسي. بدلًا من تكوين ندبة مرتبة ومحددة تحيط بالنواة المتضررة، أنتجت خلاياهم النجمية حدًا سميكًا وفوضويًا فشل في تضييق الجرح مع مرور الوقت. تعكّر التوازن الطبيعي لبروتينات مصفوفة الدعم حول الإصابة، وتكوّن هيكل حاجز خارجي رئيسي معروف بالحد الغلِيّ ليْفِي (glial limitans) بشكل سيئ، مما ترك الدماغ المحيط أقل حماية.
عندما تنحرف برامج الشفاء عن مسارها
غوصًا في التفاصيل الجزيئية، عزل الفريق الخلايا النجمية والخلايا المناعية القريبة لتحليل جيني تفصيليًا. في الحيوانات السليمة، تُكبَت بعض وظائف الخلايا النجمية اليومية بعد الإصابة بينما تُشغَّل جينات تدعم إغلاق الجروح والتجدد. على النقيض، بدت الخلايا النجمية ذات NF-κB النشط بشكل مزمن «مصابة» حتى قبل الصدمة، وبعد التأثير فشلت في تفعيل برامج الإصلاح المفيدة بالكامل مثل التحولات المنظمة التي تساعد الخلايا على بناء حد فعال. بدلًا من ذلك، فضّلت بقوة الجينات الالتهابية، وتبنّت سمات حالة خلوية نَسِمَت بالسمّية المرتبطة بالتقدم في السن والأمراض التنكسية العصبية، وأظهرت مؤشرات لملف إفرازي شبيه بالشيخوخة مرتبط بالجروح المزمنة غير المتحللة.
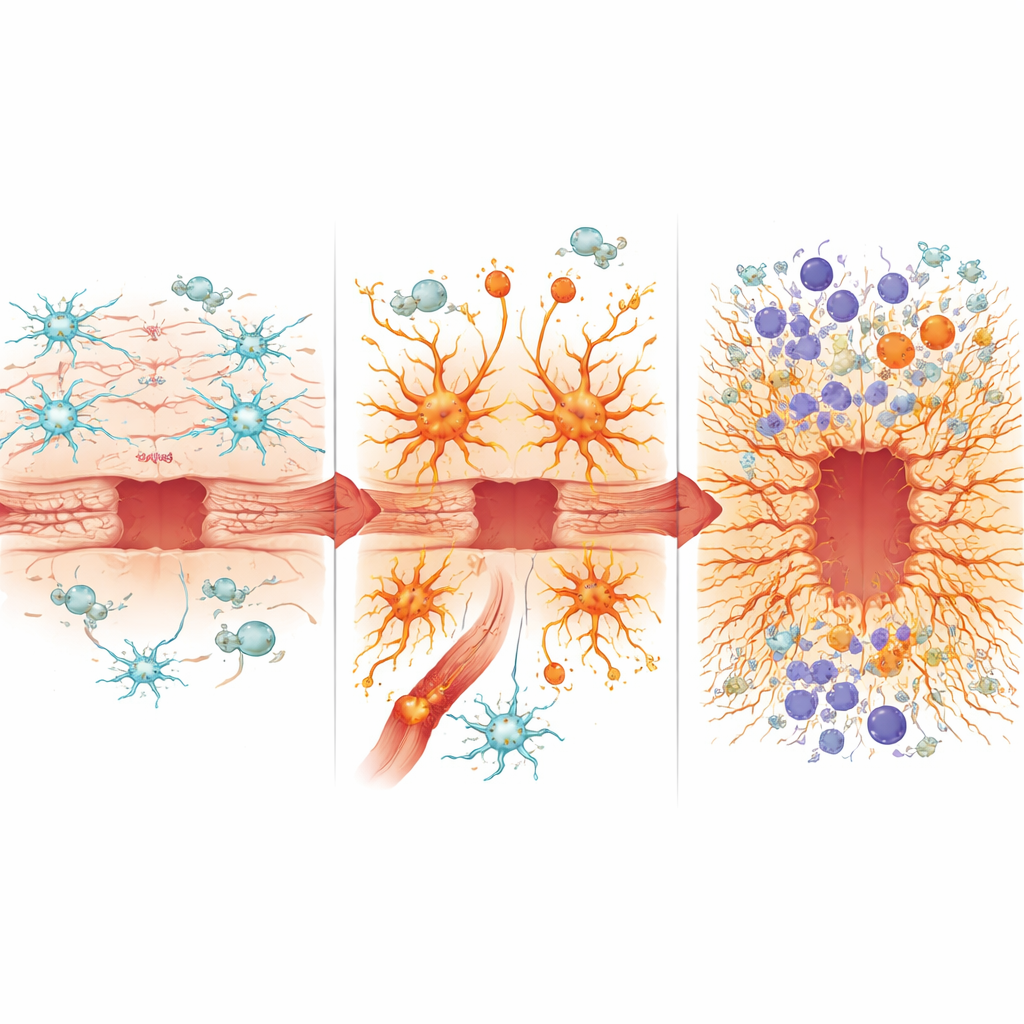
تأجيج نار الاستجابة المناعية
أعادت هذه الخلايا النجمية المبرمجة بشكل خاطئ أيضًا تشكيل المشهد المناعي في الدماغ. أصبح الحاجز الدماغي الدموي أكثر تسربًا، مما سمح بدخول مزيد من الخلايا المناعية المحيطية. أظهرت الفئران ذات NF-κB المفرط النشاط في الخلايا النجمية تسللًا أكبر لخلايا نَخاعية التهابية وتغيرات في نسب العدلات والوحيدات والخلايا الشجرية، بالإضافة إلى زيادة في الخلايا التائية السامة للخلايا التي قد تلحق مزيدًا من الضرر بالنسيج. عبرت الخلايا المناعية في هذا المحيط عن إشارات أقوى يقودها الإنترفيرون ومسارات الإنفلاماسوم، المرتبطة بالالتهاب العدواني وقد يكون عصبيًا سامًا. في الوقت نفسه، انخفضت مستويات عدة بروتينات واقية أو محفزة للإصلاح، مثل الأوستيوπόνتين، بينما ارتفعت بروتينات مرتبطة بالإجهاد التأكسدي وحمل الحديد والتندب، بما في ذلك هيم أوكسجيناز-1 وليبوكانين-2. برزت النسبة بين الأوستيوπόνتين ولبوكانين-2 كمؤشر بسيط يتتبع الشفاء الأفضل أو الأسوأ بين سلالات الفئران المختلفة.
ماذا يعني هذا لتعافٍ من إصابات الرأس
تُظهر النتائج معًا أنه عندما يكون مسار الضغط NF-κB في الخلايا النجمية مرفوعًا باستمرار، تتحول هذه الخلايا من داعمة للإصلاح المنظم إلى محركة لتندب فوضوي والالتهاب المطوّل. بدلًا من بناء حد نظيف يحتوي التلف ويسمح بإعادة تشكيل النسيج، تساهم في خلق موضع متسرب وملتهب يوسع الآفة ويقوّض النتيجة على المدى الطويل. وعلى الرغم من أن العمل أُجري في ذكور الفئران، فإنه يشير إلى NF-κB في الخلايا النجمية كهدف واعد للعلاجات التي تهدف إلى تحسين التعافي بعد إصابة الدماغ الرضحية ويقترح أن مستويات جزيئات مثل الأوستيوπόνتين ولبوكانين-2 في الدم قد تساعد يومًا ما الأطباء على مراقبة مدى نجاعة شفاء دماغ المريض.
الاستشهاد: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
الكلمات المفتاحية: إصابة الدماغ الرضحية, الخلايا النجمية, الالتهاب العصبي, تشكّل ندبة الدماغ, NF-كابا B