Clear Sky Science · ar
انتقال معتمد على دورة الخلية من الأسيتيليشن إلى الفسفرة ينظم نضج المراكز في الوقت المناسب
الحفاظ على شحنتنا الوراثية على المسار الصحيح
في كل مرة تنقسم خلية في أجسامنا، يجب أن توزّع حمضها النووي بدقة متناهية. عندما يسوء هذا الإجراء، قد تكسب الخلايا أو تفقد كروموسومات، وهو وضع خطير مرتبط بالسرطان وأمراض أخرى. تكشف هذه الدراسة عن جهاز توقيت جزيئي يساعد الخلايا على بناء البُنى الصغيرة اللازمة لفصل الكروموسومات بشكل صحيح، كاشفة عن نقطة ضعف محتملة قد تستغلها علاجات مكافحة السرطان المستقبلية.
مراكز الحركة الصغيرة داخل الخلية
في قلب كل خلية منقسمة توجد المراكز، هياكل صغيرة تعمل كمحاور للحركة للألياف التي تسحب الكروموسومات بعيدًا عن بعضها. قبل أن تدخل الخلية في الانقسام، يجب أن "تنضج" هذه المحاور: تزداد فيها البروتينات المساعدة وتصبح منظّمات قوية للأنابيب الدقيقة، الألياف الديناميكية التي تشكّل المغزل الانقسامي. إذا حدث هذا النضج مبكرًا جدًا أو متأخرًا جدًا أو لم يحدث على الإطلاق، فقد تُوزع الكروموسومات بشكل خاطئ، مما يؤدي إلى خلايا ذات أعداد كروموسومات غير طبيعية. كان فهم كيفية تشغيل الخلايا للمراكز في اللحظة المناسبة سؤالًا طويل الأمد في بيولوجيا الخلية.
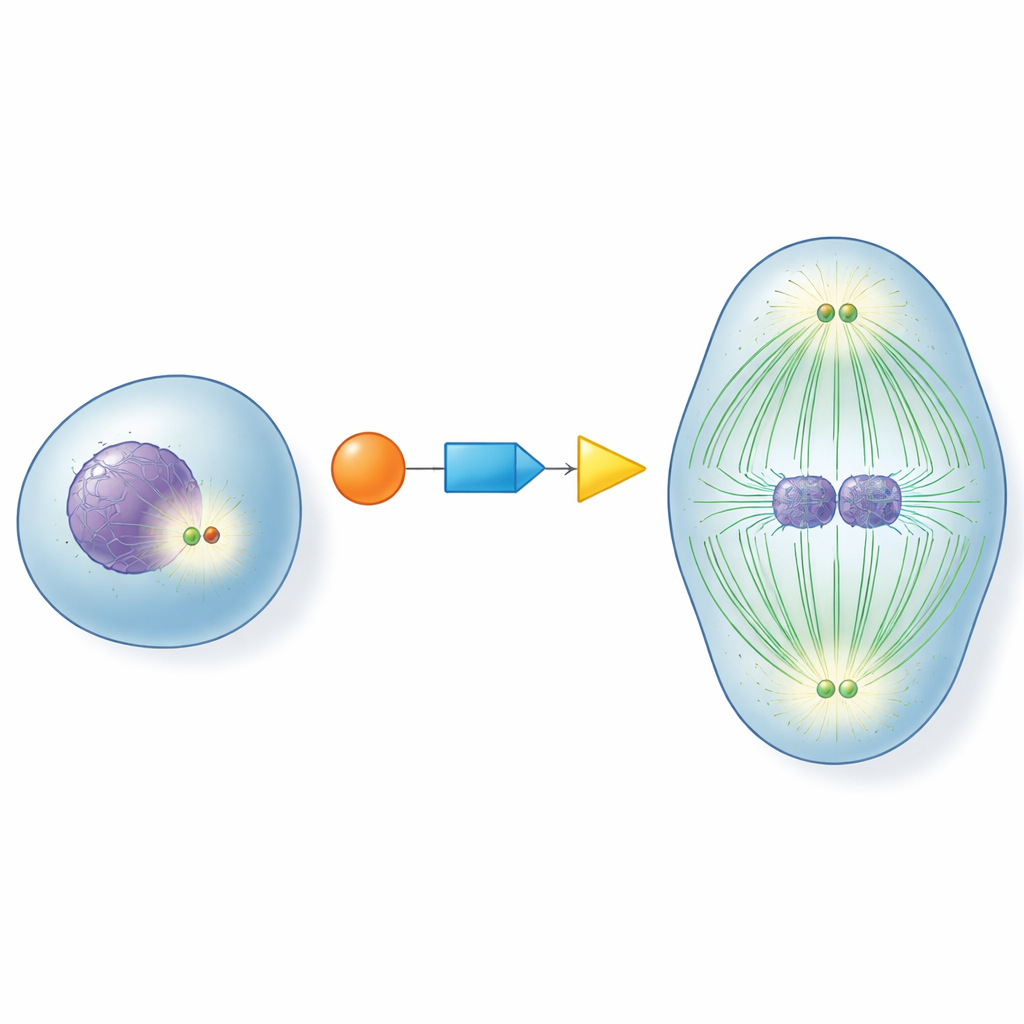
تتابع جزيئي للتوقيت المثالي
ركز المؤلفون على ثلاثة بروتينات رئيسية تعمل معًا كتتابع: CDK1، المتحكم الرئيسي في دورة الخلية؛ RNF40، المعروف سابقًا أساسًا بتعديل بروتينات تغليف الحمض النووي؛ وPLK1، محرك رئيسي للانقسام الخلوي. اكتشفوا أن RNF40 يتواجد فعليًا في المراكز طوال دورة الخلية ويرتبط مباشرةً بـPLK1. مع اقتراب الخلايا من الانقسام، يضع CDK1 علامات كيميائية على RNF40 في موقعين محددين، مما يجعل RNF40 موقع إرساء أفضل لـPLK1. يضمن هذا السلسلة CDK1–RNF40–PLK1 وصول PLK1 إلى المراكز بدقة خلال المرحلة المتأخرة من التحضير للانقسام، مما يحفز نضج المراكز بشكل قوي، ونمو الأنابيب الدقيقة، وتكوين مغزل ثنائي القطب مكتمل.
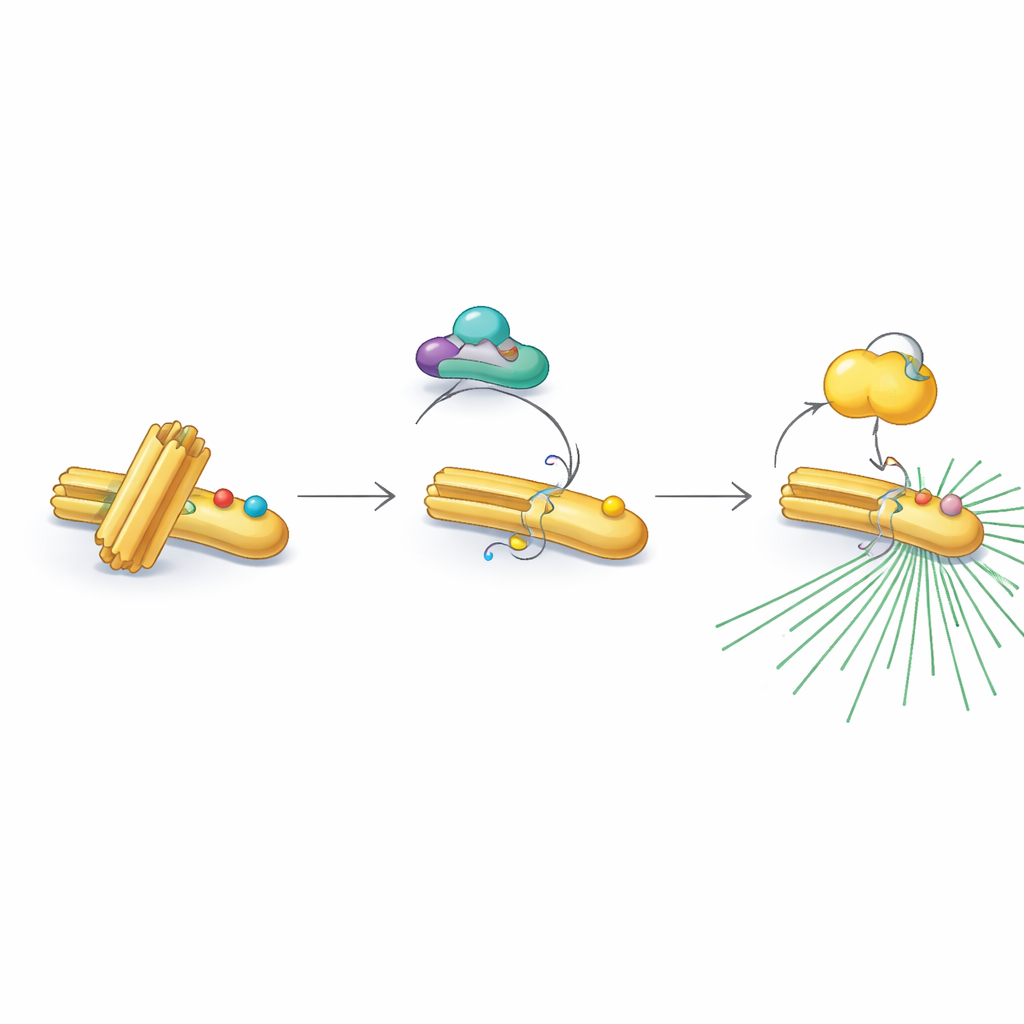
مفتاح بروتيني يغيّر شكله
من المثير أن RNF40 لا يقبل هذه العلامات المنشطة دائمًا. في المراحل غير المنقسمة ومراحل نسخ الحمض النووي، يحمل RNF40 زخرفة كيميائية مختلفة—مجموعات أسيتيلا—على موضعين متجاورين. تُضاف هذه العلامات الأسيتيليّة بواسطة إنزيم يُدعى PCAF وتُزال لاحقًا بواسطة شريك مزيل للأسيتيلا، HDAC1. النسخة الأسيتيلية من RNF40 تقاوم التعديل بواسطة CDK1، مما يعيق عمليًا الخطوة التالية في التتابع. عندما تنتقل الخلايا إلى المرحلة النهائية قبل الانقسام، يمحو HDAC1 تدريجيًا علامات الأسيتيلا، مما يسمح لـCDK1 بإضافة مجموعات الفوسفات بدلاً منها. يحول هذا التبديل المضبوط من الأسيتيلا إلى الفسفرة RNF40 من حالة "استعداد" إلى حالة "تشغيل"، جاهزًا لتجنيد PLK1 وتشغيل المركز.
ماذا يحدث عندما يفشل التوقيت
لاختبار أهمية هذا التبديل، مهندس الباحثون خلايا بحيث لا يمكن فسفرة RNF40 بعد ذلك، أو جُبرت على البقاء في حالة تحاكي الأسيتيلا. في كلتا الحالتين، فشل PLK1 في التراكم بشكل سليم في المراكز. أظهرت هذه الخلايا ضعفًا في نمو الأنابيب الدقيقة من المراكز، ومغارفًا مشوّهة، وكروموسومات غير مصطفة. انتهى الأمر بالعديد منها إلى وجود كروموسومات زائدة أو مفقودة—حالة غير طبيعية تُعرف باللازوجية—وبعضها أصبح ذا نواتين، وهي علامات على أخطاء انقسام كارثية. في نماذج السرطان، كوّنت الخلايا المحبوسة في حالة RNF40 "المأسيتلة" أورامًا أصغر في الفئران وكانت أكثر حساسية للأدوية الكيميائية الشائعة المستخدمة لعلاج سرطان القولون والمستقيم، مما يشير إلى أن تعطيل هذا التبديل يمكن أن يبطئ نمو الورم.
روابط بالسرطان البشري وإمكانيات مستقبلية
فحص الفريق أيضًا بيانات مرضى وعينات أورام. وجدوا أن RNF40 غالبًا ما يكون زائد الوجود بشكل غير طبيعي في سرطانات القولون والمستقيم وأن طفرات مرتبطة بالسرطان بالقرب من مواقع تعديله تعطل فسفرته، مما يقوّض وظيفة المراكز السليمة. تربط هذه الملاحظات آلية التوقيت الموصوفة حديثًا مباشرة بالمرض البشري. من خلال تحديد بروتين محدد ينسق متى تنضج المراكز وكيف تُفصل الكروموسومات، تبرز الدراسة "عقدة" إشارات يمكن استهدافها لدفع الخلايا السرطانية سريعة الانقسام إلى أخطاء انقسام قاتلة، مع ترك الخلايا السليمة أقل تأثرًا.
مقبض جديد للتحكم في انقسام الخلايا الموثوق
لغير المتخصصين، الرسالة الرئيسية هي أن الخلايا تعتمد على مفتاح كيميائي مضبط بعناية على بروتين واحد، RNF40، لتقرر بالضبط متى تُفعّل الآلية التي تفصل الكروموسومات. يعمل هذا الانتقال من الأسيتيلا إلى الفسفرة مثل إشارة مرورية عند تقاطع مزدحم، تتحول إلى الأخضر فقط عندما تكون الخلية مستعدة فعلاً للانقسام. عندما تعطل الإشارة، تتعثر الخلايا أثناء الانقسام، وتتراكم الأخطاء الجينية، وقد تصبح سرطانية. قد يفتح فهم هذا المفتاح والسيطرة عليه طرقًا جديدة للعلاجات التي تزعزع استقرار الخلايا السرطانية بشكل انتقائي عن طريق تخريب قدرتها على الانقسام بشكل سليم.
الاستشهاد: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
الكلمات المفتاحية: نضج المراكز, انقسام الخلية, عدم استقرار الكروموسومات, إشارات PLK1, سرطان القولون والمستقيم