Clear Sky Science · ar
إصلاح اضطراب المشابك ما بعد الولادة المبكر ينقذ تنكُّس الخلايا العصبية الحركية في نموذج فأري لضمور العضلات الشوكي والبلعومي
لماذا التغيرات الطفيفة المبكرة قد تكون مهمة لضعف العضلات لاحقاً
ضمور العضلات الشوكي والبلعومي (SBMA) حالة وراثية نادرة يفقد فيها البالغون، عادةً الرجال، القوة ببطء في الأطراف والجذع ومناطق البلعوم. تظهر الأعراض في منتصف العمر، لكن المشاكل الطفيفة تبدأ في وقت أبكر بكثير. تطرح هذه الدراسة سؤالاً مفاجئاً: هل يمكن لأحداث قصيرة خلال الأيام الأولى بعد الولادة أن تمهد بصمت لخسارة الخلايا العصبية بعد عقود—وهل يمكن لتصحيح هذه الخلل المبكر حماية الحركة؟
مرض متجذر في مفتاح حساس للهرمونات
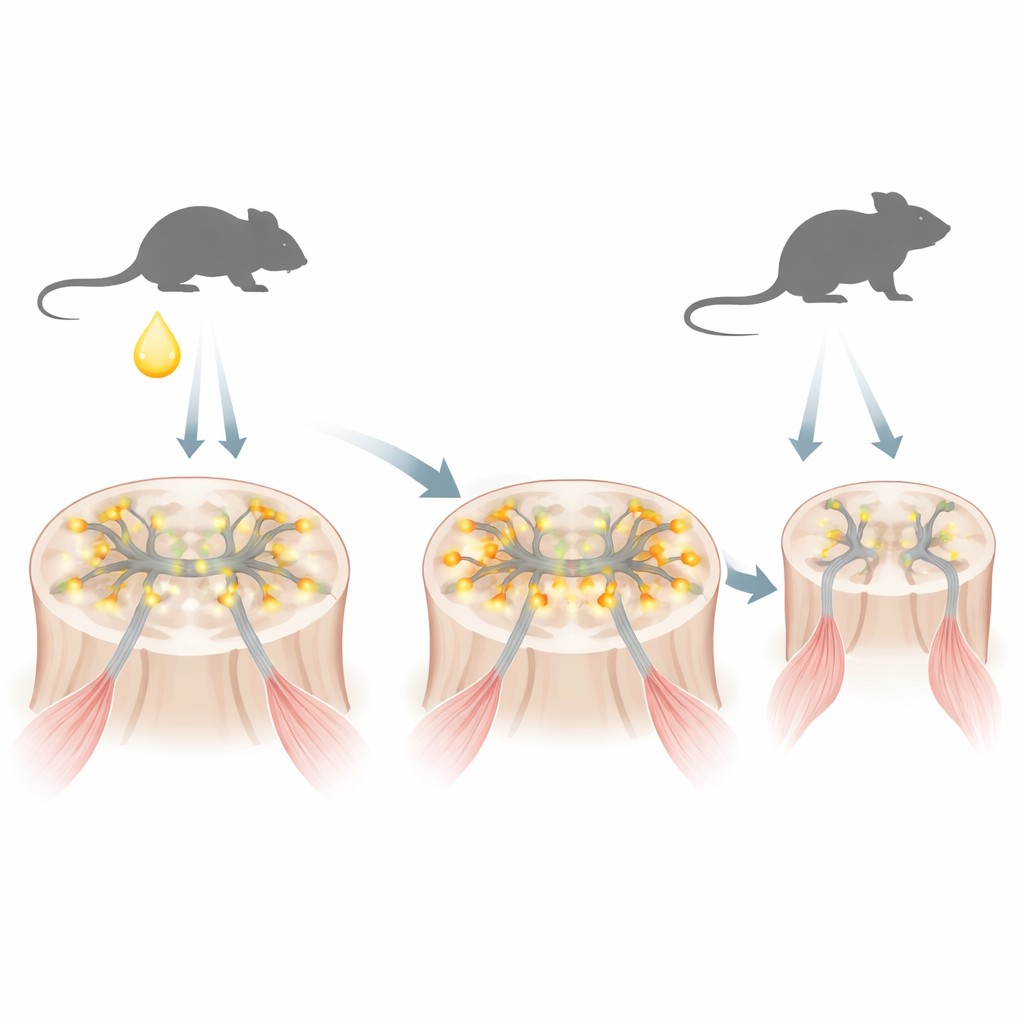
يسبب SBMA نسخة متغيرة من مستقبل الأندروجين، وهو بروتين يستشعر هرمونات الذكورة مثل التستوستيرون. يحمل المستقبل المتغير سلسلة مفرطة الطول من الحمض الأميني جلوتامين. في نموذج فأري يحاكي المرض البشري، وجد الباحثون أنه مباشرة بعد الولادة، عندما تشهد الذكور طفرة قصيرة في التستوستيرون، يتراكم هذا المستقبل الطافر بسرعة داخل نوى الخلايا العصبية الحركية—الخلايا العصبية التي تتحكم في العضلات. في هذه المرحلة المبكرة لم تتجمع البروتينات بعد في الكتل الكبيرة المرتبطة عادةً بالاضطراب العصبي التنكّسي، لكنها بدأت بالفعل تغير أي الجينات تُشغّل وأيها تُطفأ.
زيادة نشاط المشابك المبكرة وخلايا عصبية حركية مضطربة
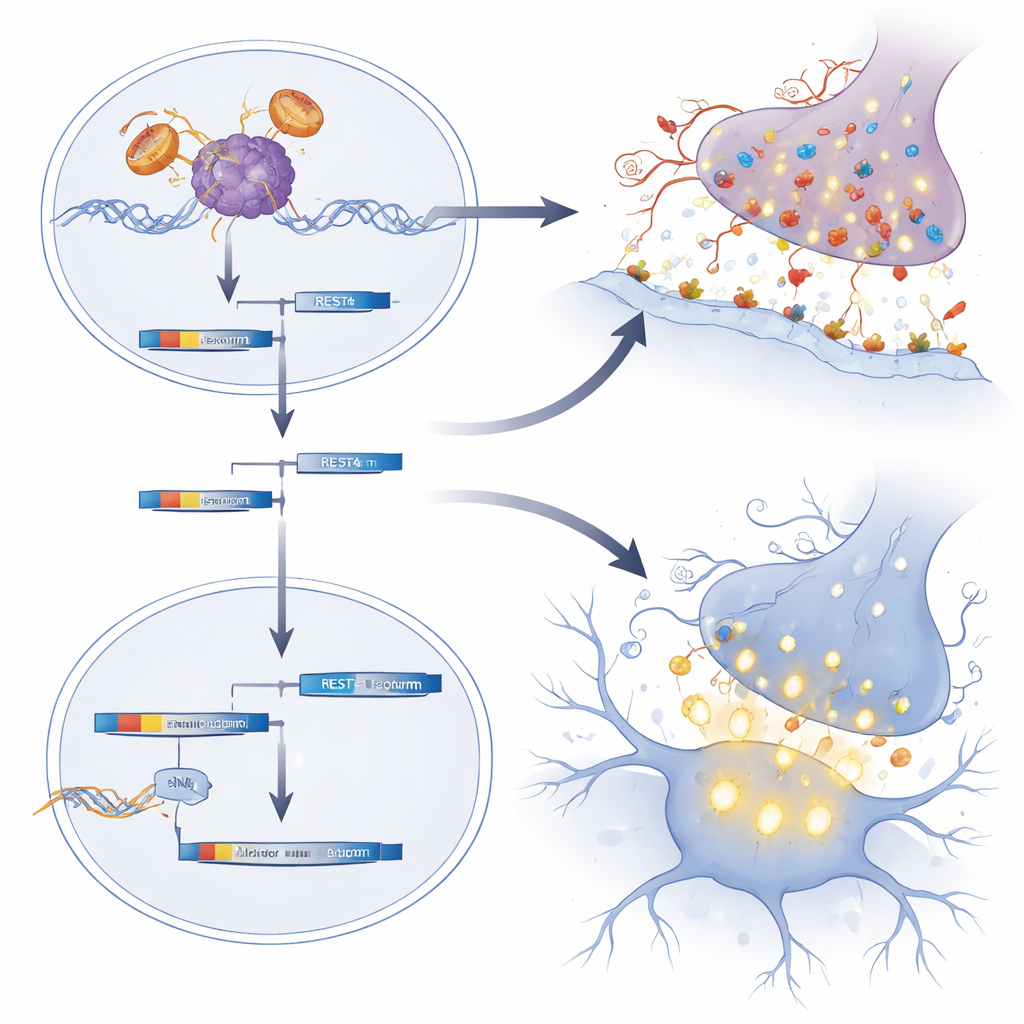
باستخدام تسلسل الحمض النووي الريبي على مستوى الجينوم لأشواك النخاع الشوكي لفئران حديثي الولادة، اكتشف الفريق أن العديد من الجينات المشاركة في المشابك المثبطة—نقاط الاتصال التي تنقل الإشارات بين الخلايا العصبية—كانت نشطة بصورة غير اعتيادية. كثير من هذه الجينات تشفر مستقبلات الغلوتامات، التي تجعل الخلايا العصبية أكثر قابلية لإطلاق النبضات. وتتبع الفريق هذا النمط إلى اضطراب في REST، وهو بروتين «مكبح» رئيسي الذي عادةً ما يحافظ على هذه الجينات المشبكية تحت سيطرة صارمة أثناء التطور. في فئران SBMA وفي الخلايا العصبية الحركية المستنبطة من خلايا جذعية مستحثة لمرضى بشريين، ضعفت نشاط REST ومالت المعادلة لتفضيل شكل مختصر يسمى REST4، مما رفع المكبح وعزَّز جينات المشابك الغلوتاماتية. متسقاً مع ذلك، أظهرت الخلايا العصبية الحركية لحديثي الولادة مستويات أعلى من c-Fos، علامة على الاستثارة الحديثة، وأظهرت خلايا عصبية حركية مشتقة من مرضى بشريين نوبات كلسيوم أقوى وأكثر تكراراً، وهي ملامح فرط الاستثارة.
علاج مبكر قصير يغيّر مسار الحياة
سأل الباحثون بعد ذلك ما إذا كان خفض نشاط المستقبل الطافر أو استعادة مكبح REST خلال هذه النافذة الوليدية فقط يمكن أن يغير مسار المرض على المدى الطويل. حقنوا أوليجونكليوتيدات مضادة—شرائط قصيرة من مادة وراثية معدلة—في السائل المحيط بالدماغ والحبل الشوكي لفئران SBMA بعمر يوم واحد. نوع واحد من الأوليجونكليوتيدات خفض مؤقتاً كل من المستقبل الطافر والطبيعي في الجهاز العصبي المركزي. والنوع الثاني حرَّك تَخييط REST بعيداً عن REST4 وإلى REST كامل الطول، مانعاً بذلك الإفراط في تعبير جينات المشابك. واللافت أنه رغم أن هذه العلاجات أُعطيت مرة واحدة فقط وتأثيراتها الجزيئية المباشرة تلاشت خلال أسابيع قليلة، فقد عاشت الفئران فترة أطول، وتحسَّنت قدرتها على المشي على قضيب دوار، وحافظت على قوة قبضة أقوى لاحقاً في الحياة. كانت خلاياهم العصبية الحركية وألياف عضلاتهم أقل انكماشاً، وتراجعت علامات النشاط العصبي المفرط المبكرة والتفجّرات اللاحقة للموصلات العصبية المرتبطة بالإجهاد.
كيف تشكِّل الهرمونات المبكرة وضبط الجينات القابلية للإصابة
تُبرز الدراسة أيضاً الحساسية الخاصة للخلايا العصبية الحركية لاندفاع التستوستيرون القصير الذي يحدث بعد الولادة مباشرة. عندما أُعطيت فئران SBMA حديثة الولادة جرعات إضافية من التستوستيرون، تفاقم ضعفها وفقدانها للوزن لاحقاً، واضطربت برامج الجينات المرتبطة بالنضوج الصحي للخلايا العصبية الحركية بشكل أكبر. لم تُظهر الفئران الطبيعية هذا الضرر، مما يؤكد أن الأمر يتعلق بتداخل المستقبل الطافر المتغير مع اندفاع الهرمون. وتشير النتائج مجتمعة إلى أنه في SBMA تؤدي كثرة المشابك المثيرة وفرط استثارة الخلايا العصبية الحركية مبكراً في الحياة إلى دفع النظام تدريجياً نحو الفشل، رغم أن الأعراض الواضحة لا تظهر إلا في منتصف العمر.
ماذا يعني هذا للأشخاص المصابين بـ SBMA
لغير المتخصص، الرسالة الأساسية هي أن SBMA قد يكون، جزئياً، مرضاً نتيجة توقيت وتوصيل خاطئين للمشابك خلال الأيام الأولى بعد الولادة. يحفز حساس هرموني معطوب الخلايا العصبية الحركية النامية على الدخول في حالة فرط نشاط، ويساهم هذا الضغط المبكر في تنكسها بعد سنوات. الخبر المشجع هو أن الأدوية الجينية المصممة بعناية، إذا نُفذت خلال هذه النوافذ الحرجة، قادرة على إعادة توازن الإشارات في الخلايا العصبية الحركية، وتهدئة فرط نشاطها، وتأخير أو تقليل خسارة الخلايا العصبية لاحقاً لدى الحيوانات. وبينما سيتطلب نقل مثل هذه التدخُّلات في مرحلة الحياة المبكرة إلى البشر حذراً ودراسة إضافية، تشير هذه النتائج إلى استراتيجيات جديدة تستهدف جذور SBMA طويلاً قبل ظهور الضعف.
الاستشهاد: Hirunagi, T., Sahashi, K., Iida, M. et al. Restoring early postnatal synaptic dysregulation rescues motor neuron degeneration in a mouse model of Spinal and Bulbar Muscular Atrophy. Nat Commun 17, 2412 (2026). https://doi.org/10.1038/s41467-026-70244-2
الكلمات المفتاحية: ضمور العضلات الشوكي والبلعومي, فرط الاستثارية للخلايا العصبية الحركية, مستقبل الأندروجين, تنظيم المشابك بواسطة REST, علاج الأحماض النووية المضادة (أوليجونكليوتيد مضاد)