Clear Sky Science · ar
الكشف متعدد الأوميكس على مستوى الخلية الواحدة عن محور ميكانيحساس PIEZO1-IL-33 البطاني الوعائي الذي يقود التليف الرئوي
لماذا تهم صلابة الرئتين
التليف الرئوي هو حالة رئوية مدمرة تتحول فيها الحويصلات الهوائية التي كانت مرنة تدريجياً إلى نسيج ندبي صلب، مما يجعل كل نفس عملاً شاقاً. يمكن للأطباء حالياً إبطاء تقدم المرض فقط، لا إيقافه أو عكسه. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكن له تبعات كبيرة: كيف تستشعر الخلايا المبطنة للأوعية الدموية في الرئة أن الأنسجة المحيطة بها أصبحت شديدة الصلابة، وكيف يتحول هذا الإحساس إلى مزيد من التندب؟ من خلال تتبع سلسلة الأحداث هذه حتى مستوى الخلايا المفردة والجينات الفردية، يكشف الباحثون عن "مفتاح" ميكانيكي في الأوعية الدموية قد يكون قابلاً للتدخل الدوائي.
من اختبارات وظائف الرئة إلى الخلايا المفردة
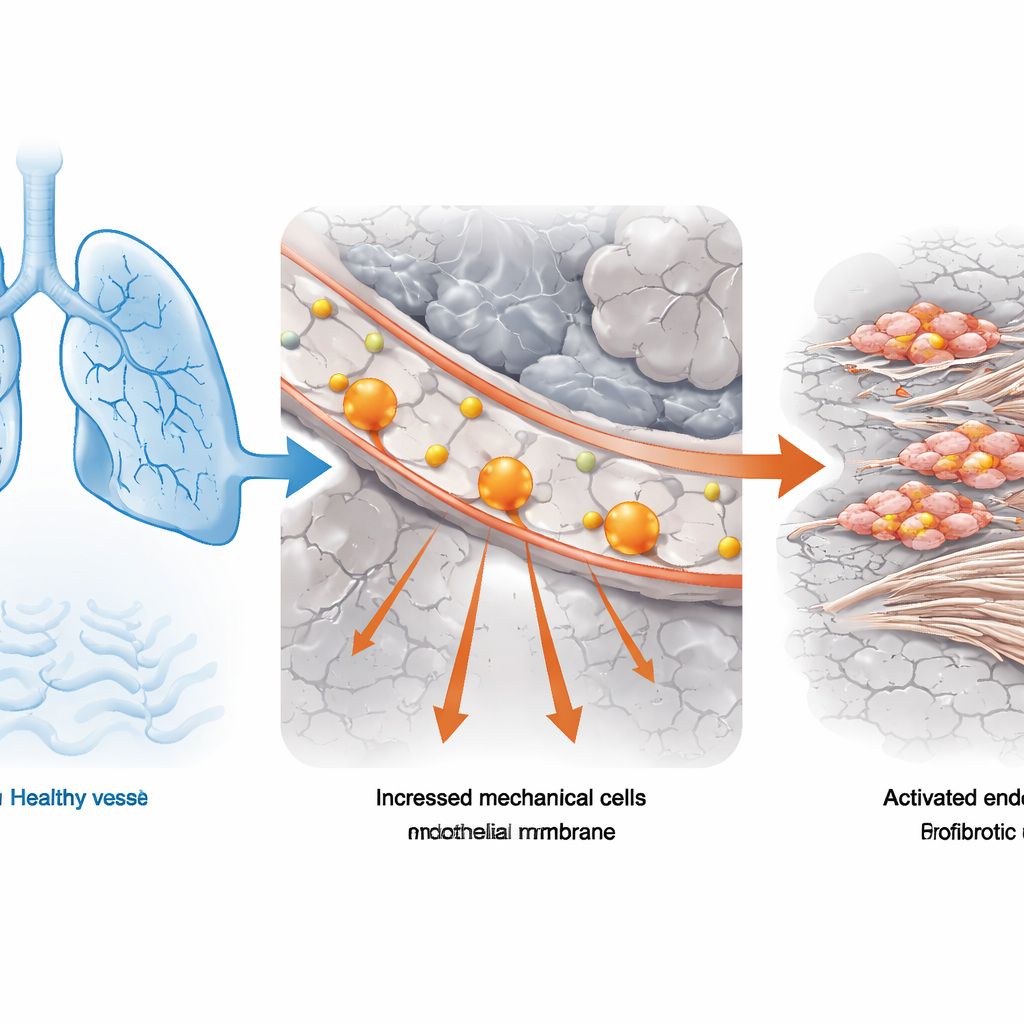
بدأ الفريق بنسيج رئوي من أشخاص مصابين بالتليف الرئوي مجهول السبب، وهو الشكل الأكثر شيوعاً للمرض، ومن متبرعين برئتين طبيعيتين. جمعوا بين قياسات وظائف الرئة التقليدية (كمية الهواء التي يمكن للشخص طردها بقوة) وتقنيات تسلسل الحمض النووي الريبي على مستوى الخلية الواحدة القوية، التي تقرأ أي الجينات نشطة في آلاف الخلايا الفردية. باستخدام أداة حاسوبية تربط البيانات السريرية المجمّعة بملفات الخلايا المفردة، حددوا أي أنواع الخلايا كانت الأكثر ارتباطاً بالضعف الشديد في وظائف الرئة. برزت الخلايا البطانية الوعائية—الخلايا التي تشكل البطانة الداخلية للأوعية الدموية—بأنها غنية بشكل خاص لدى المرضى الذين كانت سعة رئتهم أقل من نصف الطبيعي. في هذه الخلايا البطانية، كانت برامج الجينات المتعلقة "بالضغط الميكانيكي" مرفوعة باستمرار، ما يوحي بأن القوى الفيزيائية غير الطبيعية كانت جزءاً من المشكلة.
الضغط الميكانيكي كسائق خفي
لاختبار ما إذا كان هذا الارتباط بين استشعار الضغط والمرض عاماً، لجأ الباحثون إلى نموذجين فئريين لندوب الرئة: أحدهما أثاره دواء العلاج الكيميائي بليومايسين، والآخر بفعل التعرض طويل الأمد لغبار السيليكا، وهو خطر مهني. باستخدام أساليب الخلية الواحدة على هذه الرئات التجريبية، وجدوا مرة أخرى أن الخلايا البطانية حملت علامات واضحة لزيادة الضغط الميكانيكي. في كلا النموذجين، مع سماكة وتصلب النسيج الرئوي المحيط، بدا أن بطانة الأوعية تتحول إلى حالة ضارة. هذا التلاقي بين العينات البشرية ونماذج الحيوان عزز الفكرة القائلة إن القوى الفيزيائية المشوهة في الرئة، وليس الالتهاب أو نشاط الجهاز المناعي فقط، هي جوهر كيفية تطور التليف وتقدمه.
مستشعر ضغط ذو دور حاسم
بتعمق أكبر، بحث الفريق عن "مستشعرات ميكانيكية" محددة—بروتينات تحول الامتداد الفيزيائي إلى إشارات بيوكيميائية—كانت مرتفعة في الخلايا البطانية المتعرضة للإجهاد. ظهر بروتين قناة واحد، يدعى PIEZO1، مرشحاً بارزاً مراراً. في كل من الفئران والبشر المصابين بالتليف، كانت مستويات PIEZO1 أعلى بكثير في الخلايا البطانية الوعائية مقارنة بالضوابط السليمة. عندما صمم الباحثون فئراناً حذفت فيها PIEZO1 في البطانة فقط، كانت هذه الحيوانات أكثر مقاومة لتندب الرئة الناجم عن بليومايسين: كان لديها تراكم أقل للكولاجين، وعدد أقل من الخلايا المفعّلة المكونة للندوب، ومستويات أدنى من علامة كيميائية للتليف. كما أن حجب PIEZO1 دوائياً بمثبط ببتيدي خفف التندب، في حين أن تنشيطه زاد التليف—ما لم يكن المستقبل مفقوداً في الخلايا البطانية. معاً، أظهرت هذه التجارب أن PIEZO1 في خلايا بطانة الأوعية ليس مجرد مشاهد بل محرك ضروري للمرض.
سلسلة إشارية توقظ الخلايا المكوّنة للندوب
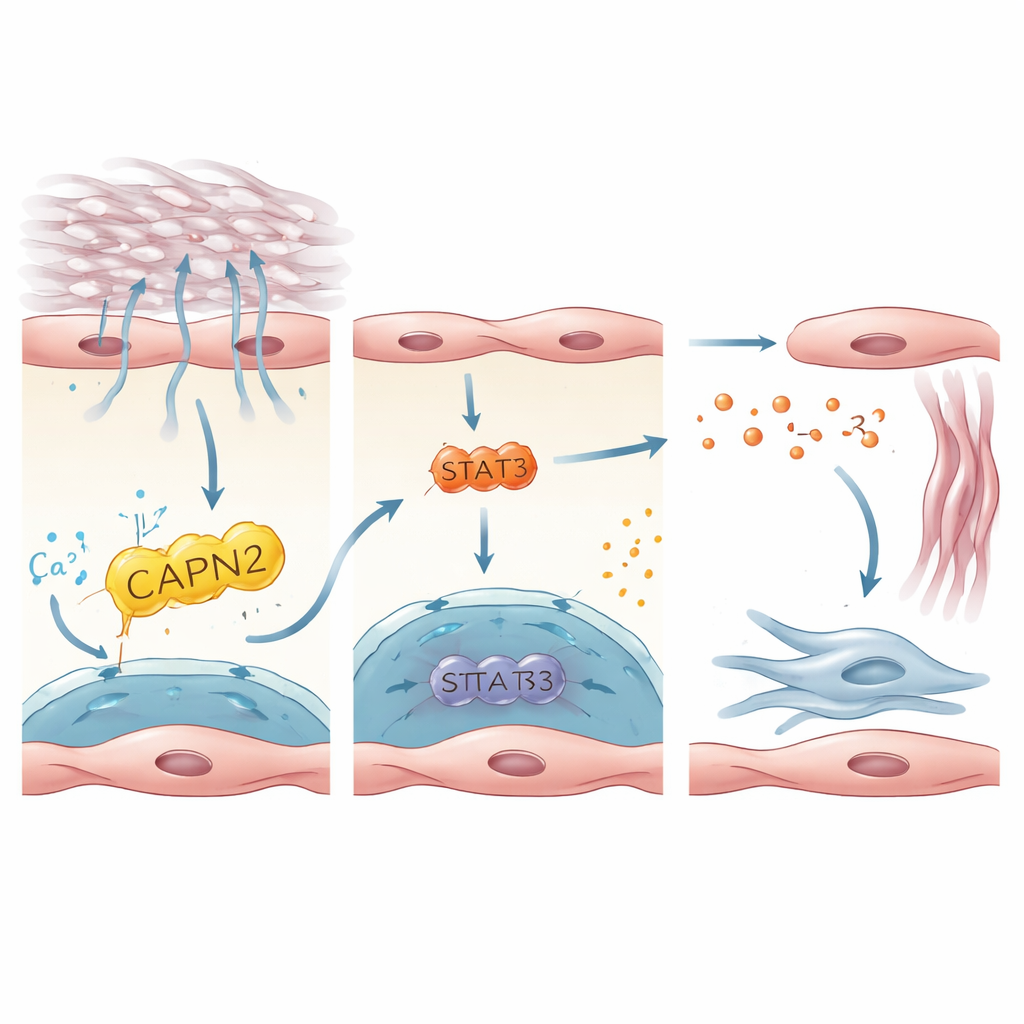
تابعت الدراسة كيف يتحول تنشيط PIEZO1 داخل الخلايا البطانية إلى إشارات توقظ الخلايا الليفية، الخلايا التي تودع النسيج الندبي. من خلال دمج مجموعات بيانات بشرية وفئرية، ركز المؤلفون على الإنترلوكين‑33 (IL‑33)، بروتين صغير تُطلقه الخلايا المتوترة أو التالفة، كمرسال رئيسي. كان IL‑33 معبراً عنه بقوة في الخلايا البطانية الإيجابية لـ PIEZO1 ومرفوعاً في رئات المرضى والفئران المصابة بالتليف. في خلايا بطانية بشرية مزروعة على ركائز صلبة أو ممدودة لمحاكاة التنفس ضد رئة جامدة، عزز تنشيط PIEZO1 إنتاج IL‑33. كان هذا الاعتماد على إنزيم تابع، CAPN2، وعامل نسخي، STAT3، اللذين معاً يوصّفان نشاط جين IL‑33. في الفئران، حمى حذف IL‑33 خصيصاً في الخلايا البطانية من التليف، بينما محاكاة إفراط إنتاج IL‑33 في الخلايا البطانية أزالت التأثير الوقائي لفقدان PIEZO1. ترسم هذه النتائج محوراً خطياً: الضغط الميكانيكي → PIEZO1 → CAPN2/STAT3 → IL‑33 → تنشيط الخلايا الليفية والتندب.
ما الذي يعنيه هذا لعلاجات المستقبل
لغير المتخصصين، الرسالة هي أن التليف الرئوي لا تديره الخلايا المناعية الخارج عن السيطرة وحدها؛ بل هو أيضاً مرض خلل في "الإحساس باللمس" في الأوعية الدموية. تشعر الخلايا البطانية بأن محيطها أصبح أكثر صلابة، وتفعل مفتاح PIEZO1، وتطلق رداً IL‑33، إشارة خطر تحث الخلايا الليفية القريبة على الاستمرار في إيداع النسيج الندبي. من خلال تفكيك هذه السلسلة من القوة الميكانيكية إلى التعبير الجيني، يبرز العمل عدة أهداف واعدة—PIEZO1 نفسه، ومرحلة CAPN2‑STAT3، وIL‑33—لعلاجات تهدف إلى مقاطعة الحلقة المعززة ذاتياً من الصلابة والتندب. ومع أن هناك حاجة لمزيد من الدراسات لتعديل هذه المسارات بأمان في البشر، فإن هذا المحور البطاني الميكانيحساس يقدم زاوية جديدة ذات أساس فيزيائي لمواجهة مرض طالما قاوم علاجات فعالة.
الاستشهاد: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
الكلمات المفتاحية: التليف الرئوي, الخلايا البطانية, التحويل الميكانيكي للإشارات, PIEZO1, IL-33