Clear Sky Science · ar
التقنيات الجينومية الخلوية الفردية تبرز تنشيط الأيض المرتبط بـ MYC وتغير تداخلات الخلايا في تقدم لمفوما التَ‑برو‑لمفاوي الخلوي
لماذا يهم هذا السرطان البطيء الاشتعال
لمفوما الت‑برو‑لمفاوي الخلوي (T‑PLL) هو سرطان دم نادر يتصرف عادة كحريق طبي سريع الانتشار، ينتشر بسرعة ويصعب التحكم فيه. ومع ذلك، لدى ما يصل إلى ربع المرضى، تتوهج المَرَضُة بهدوء لسنوات قبل أن تندلع فجأة إلى مرحلة شديدة العدوانية. تسأل هذه الدراسة سؤالاً بسيطاً لكنه حاسم: ما الذي يتغير داخل هذه الخلايا المناعية المتمردة عندما تنتقل من حالة هادئة إلى حالة نمو سريع؟ من خلال تتبع آلاف الخلايا الفردية على مرّ الزمن، يكشف المؤلفون كيف تكتسب خلايا T‑PLL بشكل تدريجي «استقلالية» أيضية وتخفف روابطها مع أنظمة الضبط الطبيعية في الجسم. قد تشير هذه الرؤى إلى استراتيجيات علاجية جديدة وأكثر دقة.
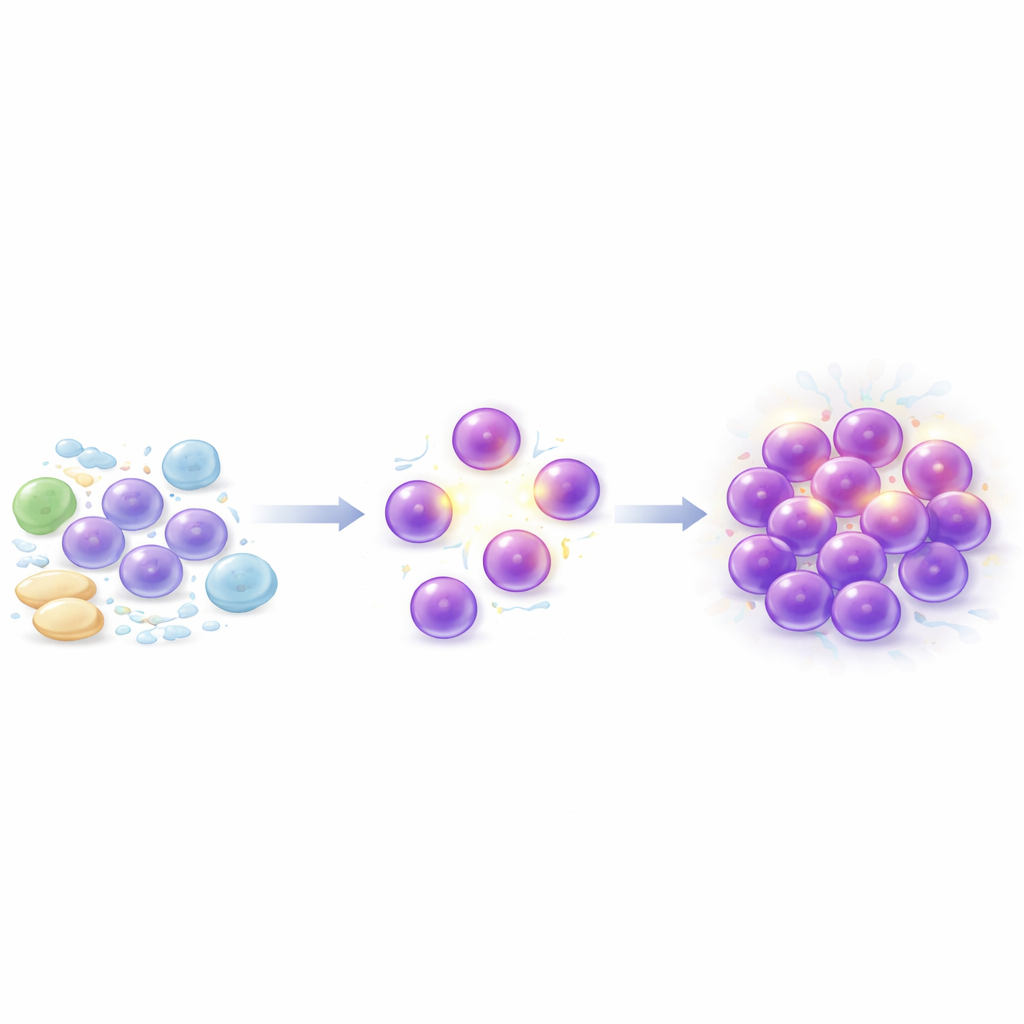
متابعة خلايا السرطان واحدة تلو الأخرى
جمع الباحثون عينات دم من 17 مريضاً لم يتلقّوا علاجاً لـ T‑PLL، بما في ذلك 11 مريضاً تمت متابعتهم على مر الزمن من مرحلة مبكرة بطيئة إلى مرحلة لاحقة عدوانية. باستخدام تسلسل الحمض النووي الريبي الخلوي المفرد، قاسوا أيّ الجينات كانت نشطة في أكثر من 200000 خلية فردية، وقارنوها بخلايا مناعية من متبرعين سليمين. كما أجروا تسلسلاً جينومياً كاملاً في مجموعة فرعية من المرضى لملاحظة التغيرات في الحمض النووي التي ظهرت مع تقدم المرض. سمح هذا المزيج لهم بملاحظة ليس فقط الآفات الجينية الحاضرة، بل أيضاً كيفية توسع أو تقلص مجموعات فرعية مختلفة من خلايا اللوكيميا بمرور الوقت وكيف استجابت البيئة المناعية المحيطة.
تشغيل محرك الخلية الداخلي
كان اكتشاف محوري أن خلايا T‑PLL العدوانية فعّلت بقوة برنامجاً جينياً يتحكم فيه MYC، وهو جين معروف بتعزيز السرطان. أظهرت الخلايا في المرحلة النشطة مستويات أعلى من MYC، ونسخاً أكثر من منطقة MYC في حمضها النووي، ونشاطاً أقوى للجينات المنظمة بواسطة MYC مقارنة بخلايا المرحلة الخاملة أو الخلايا التائية السليمة. كانت البرامج المدفوعة بواسطة MYC مرتبطة ارتباطاً وثيقاً بالمسارات التي تغذي «محركات» الخلية، بما في ذلك الفسفرة التأكسدية والتحلل السكري، وهما الطريقتان الرئيسيتان لتوليد الطاقة داخل الخلايا. أكدت الاختبارات الوظيفية باستخدام محلل أيضي أن خلايا T‑PLL في المرحلة النشطة استهلكت مزيداً من الأكسجين وأنتجت مزيداً من الحمض، وهي علامات على زيادة إنتاج الطاقة، بينما بقيت خلايا المرحلة المبكرة مقيدة أيضياً واستجابت بشكل ضعيف للتحفيز. معاً، تشير هذه النتائج إلى أنه مع تقدم T‑PLL، تهرب خلاياه من القيود الطاقية وتغذي النمو السريع عبر تسريع محطات الطاقة الداخلية.
الاستغناء عن إشارات النمو الخارجية
تعتمد الخلايا التائية السليمة عادة على إشارات من بيئتها — لا سيما عبر مستقبل الخلية التائية، الذي يستشعر المستضدات ويساعد في التحكم بالنمو والبقاء. في مرحلة T‑PLL المبكرة، يكون هذا المحور الإشاري مشوهاً بالفعل بفعل محركات السرطان المعروفة، لكنه لا يزال يبدو ذا دور كبير. تظهر البيانات الجديدة أنه أثناء الانتقال إلى المرض النشط، تقلل العديد من الفئات الفرعية من T‑PLL من مكونات آلية مستقبل الخلية التائية وتظهر استجابات أضعف عند تحفيز المستقبل تجريبياً. تصبح عوامل النسخ الرئيسية المتابعة أقل نشاطاً، ويفقد أو يقلل بعض المرضى من جزيئات مثل CD45 التي تساعد في ضبط إشارات المستقبل. بالأساس، تتطور خلايا الورم لتصبح أقل اعتماداً على إشارات البقاء الخارجية، معتمدة بدلاً من ذلك على أيضها الداخلي المعزز والبرامج المدفوعة بواسطة MYC.
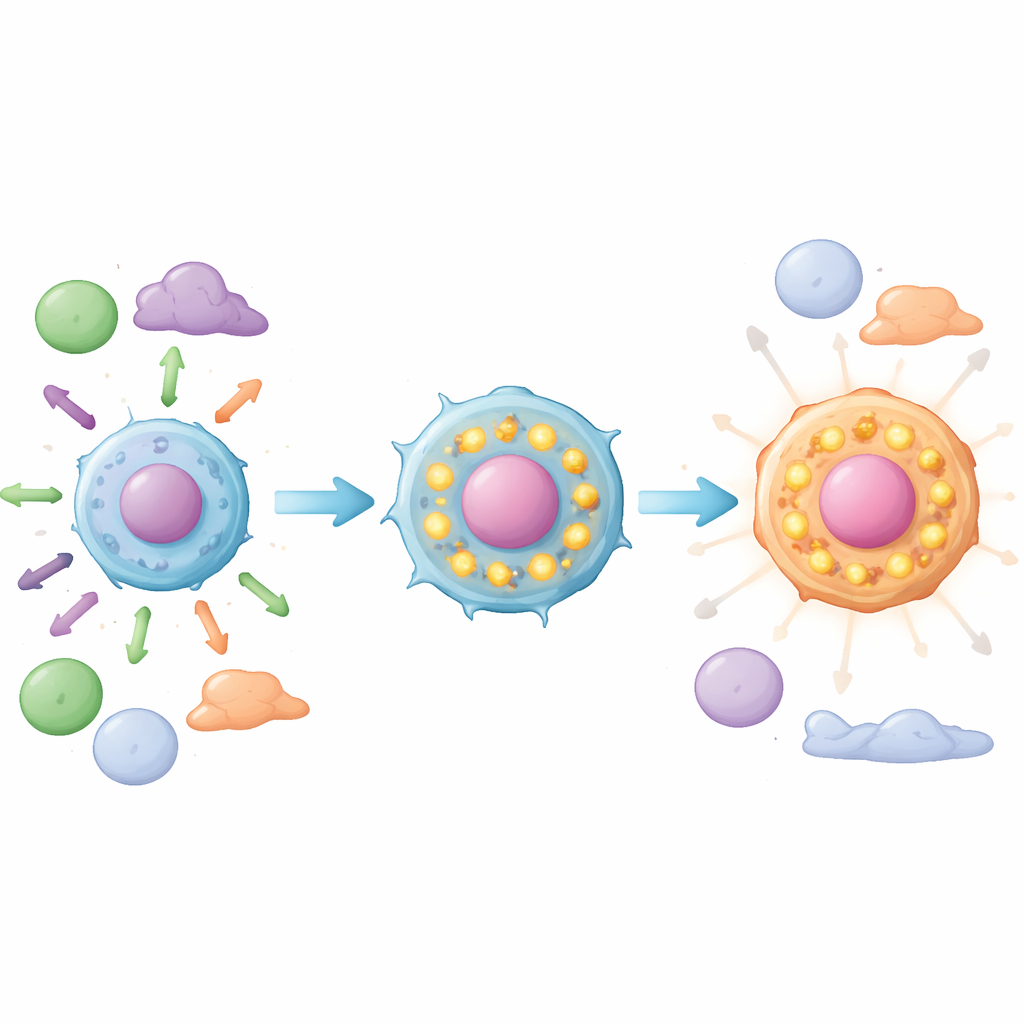
الفرار من الحي المناعي اليقظ
تفحص الدراسة أيضاً الخلايا المناعية غير السرطانية في نفس عينات الدم. مع تحول T‑PLL إلى مرحلة نشطة، يزداد عدد الوحيدات وأنواع معينة من الخلايا الشجرية، لكن نشاط جيناتها يتغير بطرق تشير إلى تراجع الالتهاب وتغير في إشارات الإنترفيرون. عبر أنواع خلايا مناعية متعددة، يتم كبح الجينات المشاركة في عرض المستضدات وإطلاق الاستجابات المناعية. في الوقت نفسه، تُظهر النماذج الحاسوبية للتواصل بين الخلايا أن خلايا اللوكيميا تتفاعل أقل مع معظم الخلايا المناعية المحيطة في المرحلة العدوانية، بينما تصبح الإشارات الموجهة إلى الوحيدات أقوى. وتبرز جزيئات مثل Annexin A1 وانخفاض مستويات بروتين السطح CD48 كمساهمات محتملة في بيئة أكثر تهرباً من المناعة وملائمة للورم.
ما الذي يعنيه هذا للمرضى
بالمجمل، ترسم النتائج مساراً تدريجياً من الهدوء إلى العدوانية في T‑PLL: خلايا اللوكيميا المبكرة لا تزال مقيدة جزئياً بإمداد طاقة محدود، واعتماد على إشارات نمو خارجية، ومراقبة مناعية. مع مرور الوقت، تكتسب الفئات الفرعية التي تضخم MYC، وتزيد من إنتاج الطاقة، وتضعف اعتمادها على الإشارات الخارجية ميزة انتقائية وتصبح مهيمنة، مما يؤدي إلى توسع سريع للمرض. بالنسبة للمرضى، يوحي ذلك بأن العلاجات التي تستهدف مسارات مرتبطة بـ MYC أو أيض الخلايا أو تداخلات محددة بين الورم والمناعة قد تكون ذات قيمة خاصة في المرحلة النشطة — وربما حتى في وقت أبكر، قبل أن تفلت اللوكيميا تماماً من هذه المكابح الطبيعية.
الاستشهاد: Wahnschaffe, L., Jungherz, D., Müller, T.A. et al. Single-cell genomics highlight MYC-associated metabolic activation and altered cell interactions in T-prolymphocytic leukemia progression. Nat Commun 17, 2319 (2026). https://doi.org/10.1038/s41467-026-70185-w
الكلمات المفتاحية: لمفوما الت‑برو‑لمفاوي الخلوي, علم الجينوم الخلوي المفرد, إشارة MYC, تمثيل سرطاني, البيئة الدقيقة للورم