Clear Sky Science · ar
استهداف الاعتماد على استخدام التيروزين المرتبط بالـ tRNA يكشف ضعفًا استقلابيًا في سرطان الكبد الكبدي
حرمان خلايا السرطان من لبنة بناء شائعة
خلايا سرطان الكبد، مثل جميع الخلايا سريعة الانقسام، تحتاج إلى إمداد ثابت من الأحماض الأمينية — اللبنات الصغيرة للبروتينات. تكشف هذه الدراسة أن سرطان الخلايا الكبدية، أكثر أشكال سرطان الكبد شيوعًا، لديه ضعف غير متوقع: اعتماده الكبير على حمض أميني واحد هو التيروزين من أجل إنتاج الطاقة والبقاء. عن طريق تقييد كيفية استخدام الخلايا السرطانية للتيروزين بشكل انتقائي، تمكن الباحثون من إبطاء نمو الأورام، وإلحاق الضرر بمحطات طاقة الخلايا، وتحفيز شكل من أشكال موت الخلية قد يُستخدم لعلاجات جديدة.
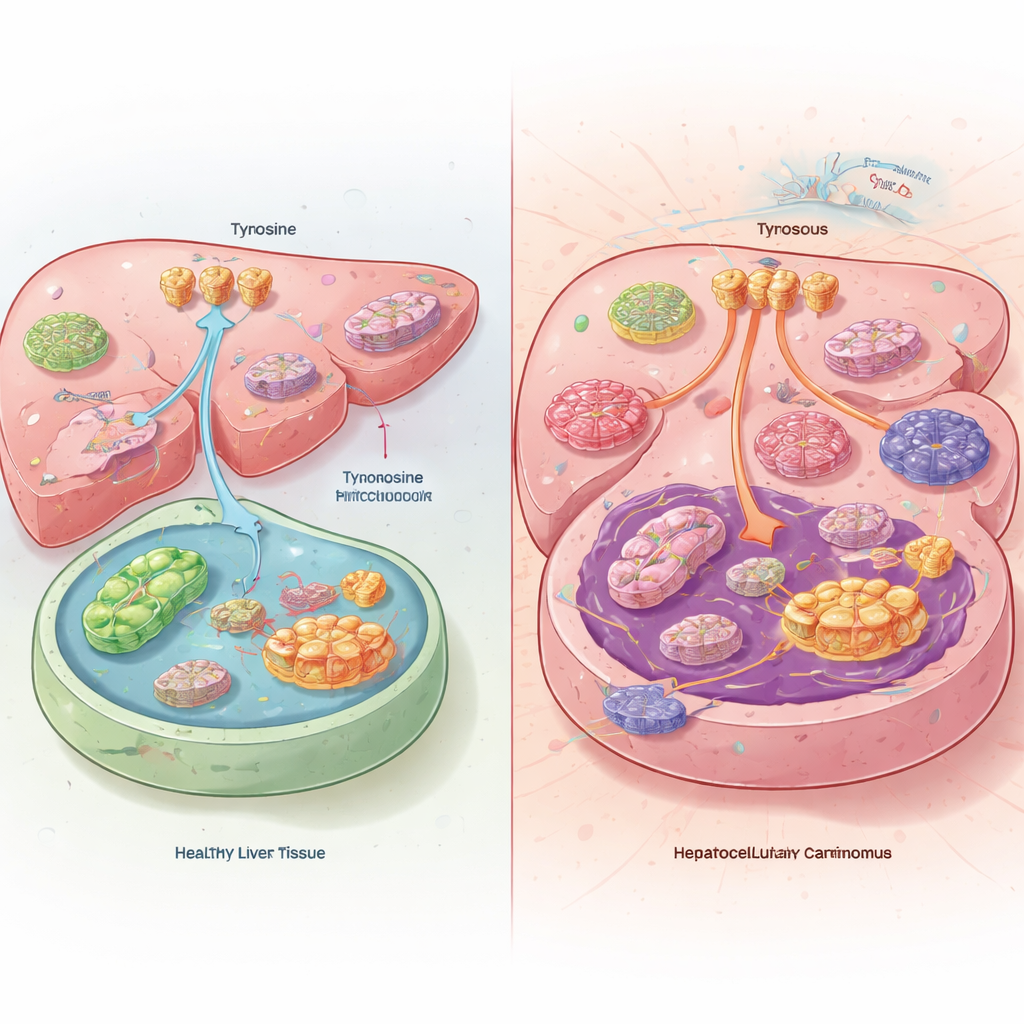
اختلال متوارٍ في أورام الكبد
عند مقارنة الفريق لأورام الكبد مع نسيج الكبد السليم من مرضى وفئران، وجدوا أمرًا محيرًا. داخل الخلايا السرطانية كانت مستويات التيروزين منخفضة فعليًا، على الرغم من أن الأورام كانت تسحب تيروزينًا أكثر من مجرى الدم وتكسّره أقل. بدلًا من حرق التيروزين كوقود، أعادت أورام الكبد توجيهه نحو إنتاج البروتين. حققت السرطانات ذلك بزيادة نشاط ناقلات التيروزين على سطح الخلية وخفض إنزيمات الكبد التي عادةً ما تفكك التيروزين. الفئران التي أعطيت نظامًا غذائيًا خاليًا من التيروزين طورت أورامًا أصغر وعاشت لفترة أطول، بينما التيروزين الزائد في الحمية سرّع نمو أورامها.
كيف تعيد السرطان توصيل إنتاج البروتين
تتبع الباحثون هذه الشهية للتيروزين إلى جين قوي يدفع السرطان يُسمى MYC. في أورام الكبد، يُشغّل MYC بروتينًا يسمى YARS1، الذي يعلّق التيروزين على حمض ناقل معين (tRNA-TyrGUA). هذا الـ tRNA المحمّل هو ما تحتاجه الريبوسومات لبناء بروتينات غنية بالتيروزين. أظهرت الدراسة أن سرطانات الكبد تعزّز كل من YARS1 وtRNA المطابق، مما يضمن خط إمداد مميزًا للتيروزين نحو تخليق البروتين. تعطيل هذا الخط — إما بتخفيض مستويات التيروزين، أو إسكات YARS1 أو tRNA-TyrGUA، أو منع تحميل التيروزين — جعل خلايا سرطان الكبد أقل قدرة على البقاء في الأطباق وفي الفئران، كاشفًا عن ضعف استقلابي مرتبط بقوة باحتياجاتها العالية لإنتاج البروتين.
شلّ محطات الطاقة وتوازن الدهون
بدمج قياسات عبر الجينوم للـ RNA وإنتاج البروتين والمواد المستقلبة، حدّد الفريق هدفين حساسَين بشكل خاص لتقييد التيروزين. الأول، NDUFB8، مكوّن من المجمع الأول في الميتوكوندريا، وهو جزء أساسي من آلية توليد الطاقة في الخلية. الثاني، SCD1، يساعد في تحويل الدهون المشبعة إلى دهون أحادية غير مشبعة أكثر أمانًا للتخزين في أغشية الخلايا والقطرات الدهنية. عندما تم تقييد التيروزين المخصّص للترجمة، انخفض إنتاج NDUFB8 وSCD1، بينما بقيت مستويات RNA الخاصة بهما دون تغيير كبير — دليل واضح على أن الترجمة، وليس التعبير الجيني، هي المتأثرة. أدى ذلك إلى تجميع ضعيف للمجمع الأول، وانخفاض التنفس الخلوي، وزيادة في أنواع الأكسجين التفاعلية، وتحول في تكوين الدهون من أحادية غير مشبعة إلى أشكال متعددة غير مشبعة أضعف وأكثر عرضة للتأكسد.
إجبار خلايا السرطان على موت مدفوع بالحديد
ألقت الأضرار المترتبة على الميتوكوندريا والدهون غير المستقرة خلايا سرطان الكبد نحو الفيروبتوز، وهو شكل من موت الخلية يعتمد على الحديد وينجم عن بيروكسدة الدهون. حاولت الأورام المقاومة بزيادة مانعات الفيروبتوز الطبيعية مثل GPX4 وجزيئات مرتبطة بها، لكن شاشة واسعة النطاق باستخدام محرّك الجينات CRISPR أظهرت أن تعطيل هذه الحمايات جعل تقييد التيروزين أكثر فتكًا. في نماذج خلوية وفأرية، أدّى الجمع بين استراتيجيات تقييد التيروزين وأدوية مثبطة لـ GPX4 أو BCL2 — أو مع أدوية سرطان الكبد الحالية مثل سورافينيب وفينيتوكلاكس — إلى تحكم أقوى في الورم، وأعباء ورمية أصغر، وبقاء أطول.
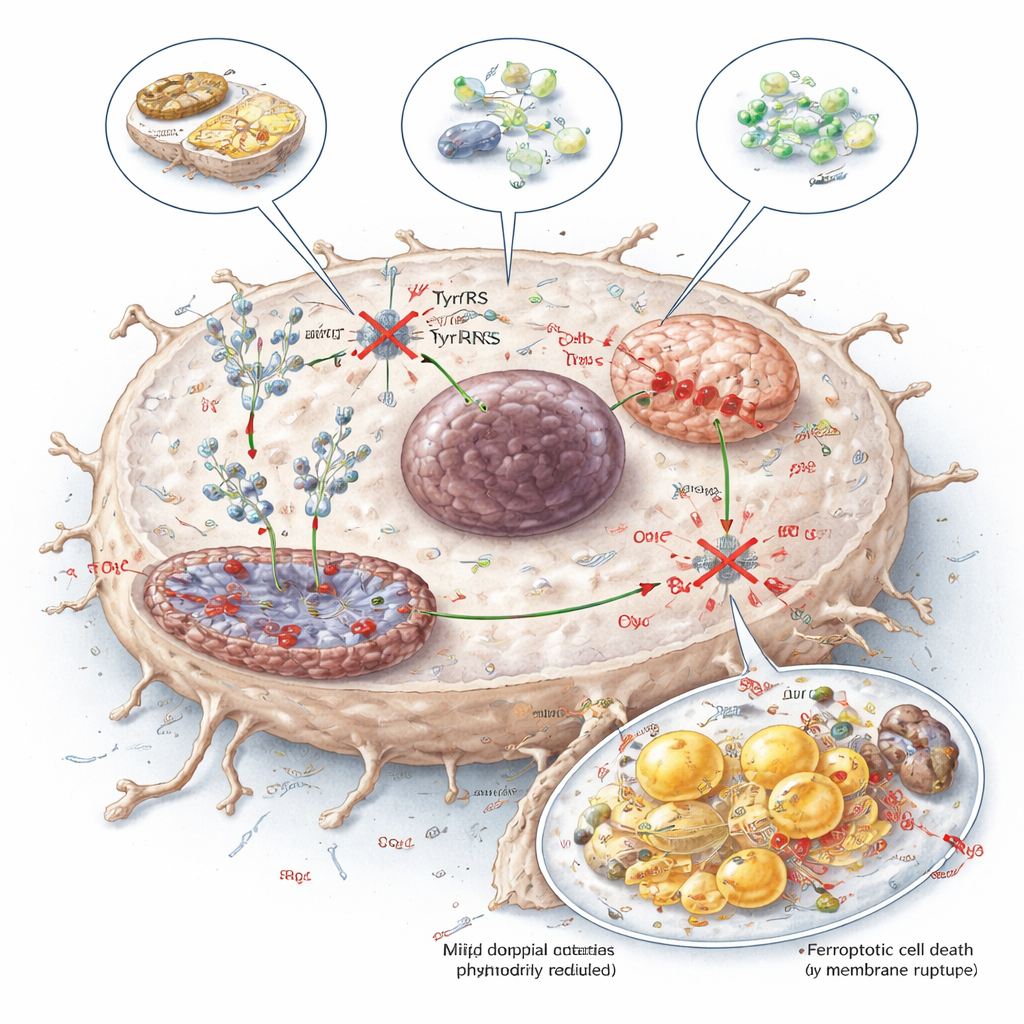
تحويل ضعف استقلابي إلى علاج
لاستكشاف طرق عملية لاستغلال هذا الضعف، اختبر الباحثون ثلاث طرق: نظام غذائي منخفض التيروزين، إنزيم (TAL) يحلل التيروزين إنزيمياً، وجزيء صغير يُسمى تايروسينول يتنافس مع التيروزين على الارتباط بـ YARS1. كل الطرق الثلاث خفّضت توفر التيروزين لتخليق البروتين، وقلّلت مستويات NDUFB8 وSCD1، وألحقت ضررًا بوظيفة الميتوكوندريا، وزادت من الفيروبتوز في أورام الكبد، مع آثار قابلة للإدارة على الأنسجة السليمة في الفئران. للمتلقي غير المتخصص، الرسالة هي أن سرطانات الكبد تبدو متعلقة بالتيروزين ليس فقط كمغذٍ، بل كوقود دقيق لآلة صنع البروتين لديها. استهداف هذا الاعتماد — عبر الحمية أو الإنزيمات أو الأدوية — يقدّم طريقة واعدة لإضعاف الأورام وتعزيز فعالية العلاجات القائمة.
الاستشهاد: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
الكلمات المفتاحية: سرطان الكبد, الأيض الأميني, التيروزين, الميتوكوندريا, الفيروبتوز