Clear Sky Science · ar
التعرّف المنهجي على تداخلات بنية الرنا-جزيئات صغيرة الخاصة بالمتغيرات موضّحًا بأرباع غوانين للرنا
لماذا تهم التغيرات الطفيفة في الرنا للأدوية المستقبلية
معظمنا يرث اختلافات صغيرة في حمضنا النووي تجعلنا فريدين. هذه التغيرات الطفيفة يمكن أن تعيد تشكيل طيات جزيئات الرنا داخل خلايانا بشكل دقيق. الدراسة الجديدة تعرض طريقة لرؤية كيف تغيّر هذه التعديلات الجينية قبضة الأدوية التجريبية التي تستهدف الرنا. والأمر مهم لأن نفس الدواء قد يتصرف بشكل مختلف للغاية من شخص لآخر، لا سيما في حالات السرطان أو الأمراض الوراثية.
طريقة جديدة لرؤية أماكن تماس الأدوية مع الرنا
العديد من مطوّري الأدوية ينظرون الآن إلى الرنا، وليس البروتينات فقط، كأهداف للعلاج. يمكن للجزيئات الصغيرة أن تتشبث بأشكال رنا خاصة وتؤثر في طريقة قراءة الجينات، لكن حتى الآن معظم الأساليب كانت تعمل على تسلسل «مرجعي» واحد فقط. وكانت تتجاهل في الغالب التغيرات المفردة الحرف الموجودة لدى المرضى الحقيقيين. أنشأ المؤلفون طريقة عالية الإنتاجية تسمى BIVID-MaP يمكنها اختبار آلاف متغيرات الرنا في وقت واحد وتحديد موضع ارتباط الجزيء الصغير بكل واحد منها، بدقة مستوى نيوكليوتيد واحد. 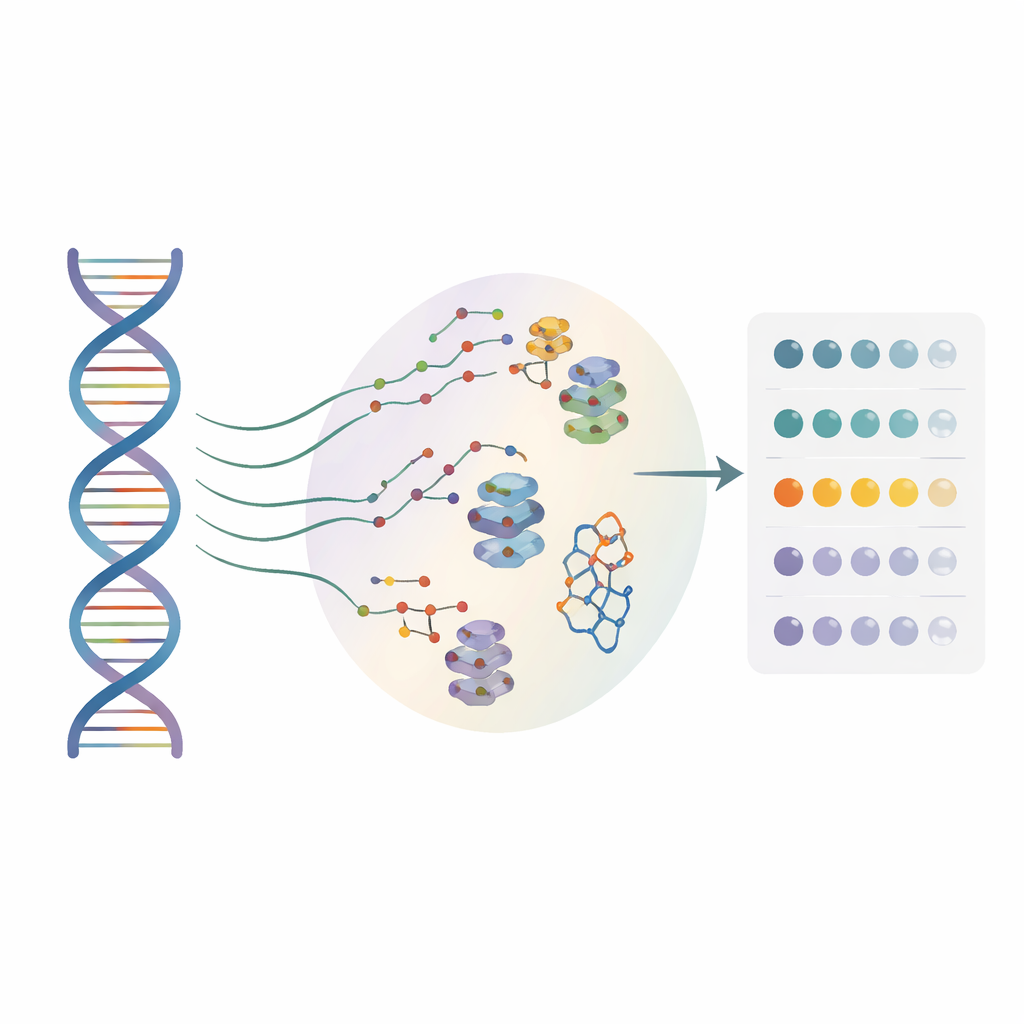
تحويل العلامات الكيميائية إلى إشارة قابلة للقراءة
تعمل BIVID-MaP في ثلاث خطوات رئيسية. أولًا، يلحق الفريق علامة تفاعلية بجزيء صغير يرتبط بالرنا. عندما يستقر هذا المركب المعلم في البنية المفضلة له في الرنا، مثل أرباع غوانين المدمجة الناتجة عن سلاسل غوانين غنية، تشكل العلامة رابطة كيميائية دائمة مع قاعدة رنا قريبة. ثانيًا، تقوم إنزيم خاص بنسخ الرنا المعدل إلى حمض نووي منقوص الأكسجين. عند مواجهته لإحدى هذه العلامات الكيميائية، يميل إلى «تخطي» قاعدة واحدة، محدثًا حذفًا طفيفًا في النسخة. ثالثًا، يقرأ التسلسل العميق هذه بصمات الحذف عبر ملايين الجزيئات. وبما أن معظم التسلسل المحيط يبقى محفوظًا، يمكن نسب الحذوفات بدقة إلى متغيرات جينية محددة في عينة مختلطة.
إثبات الطريقة على حالة اختبار مسيطرة
للتأكد من أن BIVID-MaP تكشف فعلاً عن ارتباطات خاصة بالمتغيرات، درس الباحثون مقطع رنا من جين CD44 الذي يشكّل عادة أربعة-حلقي غوانين. تغيير واحد من غوانين إلى أدين يفسد هذه البنية. في خليط يحتوي كلا النسختين، أظهرت النسخة الكاملة فقط إشارات حذف قوية بالقرب من المنطقة المطوية عند تعريضها لمسبار مشتق من البربرين، وتحقّق تجارب مستقلة من وجود ارتباط أقوى هناك. أما المتغير، الذي لا يستطيع تشكيل نفس الشكل، فأنشأ عددًا أقل بكثير من الحذوفات وارتباطًا أضعف. التقنيات الشائعة الأخرى لرسم الخرائط إما فاتتها هذه الاختلافات أو أنتجت ضوضاء مربكة، ما يبرز الحساسية والنوعية المحسّنتين للطريقة الجديدة.
مسح الطفرات المرتبطة بالسرطان عبر العديد من الجينات
ثم قام الفريق بتوسيع النطاق. بنوا مكتبة رنا من مناطق غير مترجمة 5′ (5′ UTRs) مأخوذة من 283 جينًا مرتبطًا بالسرطان، كل واحدة مقرونة بطفرات جسمية حقيقية مُبلّغًا عنها في الأورام. باستخدام مسبار يتعرّف على هياكل شبيهة بأربعة-حلقيات الغوانين، كشفت BIVID-MaP عن العديد من الطفرات التي إما قوّت أو أضعفت ارتباط الجزيئات الصغيرة. في جينات مثل DAXX وING2، غيّرت تغييرات حرفية مفردة في امتدادات غوانين-غنية الارتباط بشكل ملحوظ، متوافقة مع اختبارات فيزيائية-كيميائية مستقلة لتكوين أربعة-حلقيات الغوانين وقياسات ارتباط مباشرة بواسطة مطيافية الكتلة. في بعض الحالات، أدت الطفرات خارج امتدادات الغوانين الواضحة إلى تحويل الارتباط عن طريق تغيير احتمالية اقتران القواعد المجاورة بشكل طفيف، معيدًا تشكيل «مجموعة» البنى دون تغيير كبير في الطية المتوقعة عامة. 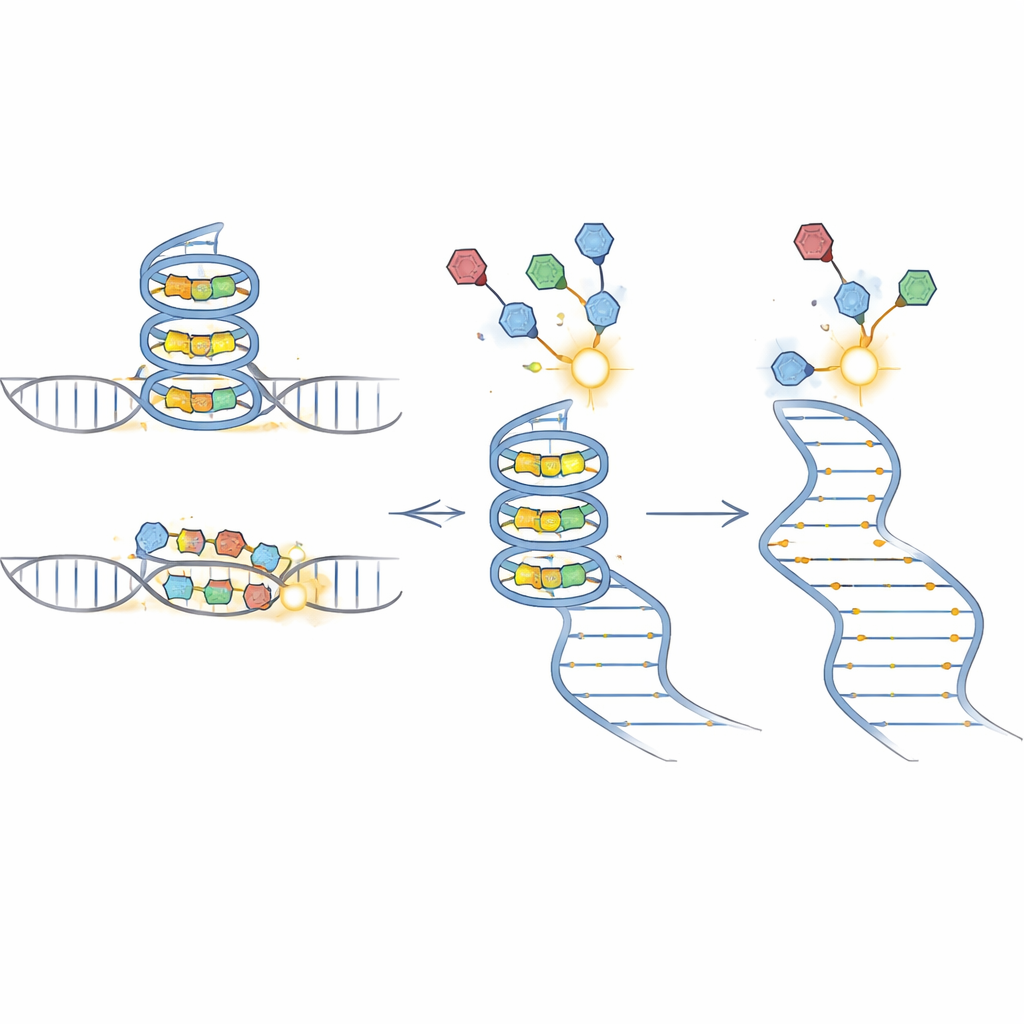
رؤية ما تفوته التنبؤات الحاسوبية
من المهم أن أدوات التنبؤ بهياكل الرنا وأربعة-حلقيات الغوانين الحالية غالبًا ما أخفقت في التنبؤ بالتغيرات التي كشفتها BIVID-MaP. بعض المتغيرات التي غيرت الدرجات الحاسوبية بالكاد أنتجت فروقًا كبيرة في العالم الواقعي من حيث الارتباط. بدا بعضها أنه يؤثر في الارتباط عبر عائلة من المركبات المستهدفة لأربعة-حلقيات الغوانين، بينما كانت لطفرات أخرى تأثيرات خاصة بدواء معين. هذا يوضح أن المتغيرات بنيوكليوتيد واحد يمكنها ضبط مشهد طيات الرنا ومواضع تماس الدواء بطرق يصعب استنتاجها من التسلسل وحده.
ما معنى هذا لأدوية الرنا الشخصية
يخلص المؤلفون إلى أن BIVID-MaP توفر طريقًا قويًا لرسم خارطة كيف تعيد الاختلافات الجينية الفردية تشكيل تراكيب الرنا وتفاعلاتها مع جزيئات الدواء الصغيرة. من خلال تحويل التعديلات الكيميائية المحلية إلى بصمات حذف دقيقة، يمكن للطريقة أن تفحص آلاف المتغيرات بالتوازي وتبرز تلك التي تغيّر ارتباط الدواء بشكل ذي مغزى. على المدى الطويل، قد توجه مثل هذه الخرائط تصميم أدوية تستهدف الرنا أكثر فعالية وأمانًا عبر تنوع المرضى، وتكشف عن تراكيب رنا مخفية سابقًا قد تخدم كأهداف دوائية جديدة.
الاستشهاد: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
الكلمات المفتاحية: أدوية تستهدف الرنا, أربعة-حلقيات غوانين, متغيرات جينية, ارتباط الجزيئات الصغيرة, طفرات السرطان