Clear Sky Science · ar
جسيمات نانوية من الأزرق البروسي تستهدف بنية PANoptosome متعددة الوسائط لـ PANoptosis لعلاج إصابة نقص تروية القلب وإعادة التدفق
لماذا تهم حماية القلب أثناء الشفاء
عندما يصاب شخص بنوبة قلبية، يسارع الأطباء إلى إعادة فتح الشريان المسدود واستعادة تدفّق الدم. لكن هذه الخطوة المنقذة للحياة تحمل ثمنًا خفيًا: فالعودة المفاجئة للأكسجين يمكن أن تصيب القلب نفسه، فتقتل خلايا وتؤسس لحدوث فشل قلبي. تستكشف هذه الدراسة دواءً نانويًا مبتكرًا يهدف إلى حماية القلب خلال هذه المرحلة الحرجة عن طريق حجب عدة مسارات مترابطة لموت الخلايا في آن واحد، ما قد يؤدي إلى تعافٍ ألطف بعد النوبات القلبية.
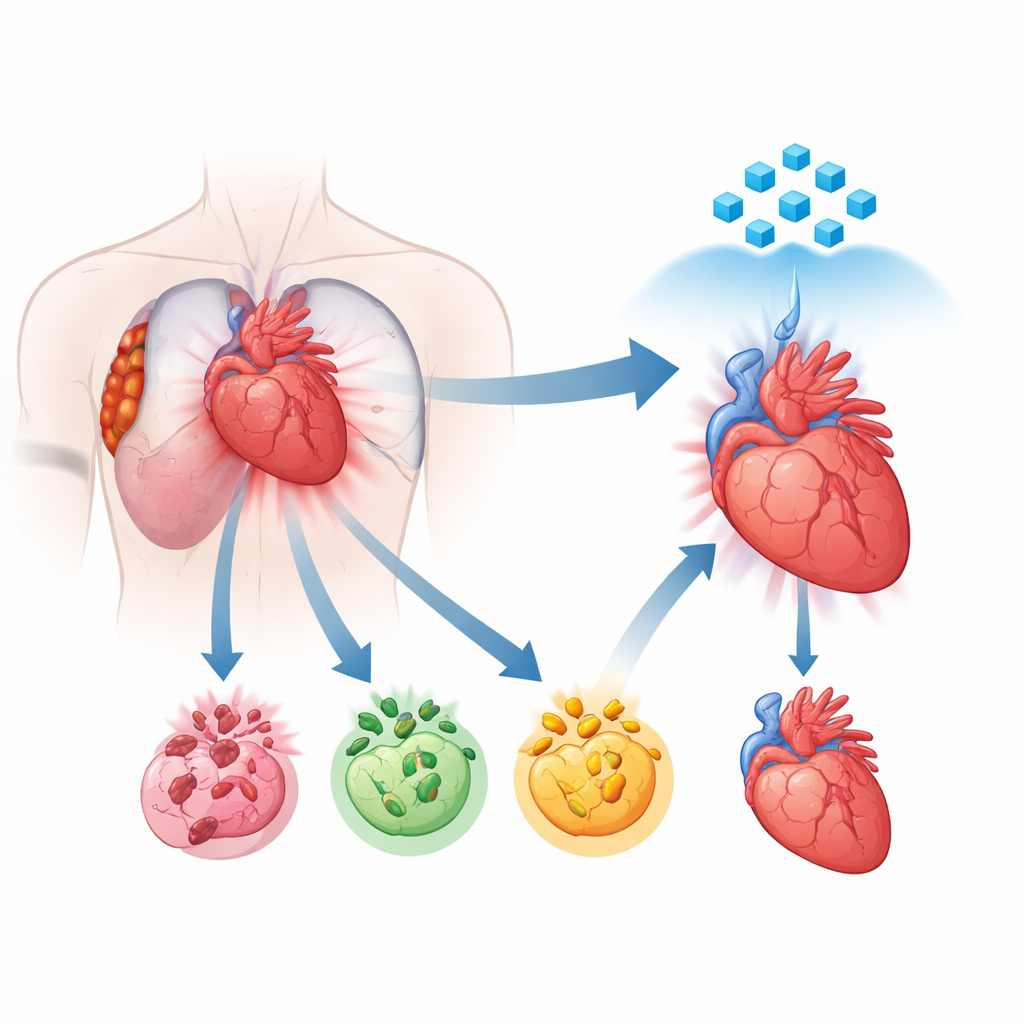
رؤية جديدة لكيفية موت خلايا القلب
لطالما عرف العلماء أن الخلايا القلبية المتضررة يمكن أن تموت عبر مسارات مبرمجة مختلفة، بما في ذلك الموت المبرمج (apoptosis)، النخر المبرمج (necroptosis)، والبيروبتوزيس (pyroptosis). لكل منها سيناريو جزيئي خاص، لكن الأدلة المتزايدة تُظهر أن هذه المسارات لا تعمل بمعزل عن بعضها. بل تتواصل مع بعضها وقد تندمج في عملية مشتركة متسارعة تُسمى PANoptosis. في هذه الحالة، تشتغل عدة برامج موت في آن واحد، ما يجعل العلاجات التي تحجب مسارًا واحدًا فقط ضعيفة إلى حد الإحباط. استخدم المؤلفون تسلسل الرنا النووي أحادي النواة لأنسجة قلبية بشرية من مرضى تعرضوا لنوبات قلبية مؤخراً لرسم خريطة أماكن وشدة تفعيل هذه البرامج المميتة. وجدوا أنه في المناطق الأكثر تضرراً، أظهرت خلايا عضلة القلب تحولاً قوياً نحو هذا الوضع المشترك للموت، مما يضع PANoptosis كسائق مركزي للإصابة.
تصميم أداة نانوية متعددة الوظائف للقلب المصاب
لمعالجة مثل هذه العملية المعقدة، لجأ الفريق إلى الأزرق البروسي، مركب طبي معتمد منذ زمن ويشتهر كمضاد لسموم بعض المعادن. على مقياس النانو، تتصرف جزيئات الأزرق البروسي كروبوتات حفزية صغيرة يمكنها تحييد الجزيئات الضارة والتأثير على سلوك الخلايا. من خلال محاكاة حاسوبية، أظهر الباحثون أن هذه الجسيمات النانوية يمكن أن ترتبط مباشرة بثلاثة محاور بروتينية رئيسية—RIPK1، ZBP1، وAIM2—التي تساعد في تجميع الآلية الجزيئية لـ PANoptosis. عن طريق الارتباط بهذه المحاور بطرق مختلفة، تنبأت النمذجة بأن الجسيمات ستعوق بناء المجمعات المسببة للموت التي تنسق المسارات الثلاثة لموت الخلايا.
توجيه الجسيمات النانوية مباشرة إلى نسيج القلب المتضرر
لا تعمل الجسيمات النانوية إلا إذا وصلت إلى المكان الصحيح، لذا غلف الفريق جزيئات الأزرق البروسي بأغشية طبيعية مستخرجة من الصفائح الدموية، وهي خلايا دموية تتوجه نحو الأوعية المصابة. خلق هذا الطلاء ناقلًا حيويَّ المحاكاة أُطلق عليه PB@PM، يدور في الدم كلوح صفائح لكنه يُسلِّم حمولة علاجية. في فئران خضعت لنوبة قلبية محكومة ثم إعادة فتح للشريان، أظهرت الصور أن PB@PM تراكمت بقوة أكبر بكثير في منطقة القلب المصابة مقارنة بالجسيمات غير المغلفة، مع تجنّب إلى حد كبير للأعضاء السليمة. والأهم من ذلك، أن الجسيمات المغلفة كانت محمولة جيدًا: اختبارات الدم وفحوصات الأنسجة لم تكشف عن سمية واضحة، ما يدعم إمكان مواصلة تطويرها.
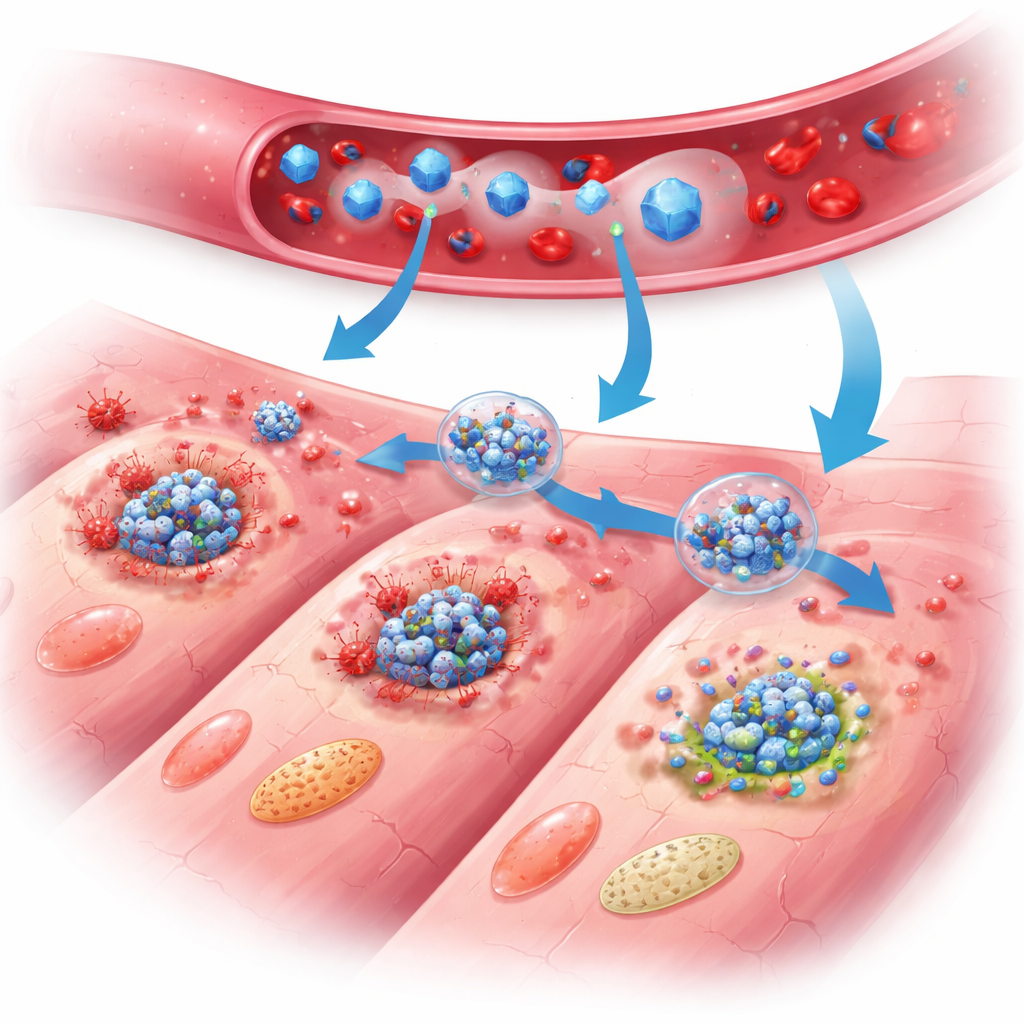
كيف يحمي الدرع النانوي القلب
في الفئران المعالجة، بانت فوائد PB@PM على مدى أيام وأسابيع. تحسنت وظيفة الضخ القلبي، تقلصت مساحة الندبة، وكان جدار القلب أقل ترققًا مقارنة بالحيوانات غير المعالجة. كشفت دراسات الأنسجة التفصيلية عن عدد أقل من خلايا القلب المتموتة، وخلايا التهابية أكثر هدوءًا، ونسيج تصليح منظمًا بشكل أفضل مع نمو أوعية دموية أكثر صحة وقلة تضخم غير طبيعي للخلايا الباقية. على المستوى الجزيئي، أظهرت تحليلات واسعة لتعبير الجينات وقياسات البروتين أن PB@PM خفّضت نشاط المسارات الثلاثة الرئيسية للموت المبرمج معاً، وعطّلت تجميع مجمعات PANoptosis متعددة البروتين، وخفضت مستويات جزيئات الإشارة التي تغذي الالتهاب. كما قامت الجسيمات بابتلاع أنواع الأكسجين التفاعلية الضارة، وثبتت الميتوكوندريا — محطة طاقة الخلية — وأعادت الأيض الطاقي إلى حالة أكثر طبيعية، فأزالت محفزات رئيسية كانت ستدفع الخلايا إلى تدمير ذاتي.
ما الذي قد يعنيه هذا لرعاية النوبات القلبية مستقبلًا
ببساطة، تُظهر هذه الدراسة أن جسيمًا نانويًا مصممًا بذكاء يمكن أن يعمل كدرع متعدد الرؤوس للقلب، مهدئًا شبكة من إشارات الموت المدمرة بدلاً من مطاردة مسار واحد في كل مرة. عبر التوجه إلى نسيج القلب المصاب، والارتباط ببروتينات التحكم الأساسية، وتخفيف الإجهاد التأكسدي والالتهابي، خفّض PB@PM بشكل حاد سلسلة فقدان الخلايا والتندب التي تتبع غالبًا إعادة فتح شريان مسدود. ومع أن اختبارات كثيرة لا تزال مطلوبة قبل أن تصل هذه الاستراتيجية إلى المرضى، تقدّم الدراسة إثبات مفهوم بأن استهداف PANoptosis ككل — وباستخدام جزيئات ذكية مستوحاة بيولوجيًا — قد يفتح فصلاً جديدًا في حماية القلب بعد النوبة القلبية.
الاستشهاد: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
الكلمات المفتاحية: نقص تروية القلب وإعادة التدفق, علاج بالجسيمات النانوية, موت الخلايا المبرمج, التهاب قلبي, حماية الميتوكوندريا