Clear Sky Science · ar
RPA تحفز مباشرةً قدرة المحلّق Mer3 على العملية لضمان تكوّن نقاط التشابك الطبيعية في الانقسام الاختزالي
كيف تعيد الخلايا خلط الحمض النووي لصنع بويضات وحيوانات منوية صحية
في كل مرة تصنع فيها نباتات أو حيوانات أو بشر بويضات أو حيوانات منوية، يجب على خلاياها إعادة خلط الكروموسومات بحيث يحصل كل نسل على مزيج جديد من حمض نوين الوالدين. وتعتمد هذه إعادة الخلط الجيني على تبادلات دقيقة من الحمض النووي، أو نقاط التشابك، بين أزواج الكروموسومات. تكشف الدراسة المذكورة كيف يعمل بروتينان أساسيان، Mer3 وRPA، معًا كآلة مجهرية لضمان تشكيل هذه النقاط بكفاءة وأمان — عملية لها تبعات على الخصوبة والتطور وربما السرطان.
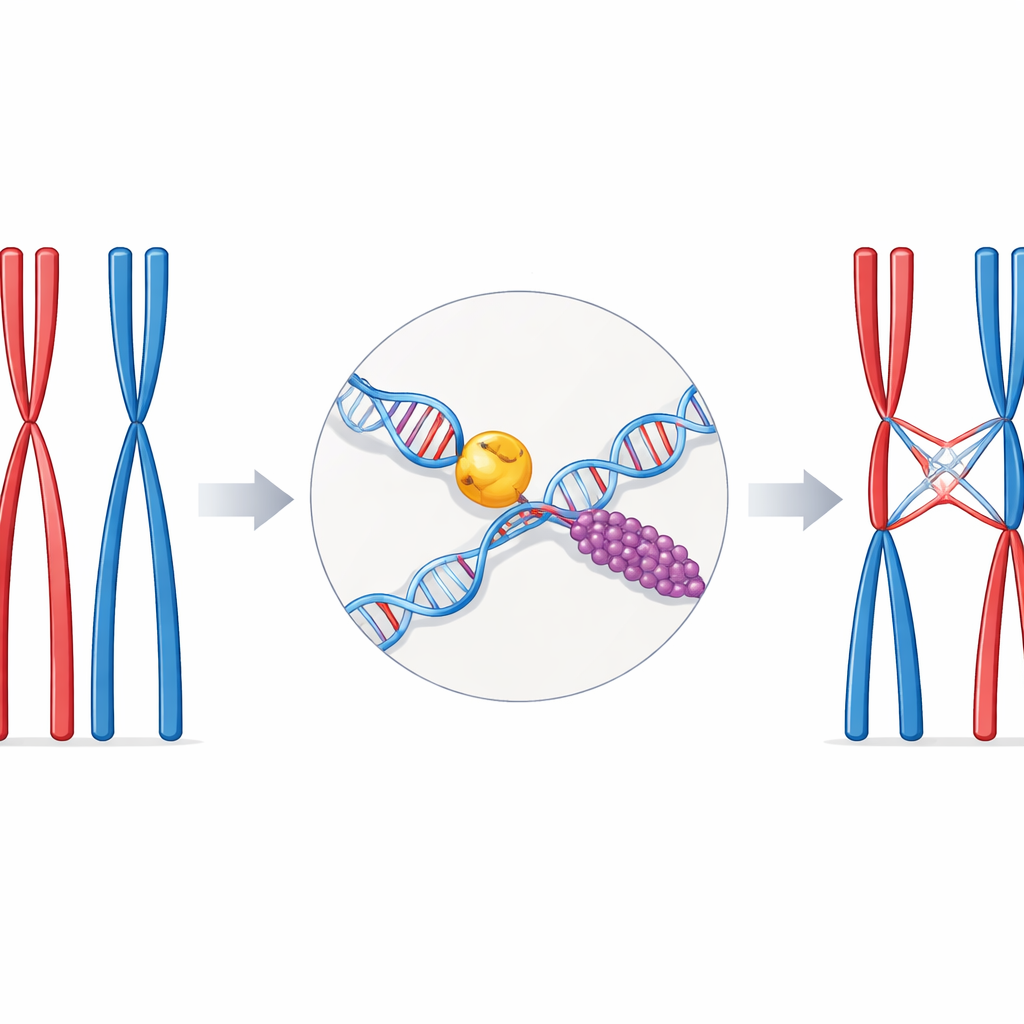
توازن دقيق في التكاثر الجنسي
خلال انقسام خلوي خاص يُسمى الانقسام الاختزالي، تتواجد الكروموسومات في أزواج متطابقة، أحدهما من كل والد. لكي تنفصل هذه الأزواج بشكل صحيح، يجب أن ترتبط ماديًا في عدد قليل من المواقع المختارة على طولها. هذه الروابط هي نقاط التشابك — مناطق تتبادل فيها سلاسل الحمض النووي من كروموسوم مع شريكه. قلة نقاط التشابك تعرض للخطر انتثار الكروموسومات وتؤدي إلى العقم؛ أما كثرتها أو وجودها في مواقع خاطئة فقد يضر الجينوم. لذلك تعتمد الخلايا على مسارات إصلاح متخصصة وبروتينات مساندة لتحويل كسر الحمض النووي الخطير إلى تشابك مُتحكم فيه بشكل صحيح.
تعرف على Mer3 وRPA، فريق فك الحمض النووي
ركز الباحثون على Mer3، وهو محرك جزيئي يفك طي الحمض النووي ويعزز تكوين نقاط التشابك. النظير البشري له، HFM1، معروف بأهميته للخصوبة. اكتشفوا أن Mer3 يرتبط مباشرةً بـRPA، وهو مركب بروتيني يغطي عادةً الحمض النووي أحادي السلسلة المكشوف ليحميه ويستدعي عوامل إصلاح أخرى. باستخدام تجارب بيوكيميائية ونمذجة هيكلية واختبارات تداخل، رسم الفريق موقع تثبيت محددًا حيث يتناسب ذيل قصير من Mer3 داخل أخدود في أحد وحدات RPA. هذا الواجهة محافظة من الخميرة إلى الثدييات، ما يشير إلى أنها حل تطوري مستمر للتحكم في إصلاح الحمض النووي أثناء الانقسام الاختزالي.
مراقبة محرك حمض نووي واحد أثناء العمل
لمعرفة ما تفعله هذه الشراكة فعليًا، استخدم العلماء ملاقط مغناطيسية أحادية الجزيء — أداة تثبت شعرة حمض نووي مفردة مثل زنبرك صغير وتقيس كيف يفكك جزيء Mer3 واحد هذا الشعر مع مرور الوقت. وجدوا أن Mer3 يتحرّك على الحمض النووي بسرعة ثابتة حتى بمفرده. لكن في ظروف تحاكي التوتر الفيزيائي المنخفض داخل الخلايا، يميل Mer3 إلى الانفلات من الحمض النووي بعد فك جزء قصير فقط. عند وجود كمية صغيرة من RPA، يصبح Mer3 أكثر استمرارًا فجأة: يمكنه فك أطوال أطول بكثير من الحمض النووي دون السقوط، خصوصًا عندما يكون الحمض النووي معرضًا للانطواء على نفسه. فشل شكل طافح من Mer3 مُهندَس لتعطيل ذيل ربط RPA في اكتساب قوة الثبات هذه، مما يبيّن أن الاتصال المباشر مع RPA هو ما يعزز قابلية Mer3 للعمل المستمر.
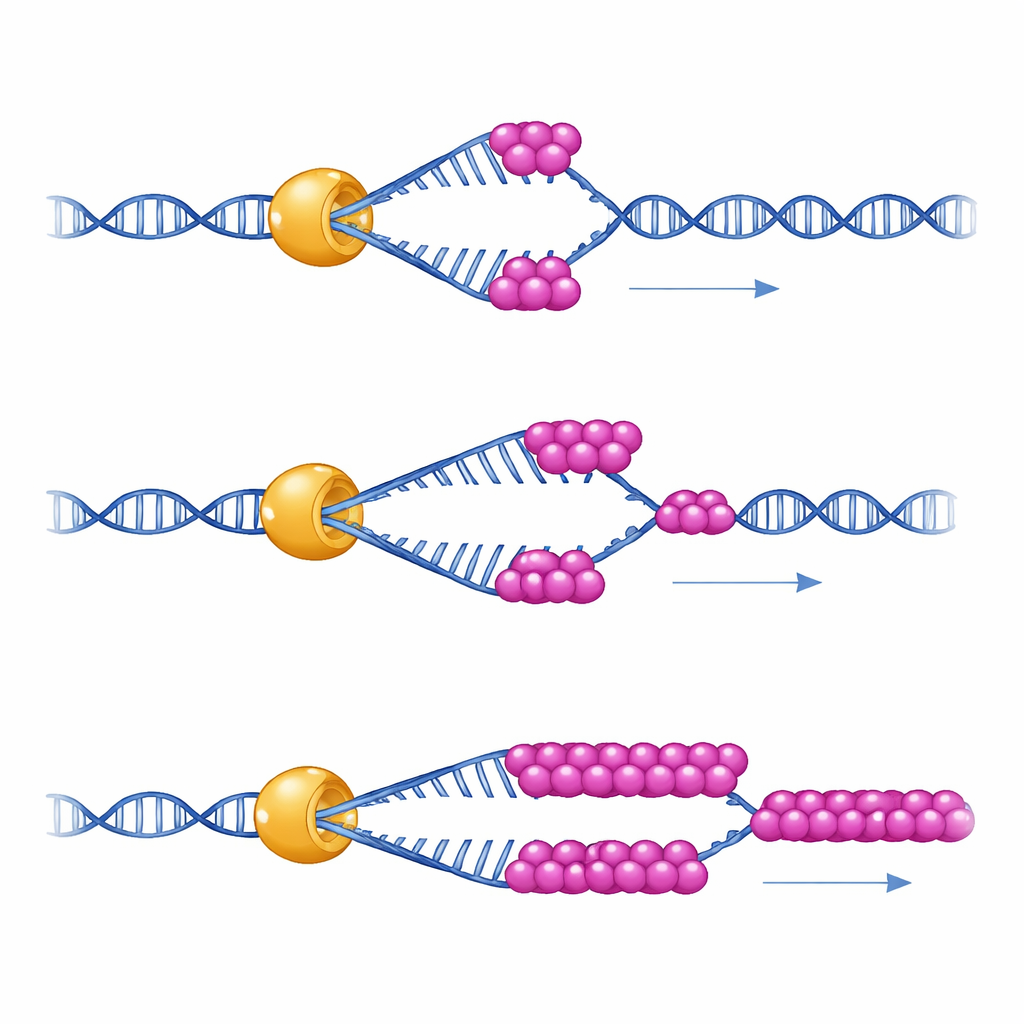
العواقب على نقاط التشابك في الخلايا الحية
سأل الفريق بعد ذلك ماذا يحدث في خلايا الخميرة الحقيقية عندما لا يستطيع Mer3 الإمساك بـRPA بشكل صحيح. استبدلوا جين MER3 الطبيعي بالطافح الذي يفقد ربط RPA وراقبوا الانقسام الاختزالي. كانت هذه الخلايا قادرة على الانقسام وتكوين الأبواغ، لكن خصوبتها انخفضت وانخفض العدد الإجمالي لنقاط التشابك على بعض مناطق الكروموسومات. أظهرت تحليلات الحمض النووي تفصيليًا مزيدًا من أحداث الإصلاح التي انتهت كغير تشابكية وتراكمًا للوسطاء في إعادة التركيب لم تُحل. كشفت خريطة المواضع الجينومية لـMer3 أن البروتين الطافح جرى توظيفه بشكل أقل استقرارًا إلى المواقع التي تحدث فيها كسور مبرمجة في الحمض النووي، رغم أن ارتباطه المبكر بمحاور الكروموسومات بدا طبيعيًا. بعبارة أخرى، بدون ربط قوي مع RPA، لا يبقى Mer3 طويلًا بما يكفي عند مواقع الكسر لدفعها بثقة نحو نتائج تشابك.
ما يعنيه هذا للخصوبة واستقرار الجينوم
تُظهر الدراسة مجتمعةً أن RPA يفعل أكثر من تغطية الحمض النووي المكشوف؛ إنه يضبط مباشرةً سلوك هيليكاز اختزالي رئيسي. من خلال التثبيت على RPA، يصبح Mer3 محقِقًا أكثر إصرارًا لفك الحمض النووي، قادرًا على تمديد وتثبيت هياكل الحمض النووي المشتركة التي تنضج إلى نقاط تشابك. عندما يضعف هذا التفاعل، تتجه الخلايا نحو نتائج إصلاح أكثر أمانًا ولكن أقل نفعًا وتترك مزيدًا من الوسطاء غير المحلولين، مما يقوّض بتدريجية فصل الكروموسومات. ولأن نفس اللاعبين الجزيئيين موجودون لدى البشر — وترتبط طفرات في HFM1 بالعقم — فإن هذا العمل يقدم إطارًا آليًا لكيفية أن تغييرات صغيرة على واجهة بروتينية يمكن أن تمتد لتؤثر على الصحة الإنجابية والتنوع الجيني للأجيال القادمة.
الاستشهاد: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
الكلمات المفتاحية: الانقسام الاختزالي, إعادة التركيب الجيني, هيليكاز الحمض النووي, الخصوبة, تبادل الكروموسومات