Clear Sky Science · ar
عدم تنظيم استجابة تلف الحمض النووي بواسطة أوليغو نيوكليوتيدات معاكسة الفسفوروتيويت
عندما تخدع علاجات الجينات المفيدة طاقم إصلاح الخلية
الأوليغو نيوكليوتيدات المعاكسة، أو ASOs، هي فئة متصاعدة من الأدوية الدقيقة المصممة لتشغيل أو إيقاف جينات فردية. تُستخدم بالفعل لعلاج بعض الاضطرابات الوراثية النادرة وتُجرَّب على العديد من الأمراض الأخرى. تكشف هذه الدراسة عن جانب سلبي غير متوقع في تعديل كيميائي شائع يُستخدم لجعل هذه الأدوية أكثر استقرارًا: في ظروف معينة، يمكن أن تخدع الخلية للاعتقاد بأن حمضها النووي تالف، ما يعرقل آليات الإصلاح ويعرض الجينوم لخطر أذى طويل الأمد.
مفاتيح جينية مصممة وترقيتها الكيميائية
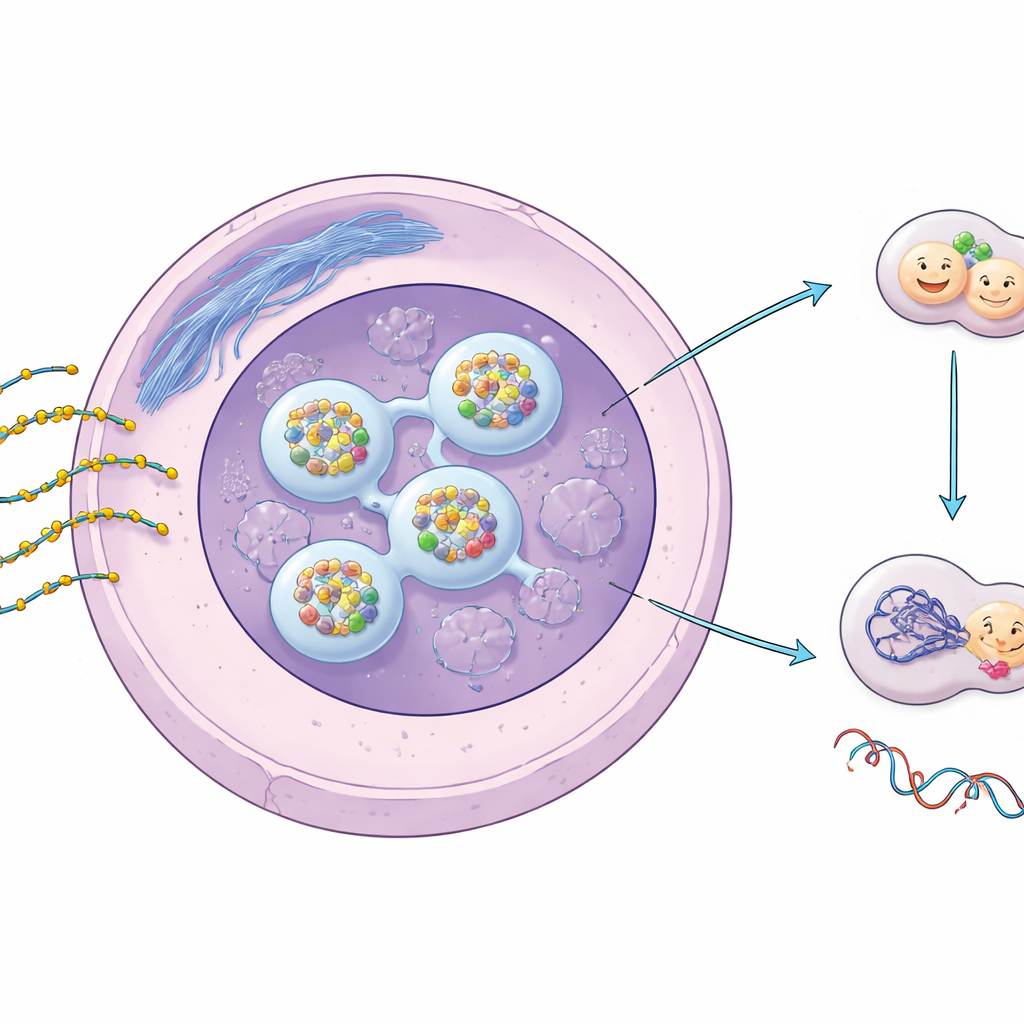
تتألف ASOs من سلاسل قصيرة أحادية من المادة الجينية مصممة للتعرف على رسائل RNA محددة داخل خلايانا والارتباط بها، وبالتالي إسكاتها أو تغييرها. للبقاء في الجسم والدخول إلى الخلايا بكفاءة، تحمل معظم ASOs العلاجية تعديل فسفوروتيويت (PS)، حيث يُستبدل ذرة كبريت لذرة أكسجين في عمود السلسلة. هذا التغيير الصغير يعزز بشكل كبير استقرارها وميلها للتفاعل مع البروتينات. أظهرت أعمال سابقة أن PS‑ASOs تتجمع في نقاط مميزة داخل نواة الخلية وقد تسبب ضغطًا على بعض الهياكل النووية، لكن ما يشمله ذلك بالنسبة لإصلاح الحمض النووي والسلامة طويلة الأمد لم يكن واضحًا.
قطرات اصطناعية تحاكي مواقع إصلاح الحمض النووي الحقيقية
تبع المؤلفون PS‑ASOs الموسومة بمؤشر فلوري في خلايا بشرية ووجدوا أنها، عند الجرعات التجريبية الشائعة، تتراكم بسرعة في النواة وتؤسس هياكل كروية جديدة تُسمى أجسام PS. تتشكل هذه الأجسام بشكل اعتمادي على التركيز وتتصرّف مثل قطرات سائلة تندمج وتذوب وتعتمد على قوى جزيئية ضعيفة—وهي سمات انفصال الطور السائل-السائل. والأهم أنها لا تقع حيث تحدث كسور الحمض النووي الحقيقية ولا تحتوي على العلامات المعتادة للحمض النووي المكسور. بدلاً من ذلك، تُظهر الدراسة أن إنزيمات إصلاح الحمض النووي الرئيسية—بما في ذلك DNA‑PKcs وATM وATR وPARP1—ترتبط مباشرة بـ PS‑ASOs وتزداد بكثافة داخل هذه القطرات الاصطناعية، رغم سلامة الحمض النووي الأساسي.
إنذارات كاذبة تُفعّل إشارات تلف الخلية
بمجرد تكوينها، تقوم القطرات التي تؤسسها ASO بأكثر من حبس البروتينات سلبًا: فهي تُفعّل إنزيمات الإصلاح. خلال ساعة من دخول ASO، تُنشّط الإنزيمات داخل هذه القطرات وتبدأ بتعديل الكروماتين المجاور، مزينة بروتينات الهيستون بعلامات كيميائية تُرى عادةً بعد تلف حقيقي للحمض النووي. هذا يُطلق الاستجابة الكاملة لتلف الحمض النووي—مما يستدعي عوامل إصلاح إضافية، ويُشغّل إشارات نقاط التفتيش، ويقلّص نشاط محركات دورة الخلية المعروفة باسم CDKs. ونتيجة لذلك، تُبطئ الخلايا أو تتوقف عن التقدم خلال أطوار مهمة من دورة الخلية، خصوصًا عند النقطة التي تتحقق فيها عادةً من سلامة الحمض النووي قبل الانقسام. في أدمغة فئران تعرّضت لتوصيل ASO بمستويات سريرية، لاحظ الباحثون أيضًا ارتفاعًا في إشارات تلف الحمض النووي في المناطق ذات التقاط ASO الأعلى، مما يشير إلى أن هذه التأثيرات ليست محصورة على مزروعات الخلايا المختبرية.
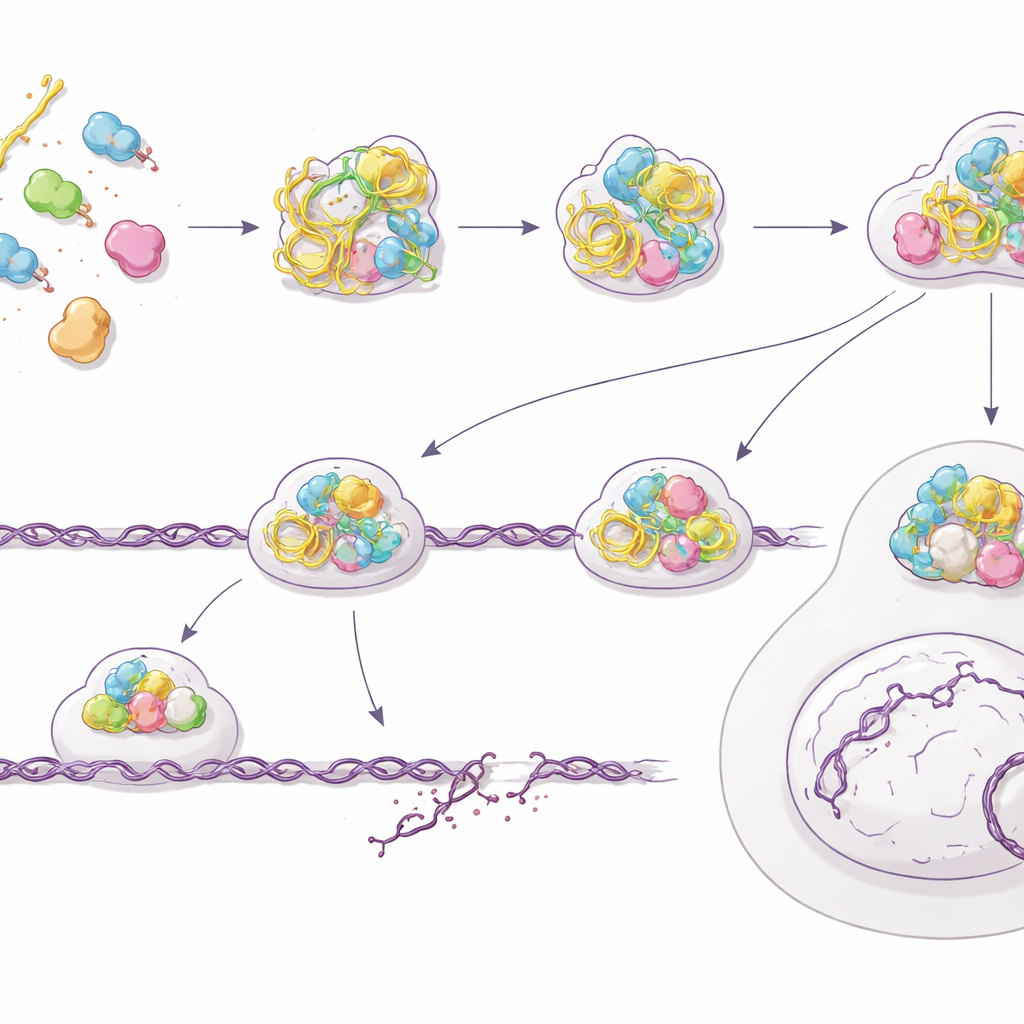
إصلاح على نحو خاطئ وزيادة مستمرة في كسور الحمض النووي
من المفارقات أنه بينما يزعق نظام إنذار الخلية، فإن قدرتها الفعلية على إصلاح الكسور الخطرة في الحمض النووي تتدهور. أظهر الفريق أن الخلايا المُعالجة مسبقًا بـ PS‑ASOs تكافح لتصفية التلف بعد التعرض للإشعاع بل وتتكاثر فيها الكسور العفوية، كما قاس ذلك بتجارب المذنبات وبؤر الإصلاح المستمرة. نظرة أقرب على أحد أكثر مسارات الإصلاح دقة—الإصلاح بالتناظر الجيني—كشفت المشكلة: الفاعلون الرئيسيون مثل BRCA2 وRAD51 يعجزون عن التجمع بشكل صحيح عند نهايات الحمض النووي المكسور، بينما تظهر علامات مبكرة لمعالجة تلك النهايات كما هي. باستخدام نظام تقرير وراثي، قدر المؤلفون انخفاضًا بنحو 60% في كفاءة الإصلاح بالتناظر الجيني بعد التعرض لـ PS‑ASO. تصبح الخلايا أقل قابلية للبقاء بشكل عام وأكثر حساسية للإشعاع بشكل ملحوظ، وهو ما يتوافق مع نظام إصلاح تُنبهه الإشارات لكنه لا يُنشَّط بشكل صحيح.
ما الذي يعنيه هذا لمستقبل أدوية استهداف الجينات
تشير النتائج مجتمعة إلى أن ASOs المعدلة بـ PS يمكن أن تُكوّن قطرات سائلة اصطناعية في النواة تُركز وتُفعّل إنزيمات إصلاح الحمض النووي حتى عندما لا يوجد تلف ليُصلح. هذا الإنذار الكاذب المزمن يخل بخيارات الإصلاح الطبيعية، لا سيما الإصلاح الدقيق بالتناظر الجيني، مما يؤدي إلى آفات حمض نووي مستمرة، وتنشيط نقاط التفتيش، وموت الخلايا. بينما تُرى أقوى التأثيرات عند مستويات نووية عالية من ASO النموذجية لتجارب النقل، يمكن اكتشاف تنشيط طفيف لإشارات التلف حتى عند جرعات منخفضة تشبه الدوائية. للمرضى ومطوري الأدوية، الرسالة واضحة: الخصائص الكيميائية التي تجعل ASOs أدوية فعالة قد تتداخل في بعض السياقات مع أهم ضامن في الخلية—قدرتها على الحفاظ على استقرار الجينوم—مما يؤكد الحاجة إلى تصميم هياكل خلفية أكثر أمانًا ومراقبة مسارات إصلاح الحمض النووي أثناء العلاج.
الاستشهاد: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
الكلمات المفتاحية: أوليغو نيوكليوتيدات معاكسة, استجابة تلف الحمض النووي, انفصال الطور السائل, إصلاح بالتناظر الجيني, استقرار الجينوم