Clear Sky Science · ar
مُقلّدات الببتيدوغليكان الكيرالية تستهدف تخليق جدار البكتيريا للتدخل ضد الممرضات
نهج جديد لصيد الجراثيم الضارة
تتزايد الإصابات المقاومة للمضادات الحيوية في جميع أنحاء العالم، ومع ذلك لا يزال الأطباء يفتقرون إلى أدوات يمكنها تحديد ومهاجمة البكتيريا الضارة بدقة دون الإضرار بخلايا الجسم. تعرض هذه الدراسة «طُعمًا» جزيئيًا ذكيًا يقلّد مكوّنًا أساسيًا في جدران الخلايا البكتيرية. يمكن لهذه الجزيئات المصممة أن تُضيء مواقع العدوى للتصوير وأن تنقل المضادات الحيوية مباشرة إلى الميكروبات، مقدّمة استراتيجية جديدة لمواجهة الممرِضات التي يصعب علاجها.
تقليد درع البكتيريا
تحاط البكتيريا بشبكة صلبة تُسمى جدار الخلية، مكونة من سكريات وأحماض أمينية مرآتية غير معتادة لا تستخدمها خلايا الثدييات إلى حد كبير. استغل الباحثون هذا الفارق عبر إنشاء سلاسل طويلة قائمة على السكريات مزدانة بصورة مرآتية محددة من الألانين، وهو حمض أميني شائع. تُصمم هذه السلاسل، المسماة مُقلّدات الببتيدوغليكان الكيرالية، لتشبه عن قرب المكوّنات الطبيعية التي تستخدمها البكتيريا لبناء جدرانها، بينما تكون غائبة في الأنسجة الدماغية للثدييات. من خلال ضبط كمية الألانين ذي الشكل D المُرفقة، أنتج الفريق نسخًا تُفضّل البكتيريا بقوة على خلايا الإنسان.
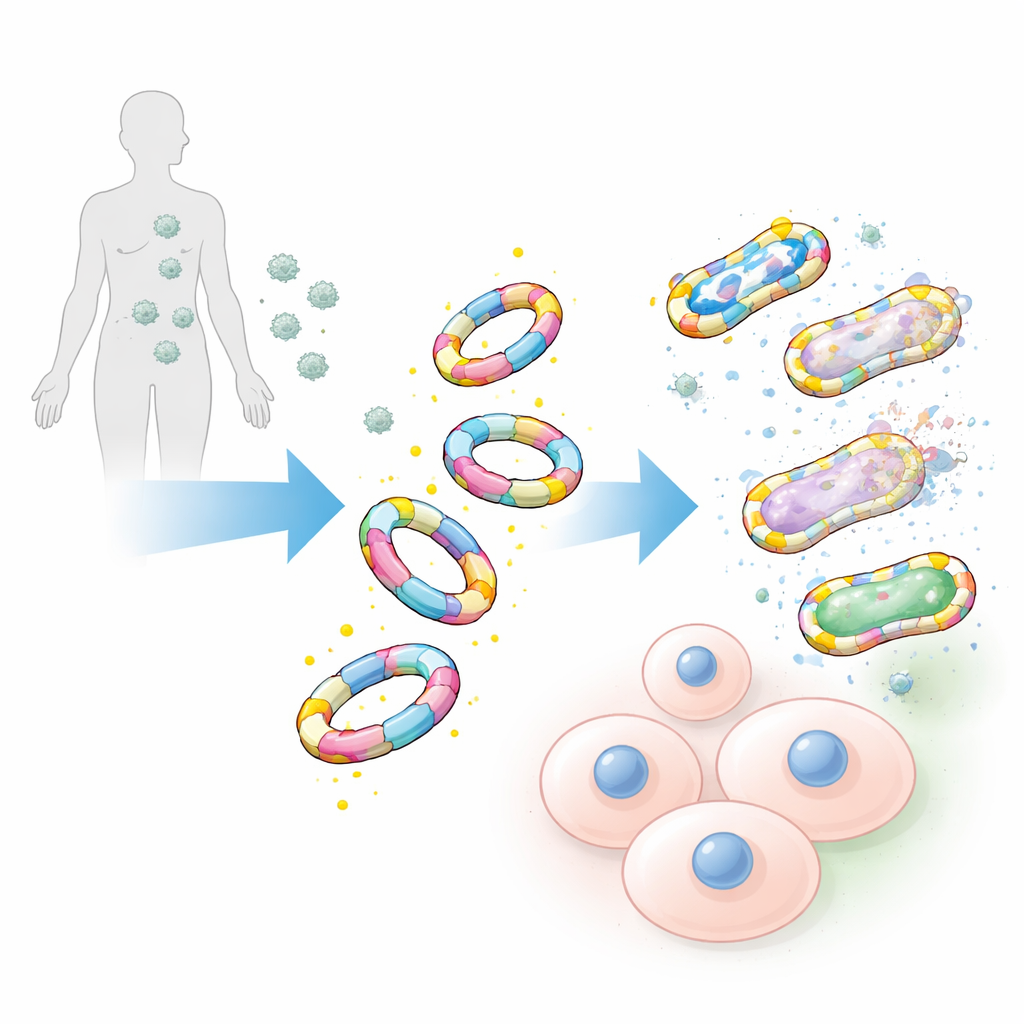
الالتصاق بالبكتيريا، لا بخلايا الجسم
عند اختباره ضد مجموعة واسعة من المُمْرِضات، بما في ذلك سلالات المستشفيات الشهيرة مثل المكورات العنقودية الذهبية المقاومة للميثيسيلين وغيرها من بكتيريا ESKAPE، ارتبطت المُقلّدات المزدانة بألانين-D بسطوح البكتيريا بكفاءة لافتة. أقرانها المرآتيون المبنيون من شكل الألانين L، وكذلك سلاسل السكريات الأصلية وحدها، أظهروا ارتباطًا ضعيفًا أو منعدمًا. كما قارن الفريق هذه المُقلّدات الكبيرة بمسبارات كيميائية تقليدية صغيرة مبنية على جزيئات ألانين-D مفردة. حتى عندما أصبحت المسبارات الصغيرة ساطعة جدًّا، فقد وسمت عددًا أقل بكثير من البكتيريا وأعطت إشارات أضعف، ما يؤكد قوة التصميم الأكبر والأكثر شبهاً بالطبيعة.
اختطاف خط تجميع جدار الخلية
لفهم سبب قوة التعرّف هذه، فحص العلماء كيفية تفاعل المُقلّدات مع آلية بناء جدار البكتيريا. وجدوا أن السلاسل القائمة على ألانين-D لا تلتصق بالسطح فحسب؛ بل تُؤخذ كما لو كانت مكوّنات بناء حقيقية وتُدخل في نفس الخطوات الإنزيمية التي تربط مكوّنات جدار الخلية عادةً معًا. كشفت التحاليل الكيميائية عن وسائط جديدة تنشأ فقط عند وجود هذه المُقلّدات، وأظهرت المحاكاة الحاسوبية أن إنزيمات بناء الجدار الرئيسية تمسك بالمُقلّدات بقوة أكبر مما تمسك بالركائز الطبيعية. عبر عدة دورات من نمو البكتيريا، تراكمت المُقلّدات في الجدار، مُشوِّهة هيكله تدريجيًا وجاعلةً إياه متسرّبًا.
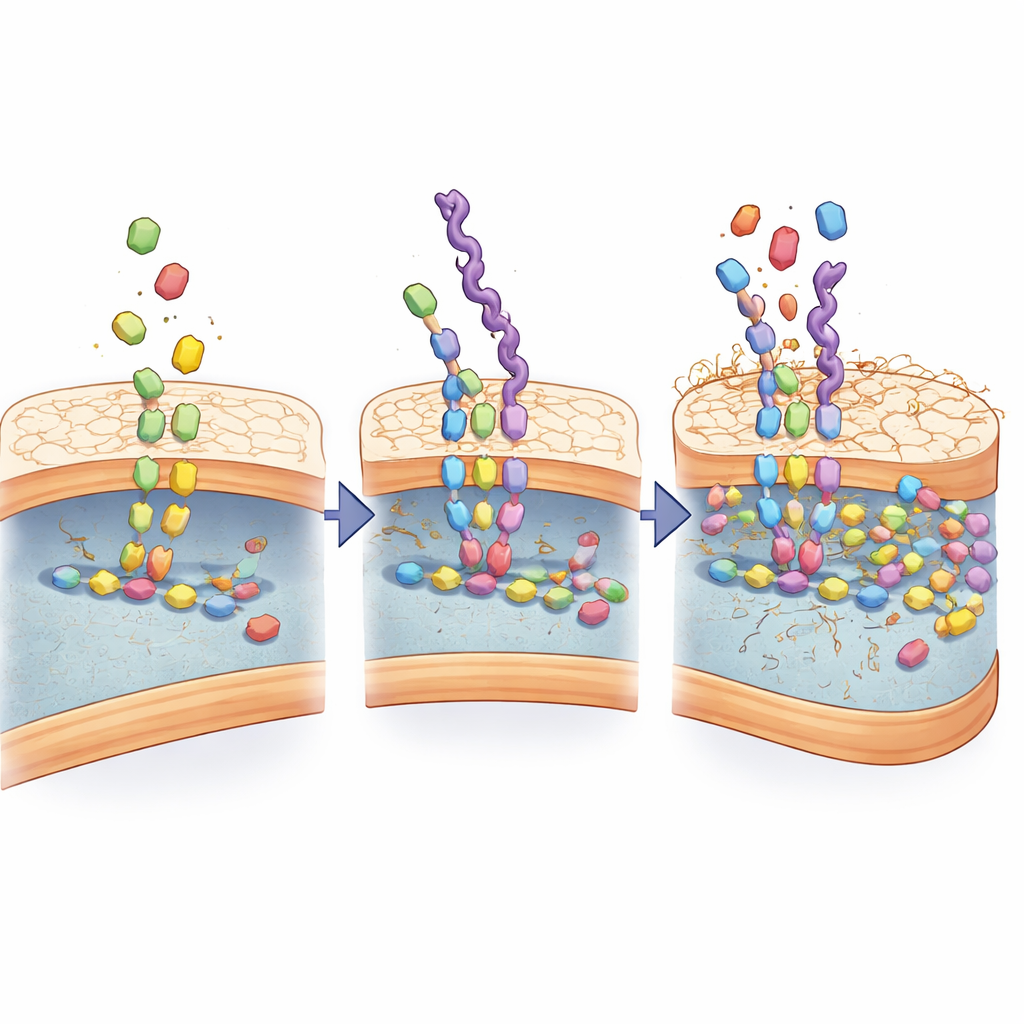
تحويل المُقلّدات إلى حوامل ذكية للأدوية
لأن هذه السلاسل تتجمع طبيعياً إلى جزيئات صغيرة في الماء وتحمل العديد من نقاط الوصل الكيميائية، استخدمها الفريق كحوامل للأصباغ التصويرية والمضادات الحيوية. أصدرت النسخ الفلورية محاذاة واضحة للبكتيريا في زرعات خلوية، مع تداخل ضئيل مع الخلايا الثديية المزروعة جنبًا إلى جنب. ثم حمّل الباحثون المضاد الحيوي تيتراسايكلين داخل الجسيمات القائمة على المُقلّدات. في تجارب المختبر، جعلت هذه التغليفات التتراسايكلين أكثر فعالية عدة مرات، ميتةً حتى السلالات المقاومة بجرعات أقل بكثير من الدواء الحر. أظهرت الميكروسكوبات أن المُقلّدات المحمّلة بالمضاد الحيوي تملأ على البكتيريا، وتخترق أغلفتها، وتسبب موتًا واسعًا للخلايا مقارنة بالتركيبات غير الموجهة.
مكافحة العدوى داخل الجسم
أصعب الاختبارات جرت في نماذج فأرية لجروح جلدية موضعية وعدوى بطنية مهدِّدة للحياة. في الجروح المصابة، حوّلت المُقلّدات الفلورية نحو البكتيريا العميقة في الأنسجة، وعند حملها التتراسايكلين، قضت تقريبًا على الميكروبات بالكامل. أدى ذلك إلى شفاء أسرع، وطبقة جلد جديدة أكثر سمكًا، وترتيب أفضل لترسّبات الكولاجين، ونمو أغنى للأوعية الدقيقة. في نماذج العدوى الجهازية، تراكمت المُقلّدات بشكل محدد في أعضاء مصابة مثل الطحال والرئتين، حيث خفضت أعداد البكتيريا بشكل حاد عند تحميلها بالمضاد الحيوي. والأهم من ذلك، أن الجرعات العالية من المُقلّدات وحدها أظهرت سلامة جيدة، دون أضرار ظاهرية للأعضاء الرئيسية أو لمعاملات الدم.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
بناء نسخة كيميائية قريبة الشبه من مكونات جدار الخلية البكتيرية، تُظهر هذه الدراسة طريقة جديدة لـ"الاندماج" مع أيض الممرض بدلاً من الهجوم فقط من الخارج. تعمل هذه المُقلّدات الكيرالية كمنارات عالية الدقة للتصوير وكمركبات ذكية توجه المضادات الحيوية مباشرة إلى أهدافها الميكروبية، بما في ذلك السلالات المقاومة، مع حفظ خلايا الثدييات. إذا تُرجمت إلى أدوات سريرية، فقد تساعد مثل هذه المنصات المقلّدة للطبيعة الأطباء على رؤية مكان تمركز العدوى بدقة ومعالجتها بفعالية أكبر وبجرعات دواء أقل، مقدّمة سلاحًا واعدًا ضد التحدي المتزايد لمقاومة الميكروبات للمضادات الحيوية.
الاستشهاد: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
الكلمات المفتاحية: مقاومة المضادات الحيوية, جدار الخلية البكتيرية, توصيل الدواء الموجه, التصوير الجزيئي, النانوطب