Clear Sky Science · ar
تشريح متعدد الوسائط لمَرَضية TDP-43 الخاصة بأنواع الخلايا في قشرة الحركة
لماذا تهم هذه الدراسة الناس
التصلب الجانبي الضموري (ALS) والخرف الجبهي الصدغي (FTD) أمراض دماغية مدمرة تسلب الأشخاص القدرة على الحركة والكلام والشخصية. يشترك معظم مرضى ALS والعديد من مرضى FTD في علامة مجهرية مشتركة: تراكم كتل من بروتين يُدعى TDP-43 في أماكن لا ينبغي أن يتواجد فيها. تطرح هذه الدراسة سؤالين عمليين لهما تداعيات كبيرة على العلاجات المستقبلية: أي الخلايا الدماغية تُصاب بشدة بمشكلات TDP-43، وماذا يحدث داخل تلك الخلايا على مستوى تنظيم الحمض النووي والنشاط الجيني؟
تتبع الضرر إلى مركز الحركة في الدماغ
ركز الباحثون على القشرة الحركية الأولية، الشريط من نسيج الدماغ الذي يتحكم في الحركة الإرادية. باستخدام عينات دماغية متبرع بها بعد الوفاة من أشخاص مصابين بـ ALS وALS-FTD ومن ضوابط عصبية سليمة، عزلوا أنوية خلايا فردية وقرأوا أي الجينات كانت نشطة وكيف كانت كثافة التغليف المحلي للحمض النووي. سمح هذا النهج «متعدد الأوميكس»، الذي طُبِّق على أكثر من 180,000 نواة، بتصنيف الخلايا إلى أنواع دقيقة: عدة أصناف من الخلايا المثيرة والمثبطة، وكذلك خلايا داعمة مثل الخلايا النجمية والخلايا قليلة التغصن والميكروغليا. ثم جمعوا ذلك مع خرائط جينية مكانية من مجموعة بيانات بشرية أخرى لوضع هذه الأنواع الخلوية داخل البنية الطبقية المألوفة للقشرة.
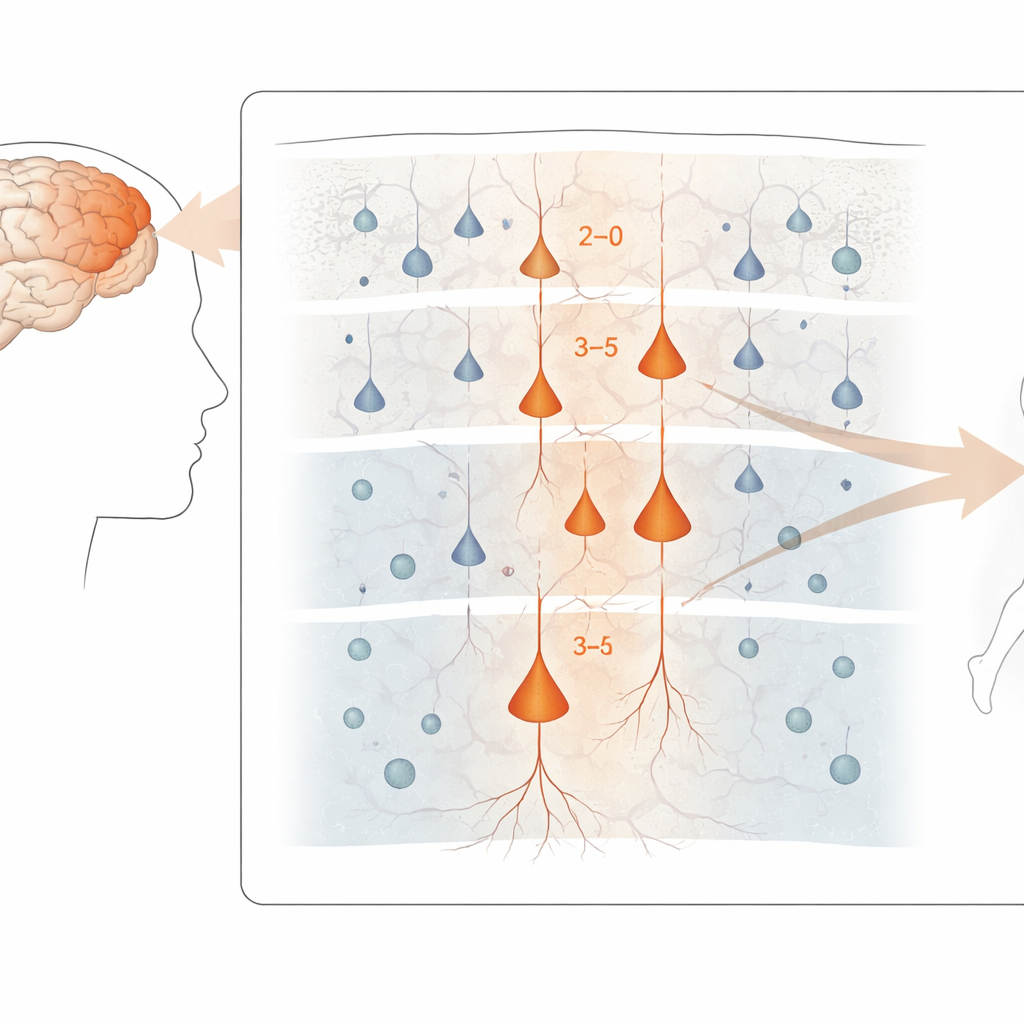
تحديد الخلايا العصبية الأكثر عرضة للخطر
عبر القشرة الحركية، بدت أقوى التغيرات الجينية المرتبطة بالمرض في الخلايا العصبية المثيرة، وهي الخلايا التي تدفع النشاط على طول الدارات الدماغية. على وجه الخصوص، أظهرت خلايا القشر العلوية والوسطى التي تتواصل ضمن القشرة، بالإضافة إلى بعض الخلايا العميقة التي ترسل إشارات خارج القشرة—بما في ذلك خلايا «بيتز» الكبيرة التي تتحكم في الخلايا الحركية النخاعية—أكثر التغييرات وضوحًا. بالمقابل، كانت الخلايا البينية المثبطة والعديد من الخلايا الداعمة أقل تضررًا على مستوى التعبير الجيني، رغم أن بعضًا منها أظهر تغيرات أدق. وبالرغم من هذه الاضطرابات الجزيئية، كان مزيج أنواع الخلايا الرئيسة في النسيج مماثلًا بشكل مدهش بين المرضى والضوابط، ما يوحي بأن الضرر يتعلق أكثر بكيفية عمل الخلايا منه بعدد الخلايا المفقودة فحسب.
كيف يعيد TDP-43 تشكيل النشاط الجيني من الداخل
لفصل التأثيرات الناتجة مباشرة عن TDP-43 عن عمليات مرضية أخرى، استخدم الفريق استراتيجية فصل ذكية. علموا الأنوية بأجسام مضادة ضد TDP-43 وعلامة عصبية، ثم استخدموا فرز التدفق لفصل الخلايا العصبية التي فقدت أنويتها TDP-43 (علامة على المَرَضية) عن تلك التي احتفظت به. كشف تسلسل أكثر من 12,000 من هذه الأنوية أن فقدان TDP-43 يحدث بصورة ساحقة في الخلايا العصبية المثيرة، خصوصًا أنواع فرعية محددة في الطبقات 2–3، 3–5، 5، و6. في تلك الخلايا العصبية الضعيفة، أُسيء تنظيم مئات الجينات، بما في ذلك العديد المرتبطة سابقًا بـ ALS. كانت البصمات الجزيئية الكلاسيكية لفشل TDP-43—مثل ظهور قطع «خفيّة» إضافية في نسخ جينات STMN2 وKALRN، وتحولات في مواقع قصّ وذيل الحمض الريبي—غنية بوضوح في الأنوية الناقصة TDP-43.
إعادة تشكيل فوق جينية: ليس كل التغيير ناتجًا عن TDP-43
نظرًا لأنهم قاسوا كلًا من النشاط الجيني وانفتاح الكروماتين في نفس الأنوية، استطاع المؤلفون أن يسألوا أي التغيرات ارتبطت بتبدلات في تغليف الحمض النووي. وجدوا عشرات آلاف المواقع في الجينوم حيث تتبع قابلية الوصول إلى الكروماتين التعبير الجيني. العديد من الجينات المتغيرة في ALS وALS-FTD تقع في مثل هذه المناطق، مما يشير إلى أن جزءًا من بصمة المرض يعكس إعادة تشكيل فوق جينية أوسع بدلًا من أن تكون نتيجة مباشرة لفقدان TDP-43. ومن المثير للاهتمام أن هذه التغيرات المرتبطة بالكروماتين غالبًا ما تلاقت على مسارات إشارية تتعلق بتواصل الخلايا وتوجيه المحاور العصبية، وكانت قوية بشكل خاص في أنواع معينة من الخلايا العصبية المثيرة والخلايا قليلة التغصن. عندما قارن الفريق التغيرات الجينية المرتبطة بمرضية TDP-43 مع تلك المرتبطة بتبدلات الكروماتين، رأوا أنها متداخلة جزئيًا لكنها في الغالب طبقات اضطراب مميزة ومختلفة.
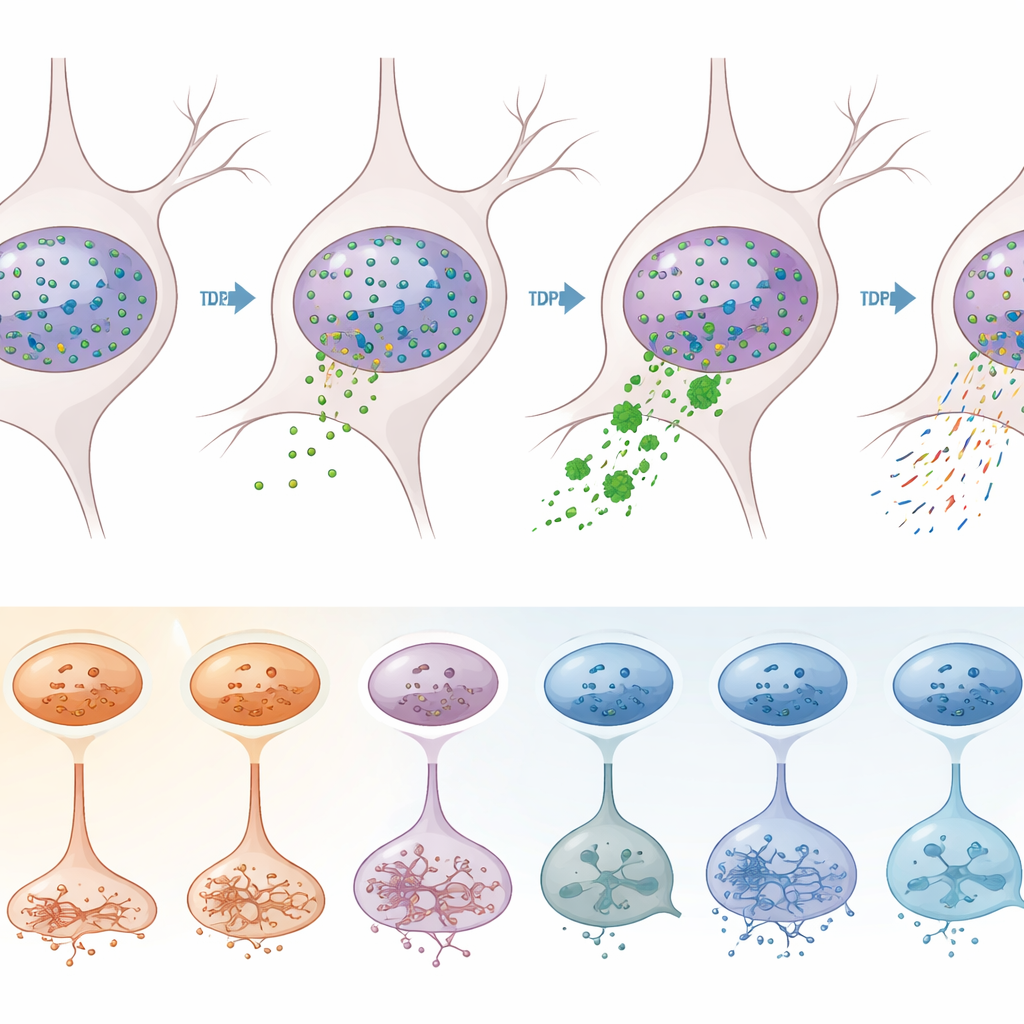
ما الذي يعنيه هذا للعلاجات المستقبلية
بالنسبة للقارئ العادي، الرسالة الأساسية هي أن ALS وALS-FTD لا يدمران القشرة الحركية بشكل موحد. بل يهاجمان أنواعًا معينة من الخلايا العصبية المثيرة وإلى درجة أقل بعض الخلايا الداعمة، ويغيرون برامجها الجينية بطرق تعتمد على كل من سلوك TDP-43 الخاطئ والتغيرات الأوسع في كيفية تغليف وقراءة الحمض النووي. تشير هذه النتائج إلى أن العلاجات الفعالة قد تحتاج إلى أن تكون محددة بحسب نوع الخلية والمسار—على سبيل المثال، استعادة وظيفة TDP-43 أو تصحيح أخطاء فردية في عملية الربط التتابعي (splicing) في الخلايا العصبية الأكثر عرضة، مع استهداف مستقل للتغيرات فوق الجينية والإشارية المشتركة عبر أنواع خلوية متعددة. من خلال رسم هذا المشهد المعقد بتفصيل عالٍ، توفر الدراسة مخططًا لتصميم تدخلات أكثر دقة تهدف إلى إبطاء أو منع فقدان التحكم الحركي في ALS وALS-FTD.
الاستشهاد: Ruf, W.P., Kühlwein, J.K., Meier, L. et al. Multi-modal dissection of cell-type specific TDP-43 pathology in the motor cortex. Nat Commun 17, 2406 (2026). https://doi.org/10.1038/s41467-026-69944-6
الكلمات المفتاحية: التصلب الجانبي الضموري, الخرف الجبهي الصدغي, TDP-43, خلايا قشرة الحركة العصبية, تعدد الأومكس النووي المفرد