Clear Sky Science · ar
خلايا Th17 تحتاج مستقبل إصلاح الحمض النووي مجموعة تكملة الصباغية الشمسية C للتحكم في تلف الحمض النووي التأكسدي في نموذج فأري
حراس مدافعي جهاز المناعة لدينا
خلايا المساعد T من النوع 17، أو خلايا Th17، هي نوع خاص من خلايا الدم البيضاء يفتش حواجز أجسامنا مثل الأمعاء والجلد لصد البكتيريا والفطريات. لكنها تشارك أيضاً في الأمراض المناعية الذاتية عندما تنحرف استجابتها. تسأل هذه الدراسة سؤالاً يبدو بسيطاً لكنه جوهري: كيف تحافظ هذه الخلايا النشطة بشدة على حمضها النووي من الإجهاد الكيميائي الذي تولده أثناء مكافحة العدوى؟ الجواب يتمحور حول مجس تلف الحمض النووي المسمى XPC، المعروف أساساً بحماية خلايا الجلد من ضوء الشمس. هنا يبيّن الباحثون أن XPC ضروري أيضاً للحفاظ على خلايا Th17 صحية ونشيطة وفعالة.
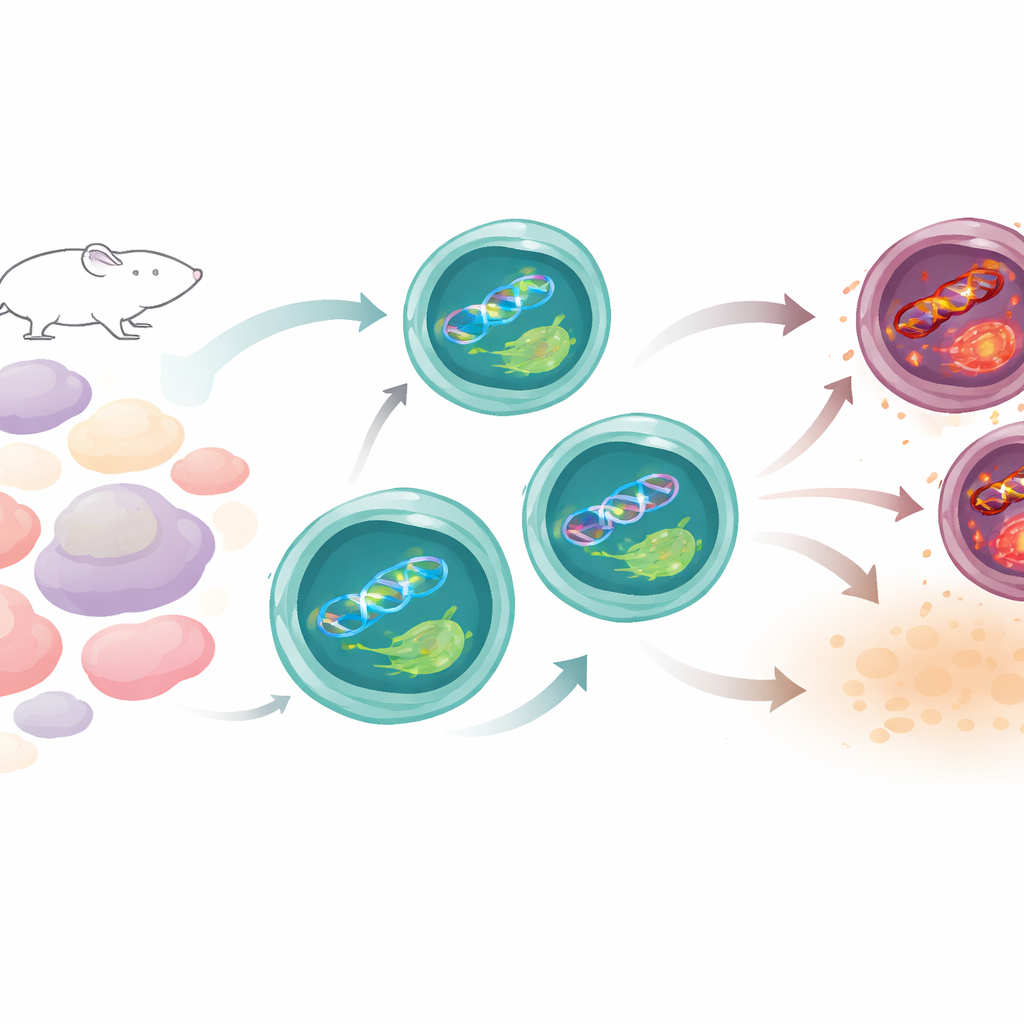
كيف تحافظ خلايا Th17 على التوازن عادةً
تعيش خلايا Th17 حياة محفوفة بالمخاطر. لكي تؤدي وظيفتها، تزيد من معدل الأيض وتنتج أنواعاً تفاعلية من الأكسجين — جزيئات كيميائية تهاجم أحياناً الحمض النووي. قارن الفريق خلايا Th17 بأنواع أخرى من خلايا T في الفئران ووجد أنه بالرغم من نشاطها المكثف، تتراكم لدى خلايا Th17 أضرار حمض نووي أقل من كثير من أقاربها. كانت علامة دالة أن الجينات المشاركة في إصلاح الحمض النووي، وخصوصاً تلك في مسار يصلح التلف الناتج عن الشمس، نشطة بشدة في خلايا Th17. ومن بينها XPC، وهو بروتين يفحص الحمض النووي بحثاً عن التلف البنيوي. مع نضوج خلايا Th17، زادت مستويات XPC وتركزت في مواقع التلف داخل النواة، ما يوحي بأنه في حالة دورية للحفاظ على سلامتها الجينية.
ماذا يحدث عندما يغيب مجس الحمض النووي
لفهم مدى أهمية XPC فعلاً، استخدم الباحثون فئراناً معدلة جينياً تفتقر لهذا البروتين. للوهلة الأولى بدا جهازها المناعي طبيعياً إلى حد كبير: أعداد الخلايا T العامة والعديد من الأنماط الفرعية لخلايا T بقيت دون تغيير. لكن عندما ركز الفريق على خلايا Th17 ظهر عيب واضح. من دون XPC، أنتج عدد أقل بكثير من الخلايا جزيء IL-17 المميز لخلايا Th17، وانخفضت علامات الهوية والمفاتيح الإشارية التي تدفع برنامج Th17. في الأطباق المزرعة، كافحت خلايا T البدائية من هذه الفئران لتتحول إلى خلايا Th17 مكتملة النضج. وفي نموذج معياري حيث تُنقل خلايا T لتثير التهاباً معوياً، فشلت خلايا T الخالية من XPC في تحريض التهاب القولون، مما يعكس قدرة التهابية مخففة. في الوقت نفسه، ازداد عدد الخلايا التنظيمية T التي تهدئ الاستجابات المناعية، مما يوحي بتحول التوازن بين العدوان والكبح.
تلف الحمض النووي ومصانع الطاقة والإجهاد الكيميائي
بالتعمق أكثر، وجد الفريق أن خلايا Th17 من دون XPC احتوت على مزيد من خيوط الحمض النووي المكسورة وقواعد حمض نووي مؤكسدة أكثر، وهو بصمة لهجوم أنواع الأكسجين التفاعلية. كما انخفضت الجينات التي عادةً ترصد تلف الحمض النووي وتوقف دورة الخلية، ما يشير إلى ضعف نظام الإنذار. تبدل أيض الخلايا: فقدت بعض قدرتها على استخدام مسارات السكر السريعة وأصبحت أكثر اعتماداً على الميتوكوندريا، مصانع الطاقة الصغيرة داخل الخلايا. ومع ذلك كانت هذه الميتوكوندريا تتسرب منها المزيد من أنواع الأكسجين التفاعلية وأظهرت علامات إجهاد، مكوّنة حلقة مفرغة من تزايد الإجهاد الكيميائي وتفاقم تلف الحمض النووي. ومن اللافت أن معالجة الخلايا بمضاد أكسدة أعاد إنتاج IL-17 وقلل تلف الحمض النووي، مما يربط الإجهاد التأكسدي مباشرة بالعطل الوظيفي الملاحظ.
جهود جماعية في إصلاح الحمض النووي التالف
بعيداً عن دورها التقليدي، عمل XPC جنباً إلى جنب مع بروتين إصلاح آخر يُدعى OGG1، الذي يتعرف على قاعدة حمض نووي مؤكسدة شائعة. أظهر الباحثون أن هذين البروتينين يرتبطان جسدياً في خلايا Th17، مما يساعد في تنسيق إزالة القواعد التالفة. عندما غاب XPC، ازداد نشاط قص OGG1 فعلياً، كما لو كان يحاول التعويض عن التلف الزائد. لكن هذا الإفراط في النشاط حدث في سياق إجهاد تأكسدي عالٍ وشبكات إصلاح مضطربة، فلم يكن كافياً لاستعادة وظيفة Th17 الطبيعية. أظهرت تحليلات جينية وهيكلية أن XPC يعمل كمركز يربط مسارات إصلاح مختلفة والتحكم في حالة الأكسدة، ضامناً ألا يقتصر الكشف على التلف بل يُعالَج بطريقة تسمح للخلية بالاستمرار في الانقسام وإنتاج الجزيئات الوقائية.
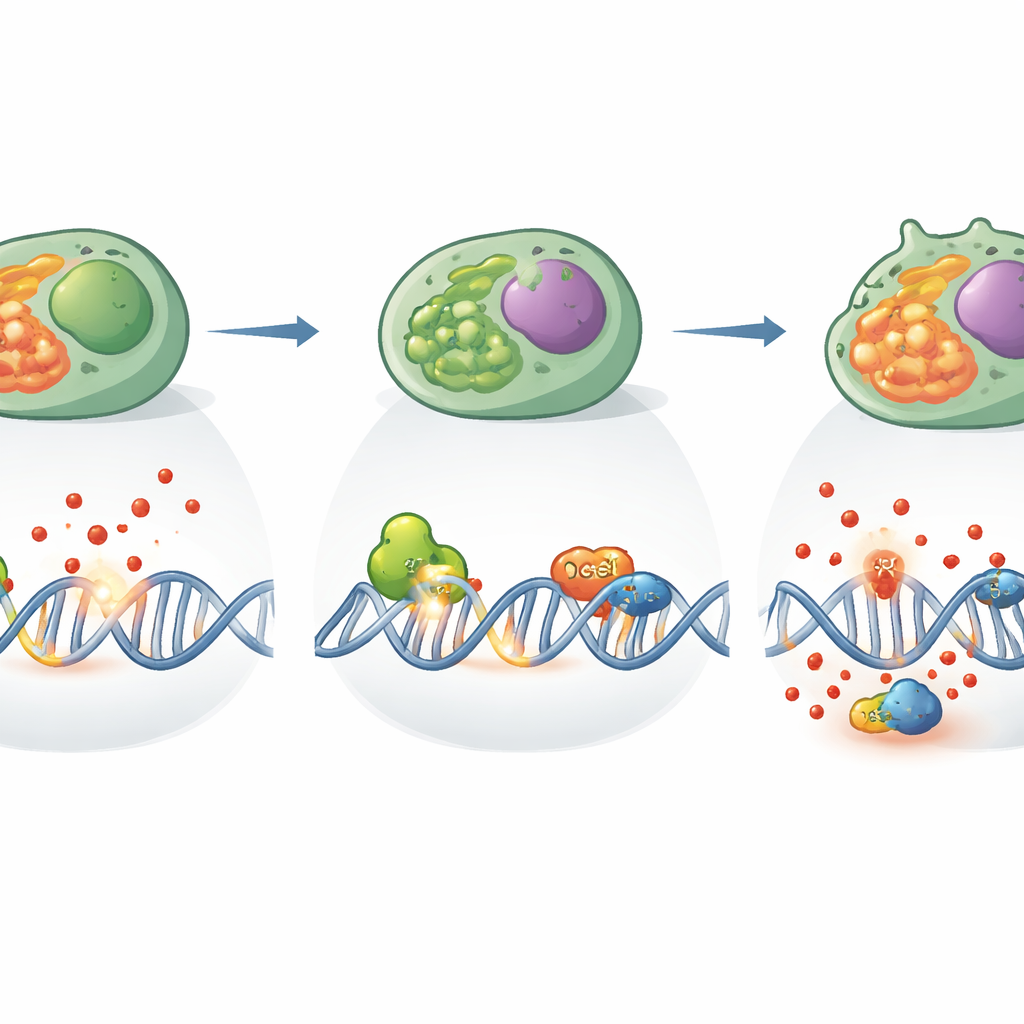
لماذا هذا مهم للمرض والعلاج
للقارئ العام، الرسالة الأساسية أن خلايا المناعة تحتاج إلى حراس داخلية لتبقى لائقة بينما تحمينا. تكشف هذه الدراسة أن XPC، المعروف سابقاً بحماية خلايا الجلد من الأشعة فوق البنفسجية، هو أيضاً حارس حيوي لخلايا Th17، يحافظ على سلامة حمضها النووي وتوازن نظم طاقتها تحت الإجهاد التأكسدي. عندما يغيب XPC، تصبح خلايا Th17 هشة جينياً وعضوياً، تنتج مخرجات التهابية أقل، وقد يتحول التوازن المناعي نحو التنظيم بدلاً من الهجوم. ونظراً لأهمية خلايا Th17 في حالات مثل داء الأمعاء الالتهابي والصدفية والتصلب المتعدد، قد تصبح المسارات التي يتحكم فيها XPC أهدافاً جديدة لضبط الاستجابات المناعية — إما لتهدئة الالتهاب الضار أو لتعزيز الدفاع حيث يكون ضعيفاً — من خلال تعديل كيفية إصلاح هذه الخلايا لحمضها النووي والتعامل مع الإجهاد التأكسدي.
الاستشهاد: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
الكلمات المفتاحية: خلايا Th17, إصلاح الحمض النووي, الإجهاد التأكسدي, بروتين XPC, مرض ذاتي المناعة