Clear Sky Science · ar
عامل بدء النسخ في حقيقيات النوى eIF6 يضبط لَدونة سرطان الرئة صغير الخلايا عبر محور إشارة الإنتغرين-FAK
لماذا يهم هذا البحث في سرطان الرئة
سرطان الرئة صغير الخلايا (SCLC) هو واحد من أشد أنواع سرطان الرئة فتكًا. عادة ما يستجيب جيدًا للعلاج الكيميائي في البداية، لكن يعود في معظم الحالات بسرعة وبشكل عدواني. يطرح هذا البحث سؤالاً محورياً: ما الذي يسمح لخلايا SCLC بـ «تغيير سلوكها» وتصبح مقاومة للأدوية، وهل يمكن إبطاء هذا التحول أو منعه؟
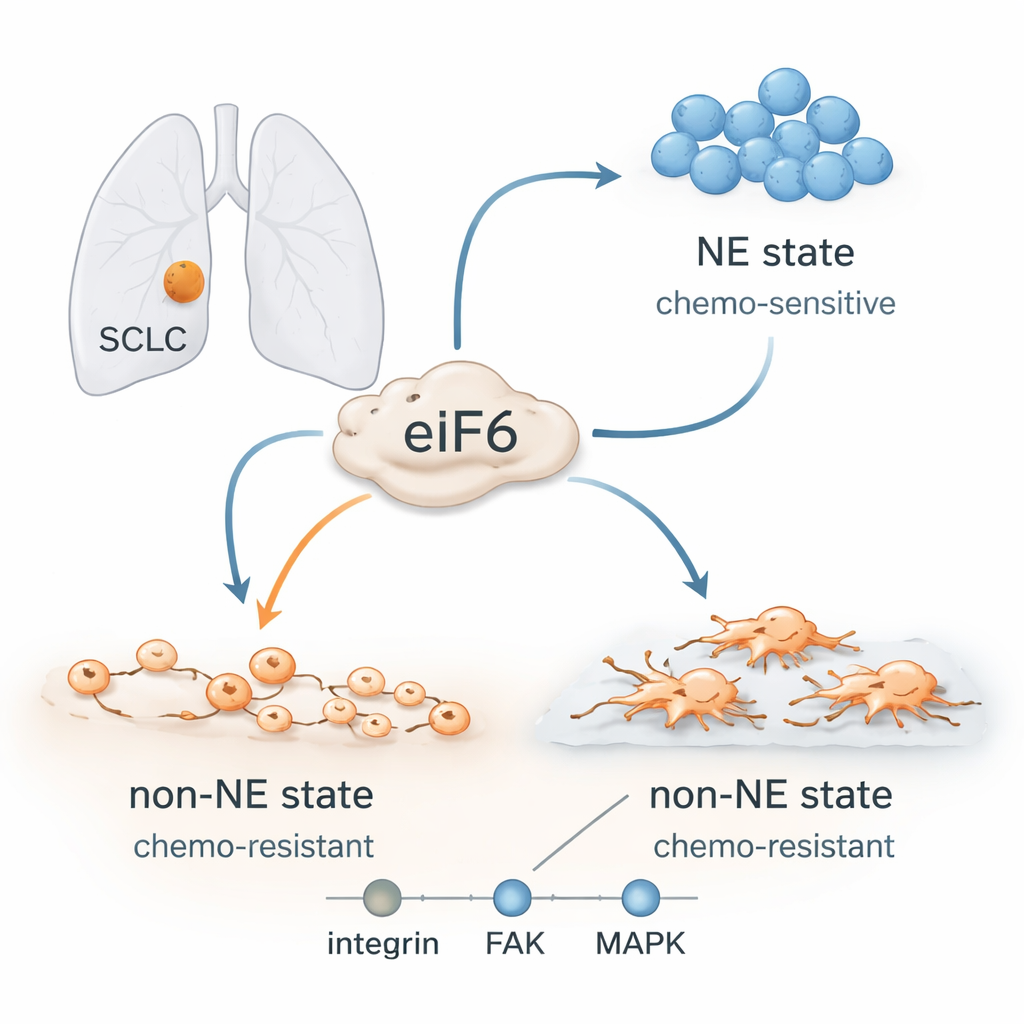
الخلايا السرطانية المتغيرة الشكل
كان الأطباء يعتقدون سابقًا أن SCLC مرض متجانس، لكن أصبح واضحًا الآن أن هذه الأورام تحوي أنواعًا خلوية مختلفة. بعض الخلايا تملك هوية «صماوية عصبية» قوية: تنمو في عناقيد عائمة متراصة، تستجيب جيدًا للعلاجات المحتوية على البلاتين، وتكون غنية ببروتينات تشبه البروتينات العصبية. أخرى تفقد هذه الهوية وتتخذ حالة «غير صماوية عصبية»: تنتشر، وتلتصق بالأنسجة المحيطة، وتظهر سمات خلايا أكثر حركة وغزوًا، وتصبح أصعب بكثير في القتل بالأدوية. غالبًا ما تتطور أورام المرضى من الحالة الحساسة إلى الحالة المقاومة أثناء العلاج أو بعده، رغم أن حمضهم النووي لا يتغير كثيرًا. هذا يشير إلى برمجيات خلوية مرنة بدلاً من طفرات جديدة كمحرِّك للانتكاس.
عامل ترجمة بحياة مزدوجة
ركز المؤلفون على بروتين يسمى eIF6، المعروف أساسًا بمساعدته في تجميع الرايبوسومات، مصانع البروتين داخل الخلايا. من خلال دراسة عينات المرضى ونماذج الفئران وعدة خطوط خلوية بشرية من SCLC، وجدوا أن مستويات eIF6 ترتفع باستمرار عندما تتحول الخلايا إلى الحالة المقاومة وغير الصماوية العصبية. وبشكل مفاجئ، صاحبت هذه الزيادة هبوط عام في إنتاج البروتين الكلي، مما يوحي بأن eIF6 قد يقوم بأدوار إضافية إلى جانب وظيفته المعروفة. أظهرت تحليلات مفصلة لكيفية ارتباط الرنا المرسال بالرايبوسومات أن الأجزاء الأساسية للرايبوسوم لم تتغير كثيرًا. بل أعيد تشكيل طريقة اختيار الرسائل ومعالجتها للترجمة عندما غيرت الخلايا هويتها.
الانفصال لربط إشارات البقاء
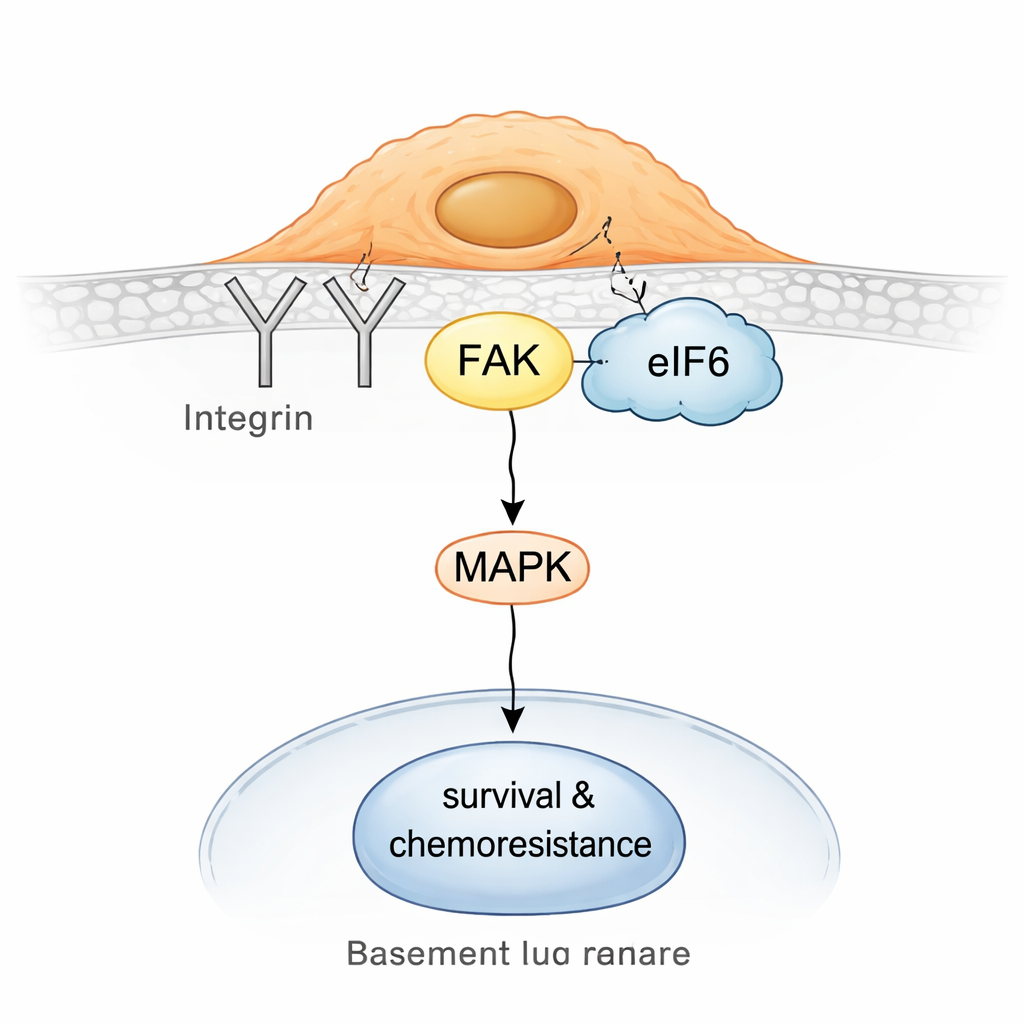
بتعمق أكثر، اكتشف الفريق أنه في الخلايا المقاومة ينفصل جزء من eIF6 عن الرايبوسومات ويرتبط بمحور إشاري سطحي مبني حول الإنتغرين وبروتين يسمى كيناز التصاق البؤرة (FAK). تساعد الإنتغرينات الخلايا على استشعار والتشبث بمحيطها؛ وينقل FAK تلك الإشارات إلى الداخل، غالبًا مفعّلًا مسارات تدعم الحركة والبقاء وتحمل الدواء. أظهرت سحبات بيوكيميائية وتجارب قرب داخل الخلايا أن eIF6 يتفاعل فعليًا مع شريك الإنتغرين CD104 ومع FAK، وأن هذه المجمعات أكثر وفرة في الخلايا غير الصماوية العصبية. بدوره يعزز هذا التجميع eIF6–إنتغرين–FAK نشاط مسار إشارة MAPK، وهو محرك معروف للنمو ومقاومة الإجهاد.
إعادة جعل الأورام المقاومة عرضة مرة أخرى
ثم تساءل الباحثون عمّا إذا كان التلاعب بمستويات eIF6 قادرًا على تغيير سلوك SCLC. عندما قللوا مستويات eIF6 في الخلايا المقاومة، تم خفض التعبير عن جينات مرتبطة ببرنامج حركي ومكوّن للندبات (التحول الطلائي البطاني-اللُّمفي) بينما استعادت جينات صماوية عصبية كلاسيكية جزئيًا. لم تُعد هذه التغييرات الخلايا بالكامل إلى الحالة السابقة، لكنها أبطأت الانتقال نحو الحالة المقاومة. والأهم أن الخلايا ذات eIF6 المنخفض أصبحت أكثر حساسية للعلاج الكيميائي القياسي بالكاربوبلاتين–إتوبوسايد في المختبر وفي أورام الفئران، حيث تركت مستعمرات أقل ناجية وانكماشًا أطول أمداً. وبما أن eIF6 نفسه يفتقر حاليًا إلى عقارات محددة، اختبر الفريق مثبطات FAK التي هي بالفعل قيد التطوير سريريًا. أدى حجب إشارة FAK إلى إعادة حساسية الخلايا المقاومة للعلاج الكيميائي، وفي الفئران أنتج العلاج المركب أقوى تحكم بالأورام.
من بصيرة مخبرية إلى أدوات مستقبلية للمرضى
أخيرًا، فحص المؤلفون عينات أورام من مرضى مصابين بـ SCLC في مرحلة محدودة خضعوا للعملية الجراحية. باستخدام طريقة تلوين حساسة تضيء البروتينات فقط عندما تكون قريبة من بعضها، قاسوا مدى تواجد eIF6 ضمن مركبات مع CD104 أو FAK داخل خلايا الورم. رُبطت المستويات العالية لهذه المجمعات—أكثر من eIF6 وحده—بحدوث انتكاس مبكر وبمدة بقاء أقصر، مما يجعلها مؤشرات تنبؤية واعدة. مجتمعة، تكشف هذه الدراسة أن eIF6 يمكن أن «يمارس عملًا ثانويًا» بعيدًا عن الرايبوسومات ليسهم في ربط خلايا السرطان بدوائر بقاء قوية. من خلال رسم خرائط محور eIF6–إنتغرين–FAK، يقترح العمل طرقًا لتحديد المرضى ذوي المخاطر الأعلى للانتكاس ويدعم الجمع بين مثبطات FAK والعلاج الكيميائي لمواجهة لَدونة SCLC الخطرة.
الاستشهاد: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
الكلمات المفتاحية: سرطان الرئة صغير الخلايا, مقاومة الدواء, لَدونة الخلايا, eIF6, إشارة الإنتغرين FAK