Clear Sky Science · ar
مثبطات الترجمة المعتمِدة على السياق كوسيلة علاجية للسرطان
تحويل مصانع البروتين ضد السرطان
تنجو خلايا السرطان عبر تصنيع كميات كبيرة باستمرار من البروتينات قصيرة العمر "المحرِّكة" التي تحافظ على نموها وانقسامها. تستكشف هذه الدراسة طريقة جديدة لمحاربة السرطان عن طريق تعطيل آلات صناعة البروتين في الخلية — الريبوزومات — بشكل طفيف وفقط عندما تحاول بناء تسلسلات بروتينية محددة، خاصة تلك الموجودة في الجينات المسرطنة التي يصعب استهدافها دوائياً مثل MYC. قد يؤدّي هذا التداخل الانتقائي إلى قتل خلايا الورم مع الإبقاء على معظم إنتاج البروتين الطبيعي دون مساس.
كيف تبني الخلايا البروتينات — وأين يمكن أن يحدث الخلل
تعتمد كل خلية على الريبوزومات، وهي مصانع جزيئية صغيرة تقرأ الرسائل الوراثية (mRNAs) وتركب الأحماض الأمينية لتكوّن البروتينات. تعمل معظم الأدوية الحالية التي تستهدف الريبوزومات، مثل المضادات الحيوية أو أدوية السرطان القديمة، كأدوات خشنة: تقوّف تركيب البروتين على نطاق واسع، ما قد يضر بالخلايا السليمة ويسبب آثار جانبية خطيرة. افترض الباحثون أنه بما أن كل سلسلة بروتينية ناشئة لها تسلسل وخصائص كيميائية فريدة، فقد يكون من الممكن تصميم جزيئات صغيرة تعيق الريبوزوم فقط عندما يكون تسلسل محدد داخل الآلة، متركّين إنتاج البروتينات الأخرى للخلايا إلى حد كبير دون تعطيل.
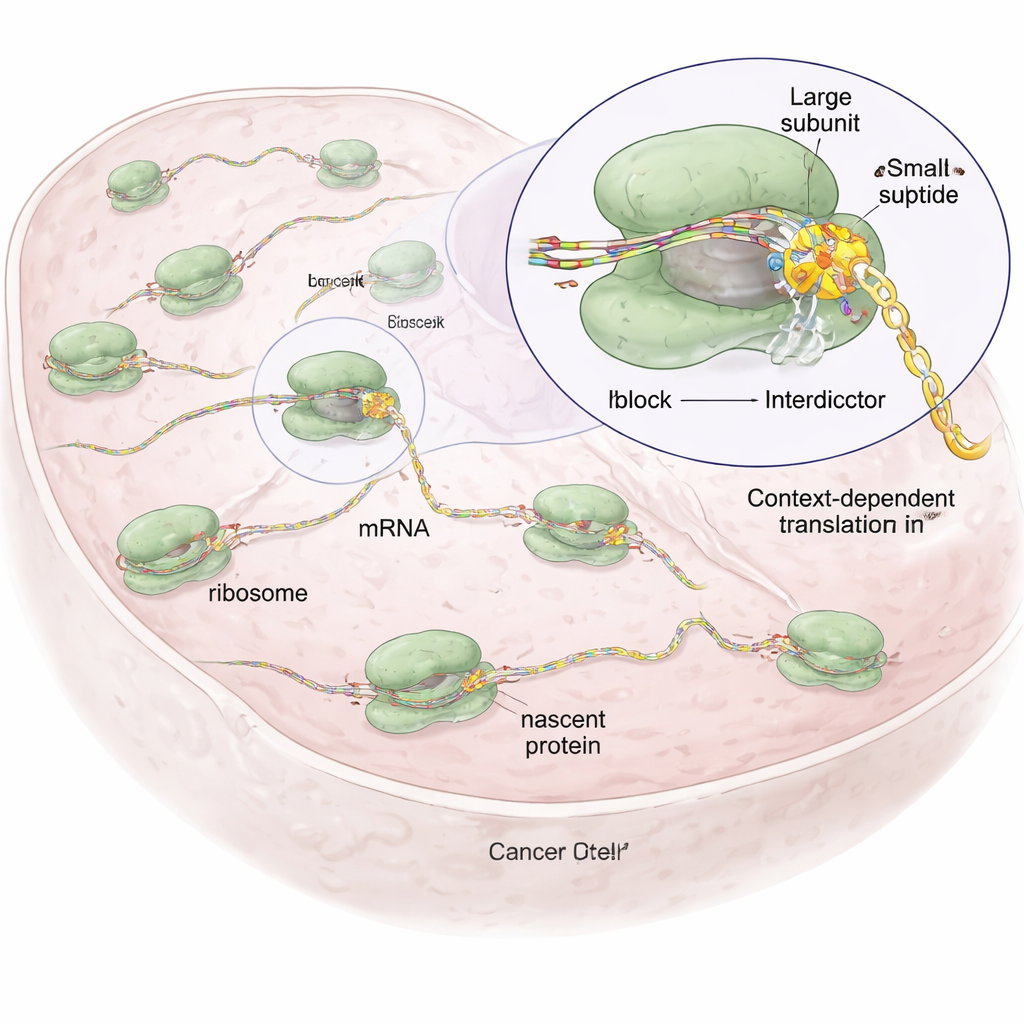
جزيئات مصممة توقف فقط تسلسلات بروتينية معينة
بالبناء على مركب طبيعي يُدعى أنيزوميسين، الذي يرتبط بمركز الريبوزوم الحفازي حيث تتكوّن الروابط الببتيدية، أنشأ الباحثون مجموعة من الجزيئات الاصطناعية أسموها "المثبطات". كلها تشترك في هيكل أساسي يثبّتها داخل الريبوزوم، لكنها تختلف في مجموعات جانبية تشير نحو السلسلة البروتينية النامية. تم ضبط تلك المجموعات الجانبية لتفضيل أنواع محددة من الأحماض الأمينية — على سبيل المثال، أحد المثبطات (IDB‑001) يجذب البقايا سالبة الشحنة، بينما يفضّل آخر (IDB‑002) بقايا صغيرة ودهنيّة (محبة للماء القليل). باستخدام تقنية تُسمى تحديد مواقع الريبوزوم (ribosome profiling)، التي ترسم خريطة أماكن توقف الريبوزومات على mRNAs داخل الخلايا، أظهر الفريق أن كل مركب يسبب توقفات عند أنماط قصيرة مميزة في السلسلة الناشئة، غالباً عند الحمض الأميني قبل الأخير (−1)، مما يبرهن على عمل معتمد على التسلسل بدلاً من إغلاق عشوائي.
مراقبة تفاعل الدواء مع الريبوزوم ذرة بذرة
لمعرفة كيف يعمل هذا الاختيار بتفصيل فيزيائي، جمد المؤلفون ريبوزومات بشرية في حالة الترجمة لتسلسلات ببتيدية مصممة وصوروها بواسطة المجهر الإلكتروني بالتبريد عند دقة قريبة من الذرية. لاحظوا المثبط متوضعاً في الموقع الفعّال للريبوزوم مُكوِّناً تواصلات دقيقة مع الأحماض الأمينية القليلة الأخيرة من السلسلة الناشئة. في بنية واحدة، تُحتضن مجموعة جانبية محبة للدهون من IDB‑002 بواسطة بقايا صغيرة غير ضخمة في الببتيد، مما يفسر سبب عدم تفضيل السلاسل الجانبية الأكبر هناك. وفي بنية أخرى، تتأرجح سلسلة جانبية حمضية من بقايا مشتقة من MYC لتكوّن جسر ملحي مع مجموعة موجبة الشحنة على IDB‑001. كما أن وجود الدواء يدفع قواعد RNA الريبوزومي المجاورة إلى أوضاع جديدة تضيق الموقع الفعّال وتعيق جزئياً دخول tRNA التالي، مما يساعد على تجميد استطالة السلسلة عند تلك التسلسلات المفضلة.
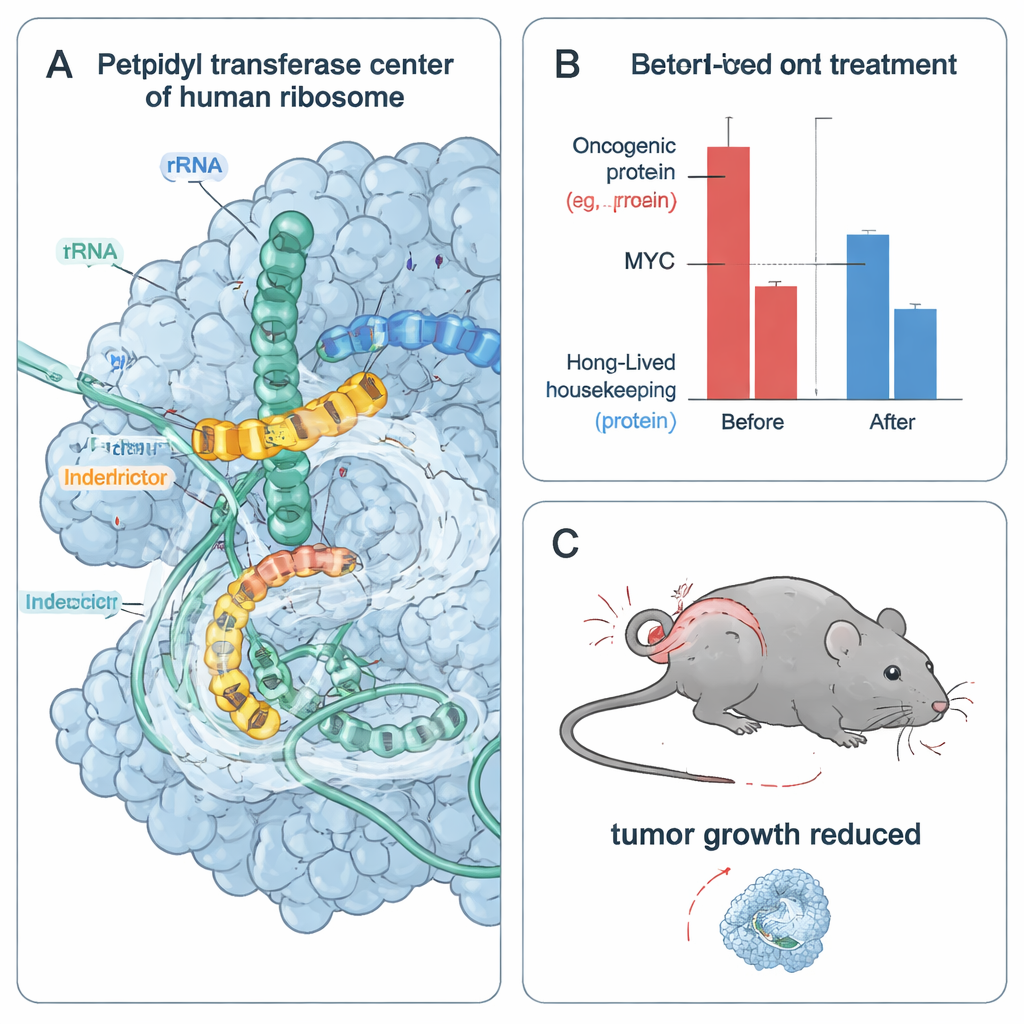
من الريبوزومات المتوقفة إلى خلايا الورم المتعرِّضة للضغط والموت
بما أن خلايا السرطان سريعة الانقسام تعتمد بشدّة على بروتينات مسرطنة قصيرة العمر مثل MYC وCCND1، اختبر الفريق كيف تؤثر المثبطات على بقاء خلايا الورم. في عدة خطوط خلوية معتمدة على MYC، قلّلت IDB‑001 وIDB‑002 من قابلية الخلايا للبقاء عند تراكيز نانومولارية إلى منخفضة ميكرومولارية. كان لتناظر محسن إضافي، IDB‑003، فعالية أقوى وكان مناسباً للإعطاء عن طريق الفم. في الخلايا، استهلكت هذه المركبات بسرعة MYC وغيرها من البروتينات المسرطنة سريعة التحلل بينما تركت بروتينات الصيانة الأطول عمراً مستقرة نسبياً خلال نفس نافذة الزمن. كما أدّت الأدوية إلى تحفيز استجابات إجهاد خلوية مرتبطة بتصادم الريبوزومات، لكن حجب مسارات إشارة الإجهاد تلك لم يلغِ فقدان القابلية للبقاء، مما يشير إلى أن الحرمان المباشر من البروتينات المسرطنة الأساسية هو عامل رئيسي في موت خلايا الورم.
إثبات المفهوم في نموذج صعب لسرطان الثدي
لاختبار ما إذا كانت هذه المقاربة تعمل في الحيوانات، عالج المؤلفون فئراناً حاملة لأورام بشرية من سرطان الثدي الثلاثي السلبي بـ IDB‑003 الممنوح عن طريق الفم. على مدى 28 يوماً، نمت الأورام في الحيوانات المعالجة ببطء أكبر بكثير من نظيرتها في الحيوانات الضابطة، مع تثبيط لنمو الورم يصل إلى 80% عند الجرعات الأعلى ودون تسجيل سميّة شديدة في هذه الدراسة. أظهر تحليل التعبير الجيني في الأورام تثبيطاً قوياً لبرامج جينات أهداف MYC، متوافقاً مع انخفاض نشاط MYC في الجسم الحي. تشير هذه النتائج مجتمعة إلى أن وقف عمل الريبوزومات بشكل انتقائي على تسلسلات بروتينية محددة يمكن أن يضعف الأورام التي تعتمد على عوامل مسرطنة غير مستقرة مع تجنّب سمية واسعة النطاق لمانعات الترجمة التقليدية.
لماذا هذا مهم لعلاجات السرطان المستقبلية
تقدّم هذه الدراسة نوعاً جديداً من الأدوية الجزيئية الصغيرة: دواء لا يعمل عبر الارتباط ببروتين مُنتهٍ، بل يعترضه أثناء تصنيعه وفقط عندما يكون وسم قصير "العنوان" الحاصل على التسلسل موجوداً. وبما أن العديد من البروتينات المعزِّزة للسرطان مرنة، قصيرة العمر، أو تفتقر إلى جيوب واضحة للعقاقير التقليدية، فإن استهداف تصنيعها مباشرة عند الريبوزوم قد يفتح مساراً لعلاج الأورام المدفوعة بجينات حالياً "غير قابلة للعلاج" مثل MYC. كما توحي الدراسة بأنه عبر ضبط كيمياء المثبطات، قد تُصمم أدوية مستقبلية للتركيز على أنماط تسلسل مختلفة وأهداف مرضية متنوعة، موسعة هذه الاستراتيجية إلى ما وراء الأورام إلى حالات أخرى حيث قد يعيد خفض بروتينات محددة الصحة.
الاستشهاد: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
الكلمات المفتاحية: علاج السرطان المستهدف على الريبوزوم, مثبط الترجمة, أورام مدفوعة بواسطة MYC, جزيئات صغيرة معتمِدة على السياق, سرطان الثدي الثلاثي السلبي