Clear Sky Science · ar
هندسة TRIM13 الموضعي تعزز القدرة المضادة للالتهاب لخلايا CAR‑M في علاج تليف الكبد
إعادة برمجة طاقم التنظيف في الكبد
تليف الكبد، عملية تندب قد تؤدي إلى تليف شامل وفشل كبدي، يصيب ملايين الأشخاص ولا تتوفر له حالياً علاجات فعالة كثيرة. تستقصي هذه الدراسة طريقة لاستغلال وإعادة برمجة خلايا المناعة في الكبد بحيث لا تكتفي بإزالة الخلايا المكوّنة للندبة، بل تطمئن أيضاً الالتهاب الضار، مما قد يوفر علاجاً أكثر أماناً وفعالية للأمراض الكبدية المزمنة.
لماذا من الصعب إيقاف تندب الكبد
عندما يتعرض الكبد للإصابة مراراً—بفعل فيروسات أو الكحول أو أمراض تمثيل الغذاء—يحاول الشفاء عبر ترسيب نسيج ندبي. تتحول خلايا متخصصة تُسمى الخلايا النجميّة الكبدية إلى حالة «مفعّلة» وتفرز أليافاً متينة، مثل العمال الذين يصبّون الخرسانة. مع مرور الوقت يشوّه هذا التندّب العضو ويعيق وظيفته. تقع الخلايا المناعية المسماة البالعات (البلعمات) في صلب هذه العملية. في كبد تالف، يمكن أن تتصرف كسيف ذي حدين: ففي وضع تدفعي تُعزز الالتهاب وتفعّل الخلايا النجميّة، أما في وضع آخر أكثر شفاءً فتساعد على تكسير النسيج الندبي وإعادة التوازن.
تحويل الإشارات الضارّة إلى مفيدة
ركز الباحثون على إشارة خطر رئيسية في الكبد التالف: الحمض النووي الميتوكوندري الذي يتسرّب من الخلايا المصابة. تستشعر البالعات هذا الحمض النووي عبر مسار معروف باسم cGAS‑STING، الذي يدفعها إلى حالة مؤيدة للالتهاب ومسببة للتليف. البروتين المسمى TRIM13 يساعد عادةً على كبح نشاط STING عن طريق تأشيرها للتدمير. افترض الفريق أن تعزيز TRIM13 داخل بالعات الكبد قد يعيد توجيهها نحو وضع مهدئ يساهم في إصلاح الأنسجة. وفي الوقت نفسه، أرادوا أن تبحث هذه الخلايا مباشرةً عن الخلايا النجميّة المكوّنة للندبة وتزيلها. لتحقيق ذلك، استخدموا مفهوم المستقبل المناعي المُهجن (CAR) المستعار من علاجات السرطان: مستقبل صناعي يمكّن الخلايا المناعية من تمييز هدف مختار—في هذه الحالة، بروتين يسمى FAP يتوافر بكثرة على الخلايا النجميّة المفعّلة.
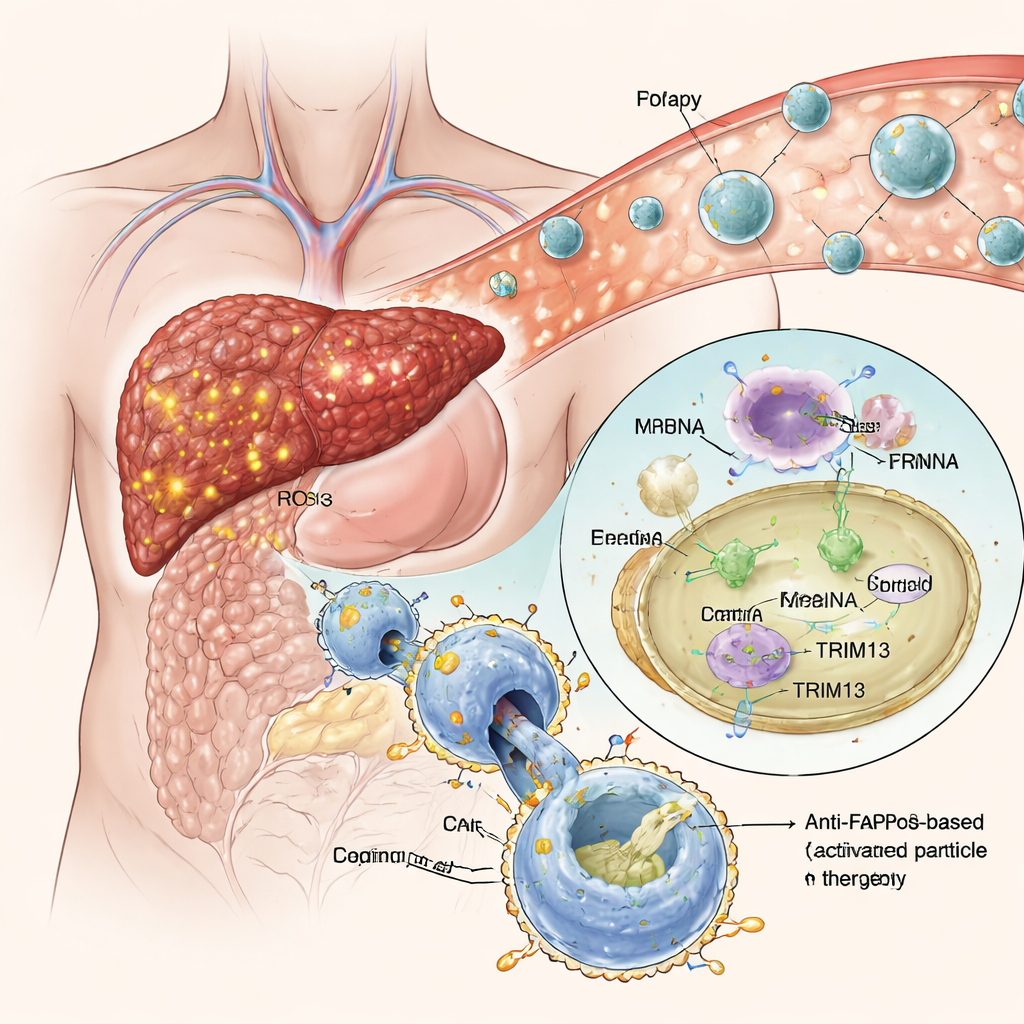
جزيئات نانوية ذكية تستهدف الأنسجة المريضة
بدلاً من هندسة البالعات خارج الجسم، بنى الفريق جزيئات دهنية نانوية «تثار بالالتهام إثر البلع الخلوي»—كرات صغيرة تحمل تعليمات جينية بصيغة الحمض الريبي الرسول (mRNA). تغطى هذه الجسيمات بصورة مخفية من الفسفاتيديل سيرين، إشارة طبيعية «كُلْني» تعرضها الخلايا المحتضرة لجذب البالعات. في البيئة المؤكسدة المرتفعة لأنسجة الكبد المتليف، تُزال المخفّية وتنكشف الإشارة، مما يدفع البالعات القريبة لالتقاط الجزيئات النانوية. حالما تدخل الخلية، يُطلق الـmRNA وتقرأه الخلية، مما يؤدي إلى إنتاج كل من TRIM13 وCAR المضاد لـFAP. في زُرعات الخلايا، نجحت هذه المقاربة في دفع البالعات نحو حالة مضادة للالتهاب مع منحها شهية قوية وانتقائية للخلايا المكوّنة للندبة موجبة FAP، دون المساس بقدرتها الطبيعية على إزالة حطام آخر.
من كبد مريض إلى متجدّد في الفئران
اختبر الفريق بعد ذلك هذه الاستراتيجية في نماذج فأرية لتليف الكبد ناجم إمّا عن مادة كيميائية سامة أو عن نظام غذائي دهنّي ناقص المغذيات. وصلت الجسيمات النانوية المحقونة جهازياً إلى الكبد بكفاءة، ولاسيما في الحيوانات المتليفة، حيث تم امتصاصها أساساً بواسطة البالعات. هناك أظهرت الخلايا المهندَسة نشاطاً منخفضاً لمسار STING وإنتاجاً أقل من الجزيئات الالتهابية، إلى جانب زيادة في قتل الخلايا النجميّة المفعّلة. كشفت تحليلات الأنسجة عن انخفاضات لافتة في الكولاجين وعلامات التندب الأخرى، وبنية مصفوفة خلوية خارجية أدق وأكثر طبيعية، وتحسّن في تحاليل الدم لوظيفة الكبد. أبانت كبد الفئران المعالجة خلايا أكثر انقساماً واستعادت بنية أكثر صحة، مما يوحي بوجود إصلاح حقيقي للعضو وليس مجرد كبح مؤقت للالتهاب.
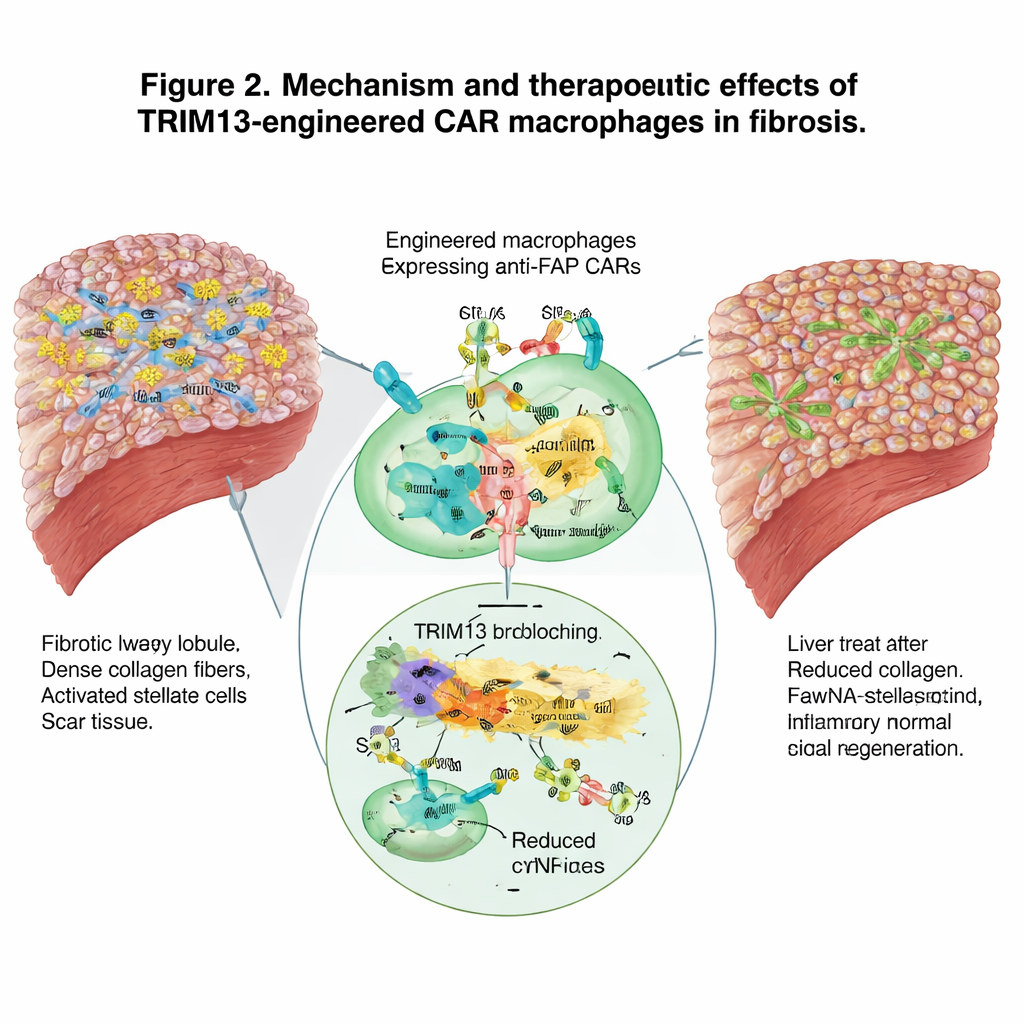
استدعاء باقي جهاز المناعة
إلى جانب الإزالة المباشرة للندبات، أعادت البالعات المهندَسة تشكيل المشهد المناعي الأوسع. تحوّلت من نمط عدواني معزّز للضرر إلى نمط أكثر حلاً وشفاءً وقلّلت الإشارات الالتهابية في الدم. وفي الوقت نفسه، ومن خلال التهام الخلايا المكوّنة للندبة، بدا أنها تعمل كمعلمين للجهاز المناعي التكيفي، جاذبةً العدلات وخلايا التغصّن والخلايا T ومشجعةً استجابة منسّقة ضد النسيج المتليف. أكدت تسلسل الـRNA خلية‑بخلايا للخلايا المناعية الكبدية الانتقال بعيداً عن برامج الجينات المؤيدة للالتهاب ونحو قدرة معززة على الابتلاع وإزالة الخلايا والحطام الضار.
ما الذي قد يعنيه هذا للمرضى
بالنسبة للقارئ العادي، خلاصة الأمر أن هذا العمل يشير إلى طريقة «لإعادة تعليم» خلايا جمع النفايات في الكبد بحيث تفكك النسيج الندبي وتطفيء إشارات الإنذار المزمنة التي تبقي الضرر مستمراً. باستخدام تعليمات mRNA قصيرة العمر مغلّفة في جزيئات نانوية ذكية، تتجنّب هذه المعالجة تغيير الخلايا بشكل دائم وتقتصر فعاليتها على المناطق المريضة، ما قد يقلّل الآثار الجانبية. وبينما لا يزال ثمة حاجة لاختبارات كثيرة قبل أن تُجرب على البشر، تحدّد هذه الاستراتيجية مخططاً واعداً لعلاج تليف الكبد—وربما أمراض تليفية أخرى—عن طريق تحويل جهاز المناعة في الجسم من مُحرّك للتندّب إلى شريك نشط في الشفاء.
الاستشهاد: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
الكلمات المفتاحية: تليف الكبد, علاج بواسطة البالعات (البلعمات), توصيل mRNA بواسطة جزيئات نانوية, المستقبل المناعي المُهجن (CAR), مسار TRIM13‑STING