Clear Sky Science · ar
وسم الأوليغوببتيدات بالنظائر المشعة عبر تبادل انتقائي لنظائر الهيدروجين مع الديوتيريوم والتريتيوم في محاليل مائية
تتبع الأدوية على المستوى الذري
تتضمن الأدوية الحديثة بشكل متزايد جزيئات بيولوجية معقدة مثل الببتيدات والبروتينات الصغيرة. لفهم إلى أين تذهب هذه الأدوية في الجسم وكم تدوم، غالباً ما يستبدل العلماء بعض الذرات العادية بذرات نادرة أو مشعة يمكن تتبعها. تعرض هذه الورقة طريقة لـ"وسم" أدوية الببتيد بهذه الذرات القابلة للتتبع مباشرة في محاليل مائية، وهو أقرب إلى الظروف البيولوجية الحقيقية بكثير من معظم الطرق السابقة.
لماذا تهم هذه التبديلات الذرية الصغيرة
استبدال الهيدروجين العادي بأشكال أثقل مثل الديوتيريوم أو التريتيوم يحول الجزيئات اليومية إلى متتبعات علمية قوية. هذه النسخ الموسومة تتصرف تقريباً بنفس سلوك الدواء الأصلي لكن يمكن تتبعها بأجهزة حساسة تكشف الكتلة أو الإشعاع. بالنسبة للجزيئات العلاجية الصغيرة، بنى الكيميائيون مجموعة أدوات واسعة لصنع مثل هذه المركبات الموسومة. وعلى النقيض من ذلك، فإن طرق وسم الجزيئات البيولوجية الأكبر والهشة — مثل الببتيدات والبروتينات — نادرة، وغالباً ما تكون معقدة وغير مناسبة للبيئات المائية الشبيهة بالدم أو سوائل الخلايا. سعى المؤلفون لسد هذه الفجوة: طريقة بسيطة وانتقائية لإدخال الديوتيريوم أو التريتيوم في لبنات بناء الببتيد مباشرة في محاليل عازلة مائية.
استراتيجية وسم خطوة واحدة في الماء
ركز الفريق على نوع من التفاعل يُدعى تبادل نظائر الهيدروجين، حيث يتم استبدال ذرة هيدروجين على جزيء بنظير أثقل من غاز مثل الديوتيريوم (D2) أو التريتيوم (T2). بنوا محفزاً داخلياً قائمًا على معدن الإيريديوم ومساعد فسفيني مُختار بعناية. عند خلطه في محلول عازل ضعيف القلوية وتسخينه، يفعل هذا النظام روابط كربون–هيدروجين محددة في الأحماض الأمينية والببتيدات الصغيرة ويستبدل تلك الهيدروجينات بالديوتيريوم أو التريتيوم من الغاز. والأهم أن ذلك يُنجز في خطوة واحدة، في وسط غني بالماء، وبكميات ضئيلة جداً من المعدن — شروطٍ ألطف على الأدوية الببتيدية الحساسة وعلى إجراءات المختبر العملية. 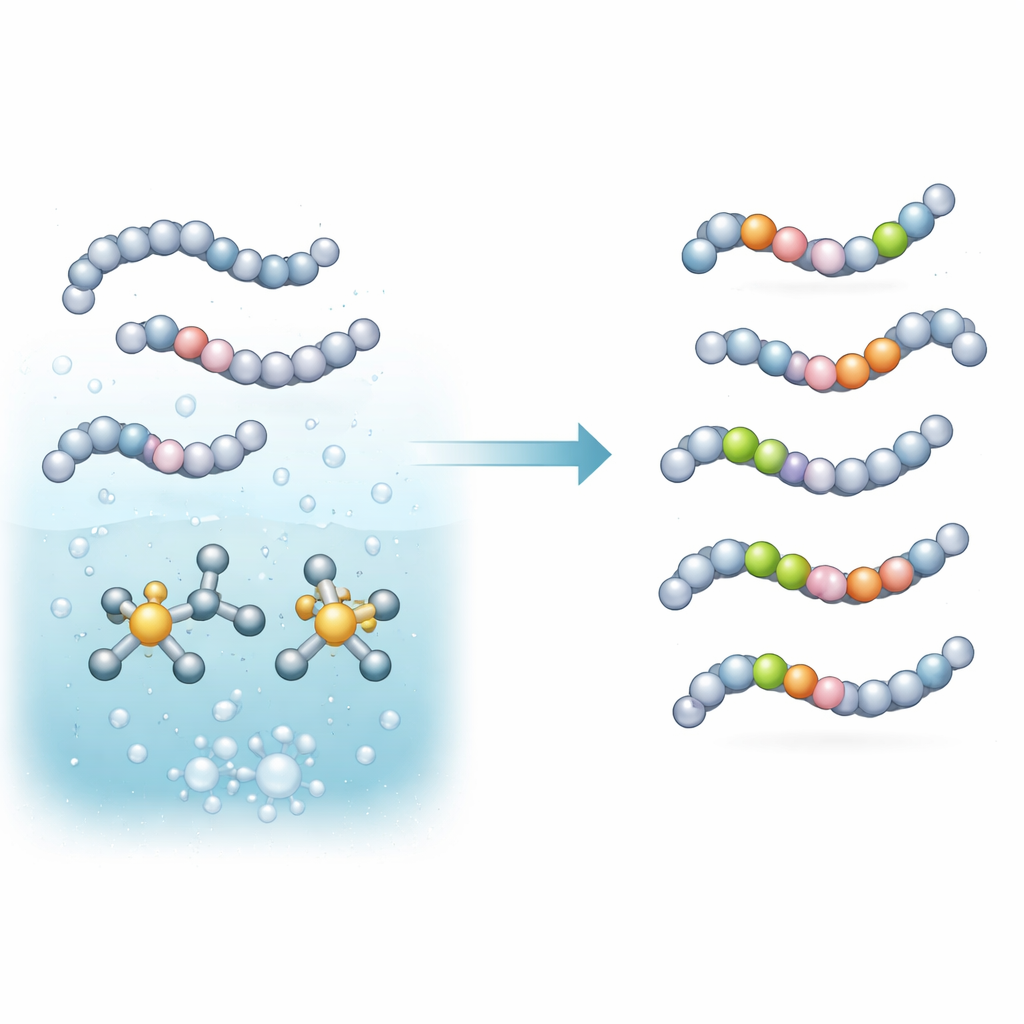
اختيار المواضع الصحيحة على الببتيدات
ليست كل ذرة هيدروجين في الببتيد مفيدة بنفس الدرجة كوسم. بعضٌ منها يُفقد بسهولة أثناء الأيض، مما سيمحو الوسم المشع. استكشف المؤلفون بعناية الأماكن التي يفضل محفزهم العمل عندها. اكتشفوا أن الأحماض الأمينية غير المحمية مثل الليسين والأرجينين مناسبة بشكل خاص. في الليسين، تُعامل الطريقة بشكل انتقائي كربوناً في السلسلة الجانبية (الموقع المسمى جاما)، وهو موقع يعتبر "غير منشط" وأكثر احتمالاً للبقاء مستقراً في الجسم. يظهر الأرجينين سلوكاً مشابهاً في مواقع مجاورة على سلسلته الجانبية. من خلال اختبار سلسلة من الجزيئات ذات الصلة، بما في ذلك سلاسل قصيرة تحتوي على مجموعتي أمين، وجد الفريق أن وجود موقعين نيتروجين موضوعين بشكل مناسب يساعدان محفز المعدن على التمسك بالمركب والوصول إلى رابطة الكربون–هيدروجين المستهدفة.
نظرة إلى آلية عمل المحفز
لفهم سبب نشوء هذه الانتقائية، جمع الباحثون بين تجارب مخبرية ومحاكاة حاسوبية مفصلة باستخدام نظرية الدالات الكثافية. ترسم هذه الحسابات خريطة للمشهد الطاقي أثناء تشكل مركب الإيريديوم من مادة بادئة ديمرية، ارتباطه بالماء، ثم بالحمض الأميني، وفي النهاية إدخاله في رابطة كربون–هيدروجين محددة. تُظهر النماذج أن تكسير ديمر الإيريديوم الأصلي ممكن طاقياً في الماء لنوع واحد من المواد الأولية لكن ليس لآخر مرتبط ارتباطاً وثيقاً، مما يفسر لماذا تكون بعض المركبات الأولية فقط فعالة. تكشف النماذج أيضاً أن الركيزة نفسها تساعد في تثبيت مركز المعدن النشط ومنعه من التكتل إلى جزيئات غير نشطة. المسار الأكثر ملاءمة ينطوي على ارتباط الحمض الأميني عبر ذرتي نيتروجين، مكونًا قبضة "مشبكية" تضع رابطة كربون–هيدروجين مفردة في وضع مناسب للتبادل مع الديوتيريوم أو التريتيوم.
من لبنات بناء بسيطة إلى أدوية ببتيدية حقيقية
مع فهم الآلية، وسع الفريق تطبيق الطريقة من الأحماض الأمينية المفردة إلى ببتيدات قصيرة تحتوي حتى سبعة بقايا ثم إلى سلاسل علاجية أقرب للواقع تضم ما يصل إلى 13 حمضاً أمينياً. في جميع الحالات، وقع الوسم على السلاسل الجانبية لليسين أو الأرجينين في نهاية الببتيد، وبقيت الببتيدات سليمة إلى حد كبير تحت ظروف التفاعل. بالنسبة للتريتيوم، أمثلوا التفاعل عند ضغوط غاز منخفضة لتحقيق نشاط نوعي مرتفع بأمان، ما يعني أن جزءاً كبيراً من الجزيئات يحمل على الأقل ذرة تريتيوم واحدة. أنتجت هذه الببتيدات الموسومة بالتريتيوم في وعاء واحد وهي جاهزة للاستخدام كمتتبعات في دراسات مخبرية وربما داخل الكائن الحي.
ماذا يعني هذا لمستقبل الأدوية
تُظهر هذه الدراسة أنه من الممكن ربط الديوتيريوم أو التريتيوم انتقائياً بالأدوية الببتيدية الواقعية في خطوة مائية بسيطة مع استهداف مواقع مقاومة أيضياً في الأحماض الأمينية الرئيسية. بالنسبة لمطوري الأدوية، يعني ذلك سهولة أكبر في الحصول على نسخ متتبعة موسومة بدقة من العلاجات الببتيدية، وهي ضرورية لقياس الامتصاص والتوزيع والأيض. وبالإضافة إلى إنتاج المتتبعات، قد تلهم البصائر الآلية حول تفاعل محفز الإيريديوم مع الأحماض الأمينية طرقاً جديدة لضبط أين وكيف تُعدَّل الجزيئات البيولوجية المعقدة، فاتحةً الباب إلى تحكم كيميائي أكثر دقة على الأدوية البيولوجية المستقبلية.
الاستشهاد: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
الكلمات المفتاحية: الببتيدات الموسومة إشعاعياً, تبادل نظائر الهيدروجين, وسم بالديوتيريوم والتريتيوم, علاجات ببتيدية, تحفيز بالإيريديوم