Clear Sky Science · ar
تسخير مفاعل أمعاء فأر خالٍ من الجراثيم للتطور الموجَّه للبروبيوتيك لمكافحة مرض الكبد الدهني غير الكحولي
لماذا تهم هذه القصة المعوية كبدك
يؤثر مرض الكبد الدهني غير الكحولي (NAFLD) الآن على مئات الملايين من الأشخاص ويرتبط ارتباطًا وثيقًا بالنظام الغذائي وصحة الأمعاء. تستكشف هذه الدراسة فكرة غير مألوفة: استخدام الأمعاء نفسها كنوع من المصنع الحي لـ«تدريب» البكتيريا المفيدة حتى تصبح أدوية أفضل. من خلال السماح للبروبيوتيك بالتطور داخل فئران خالية من الجراثيم وتغذيتها بنظام عالي الدهون، شكّل الباحثون سلالة بكتيرية تتعامل بكفاءة أكبر مع أحماض الصفراء—الجزيئات الشبيهة بالمنظفات التي تربط ما نأكله بكيفية تخزين الكبد للدهون. تشير النتائج إلى طريقة جديدة لصياغة بروبيوتيك من الجيل التالي تكون مُنَسَّقة طبيعيًا مع أجسامنا بدلاً من أن تُصمَّم فقط في أنابيب المختبر.
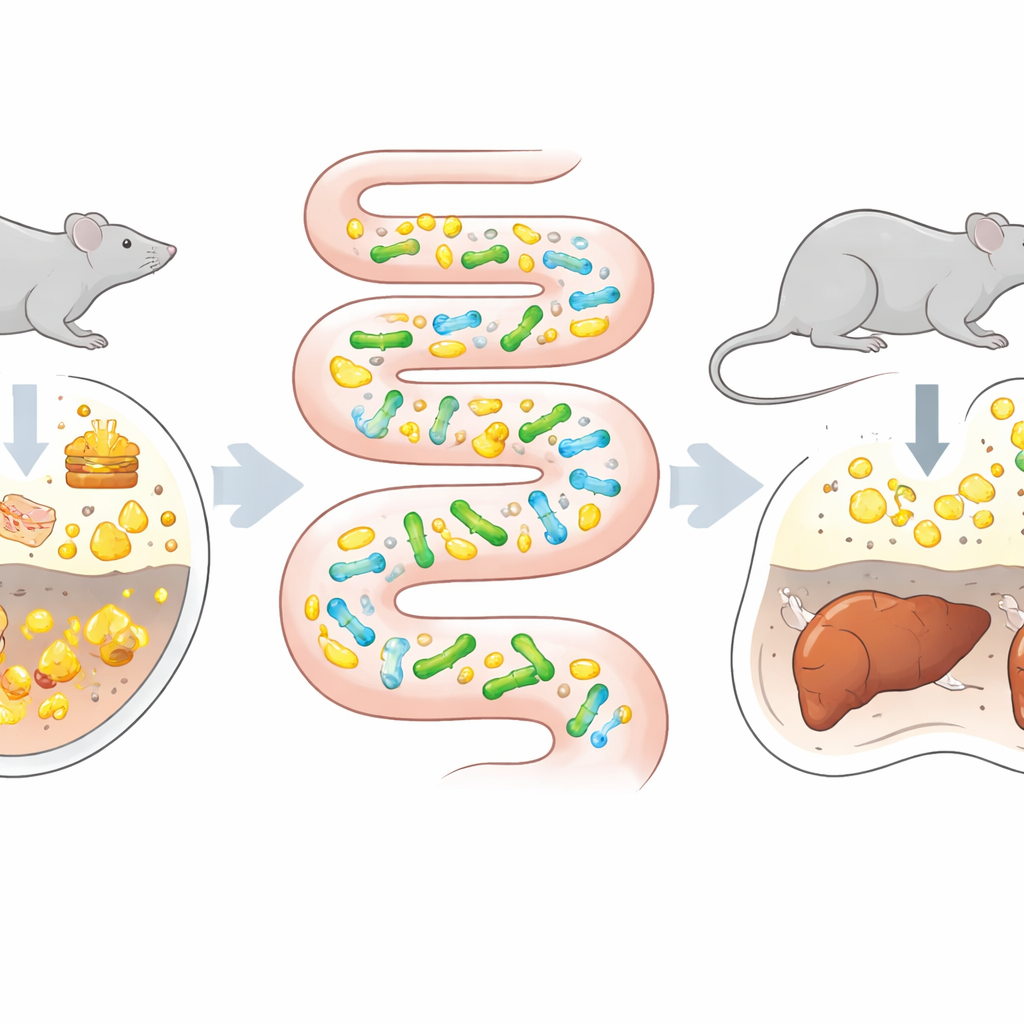
تحويل الأمعاء إلى غرفة تطور
التطور الموجَّه التقليدي—تسريع الطفرات في الميكروبات واختيار الأداء الأفضل—يحدث عادة في قوارير المختبر. هذا ينجح مع الإنزيمات أو الميكروبات الصناعية لكنه غالبًا ما يفشل مع البروبيوتيك، التي يجب أن تتعامل مع الكيمياء المعقدة وإشارات الجهاز المناعي والقوى الفيزيائية في الأمعاء. تساءل المؤلفون: ماذا لو استُخدمت الأمعاء نفسها، بكل ضغوطها الطبيعية، كبيئة اختيارية؟ اختاروا نوعًا بروبيوتيكيًا، Bifidobacterium animalis subsp. lactis، الذي يمتلك بالفعل بعض القدرة على تكسير أحماض الصفراء. تم استعمار فئران خالية من الجراثيم، التي لا تحمل ميكروبات أخرى، بهذه السلالة ثم أُطعِمت بنظام متزايد الدهون والكوليسترول خطوة بخطوة، المعروف بزيادة مستويات أحماض الصفراء في الأمعاء. بالتوازي، دفعوا نفس السلالة للتكيف في وسط مخبري قياسي يحتوي أحماض صفراء، مما أتاح مقارنة وجهًا لوجه بين التطور في المختبر مقابل التطور داخل الكائن الحي.
بروبيوتيك مدرَّب في الأمعاء يتفوق على نظيره المخبري
بعد التمرير المتكرر في القوارير، لم تُظهر البكتيريا المتطورة في المختبر أي تحسّن ذي معنى في نشاط معالجة أحماض الصفراء. على النقيض الواضح، أظهرت العزلات المأخوذة من أمعاء الفئران المُطعَّمة عاليًا بالدهون تباينًا واسعًا في الأداء؛ نحو ربعها امتلك قدرة أقوى بوضوح على تكسير أحماض الصفراء. المتغير البارز، المسمى W5S9، أيض أحماض الصفراء بشكل أفضل بنسبة 77 بالمئة مقارنة بالسلالة الأم. هذه التنوعات، ووجود منتصرين وخاسرين، أبرزت كيف أن بيئة مضيف الأمعاء تطبّق ضغوطًا غنية ومتعددة الأوجه لا يمكن للوسائط المخبرية البسيطة تقليدها. كما أكدت أن الأمعاء يمكن أن تعمل كمَفاعل حيوي قوي، يولّد ويختبر باستمرار المتغيرات الجينية في ظروف تشبه الحياة الواقعية.
التعمق في الطفرات المهمة
لفهم ما تغير داخل W5S9، قام الفريق بتسلسل جينومها وقياس أيّ الجينات كانت أكثر أو أقل نشاطًا مقارنةً بالسلالة الأصلية. من بين مئات الاختلافات الصغيرة في الحمض النووي، برزت اثنتان. الأولى كانت موجودة مباشرة أمام جين يسمى cbh، الذي يُنتج إنزيمًا يقطع أملاح الصفراء؛ هذا التغيير عمل كمفتاح تشغيل أقوى، معززًا إنتاج الإنزيم تحت ضغط الأحماض الصفراوية. الطفرة الثانية غيرت بنية ونشاط بروتين ناقل (MDR) يضخ أحماض الصفراء المعالجة خارج الخلية. أظهرت الاختبارات المخبرية أن هذه التعديلات جعلت البروبيوتيك أفضل في كل من تقطيع أحماض الصفراء المترافقة وتصدير المنتجات الناتجة، مما حسّن بقاؤه في ظروف غنية بالأحماض الصفراوية القاسية. بعبارة أخرى، ضبط التطور داخل الأمعاء كلًا من «المقصات» و«باب الخروج» في مسار أحماض الصفراء.
حماية أكباد دهنية في جسم متوتر غذائيًا
الاختبار الحاسم كان ما إذا كانت هذه السلالة المدربة في الأمعاء يمكنها فعلاً حماية الحيوان من تلف الكبد. استخدم الباحثون نموذج فأر لـ NAFLD، حيث يتسبب النظام الغذائي عالي الدهون طويل الأمد في زيادة الوزن وتراكم الدهون في الكبد والالتهاب. قُسِّمت الفئران إلى أربع مجموعات: نظام غذائي عادي، نظام عالي الدهون وحده، نظام عالي الدهون مع البروبيوتيك الأصلي، ونظام عالي الدهون مع السلالة المتكيفة W5S9. أظهرت كلتا مجموعتي البروبيوتيك تحسناً مقارنةً بمجموعة العالي الدهون، لكن W5S9 تفوقت باستمرار. فقد اكتسبت هذه الفئران وزناً أقل، كان لديها ملفات كوليسترول صحية أكثر، أظهرت مؤشرات أقل لإصابة الكبد والالتهاب، وكان هناك قطرات دهنية أقل بوضوح في نسيج الكبد. كشف التحليل الكيميائي المفصّل للبراز أن W5S9 قلّلت بقوة أكبر من أحماض الصفراء المرتبطة بالمرض ودفعت تجمع أحماض الصفراء نحو توازن صحي أكثر، دون إعادة تشكيل دراماتيكية للمجتمع الميكروبي الكلي في الأمعاء.
ماذا يعني هذا لأدوية البروبيوتيك المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن الباحثين لم يكتفوا بإيجاد بروبيوتيك «جيد»—بل استخدموا الجسم نفسه لنحت واحد أفضل. بمنح الانتقاء الطبيعي حرية العمل داخل فئران خالية من الجراثيم في بيئة مصممة بعناية عالية الدهون وغنية بالأحماض الصفراوية، أنتجوا سلالة تتعامل بكفاءة أكبر مع أحماض الصفراء وبالتالي تحمي الكبد بشكل أفضل من الضرر الناجم عن النظام الغذائي. وبما أنه لم تُضاف حمض نووي غريب، تظل هذه الميكروبات المتطورة غير معدلّة وراثيًا (غير GMO)، مما قد يسهّل القبول التنظيمي والعام. الدلالة الأوسع هي أن استراتيجيات التطور الموجهة بواسطة المضيف يمكن تكييفها لحالات أخرى، من أمراض الأمعاء الالتهابية إلى الاضطرابات الأيضية وحتى العصبية، فاتحة الباب أمام علاجات ميكروبية حية مخصصة وُفِّقت وظيفيًا.
الاستشهاد: Han, Z., Sun, Z., Liu, X. et al. Harnessing a germ‑free mouse gut bioreactor for directed evolution of probiotics to combat non-alcoholic fatty liver disease. Nat Commun 17, 3133 (2026). https://doi.org/10.1038/s41467-026-69823-0
الكلمات المفتاحية: بروبيوتيك, ميكروبيوم الأمعاء, أحماض الصفراء, مرض الكبد الدهني, التطور الموجَّه