Clear Sky Science · ar
خلايا بيتا المولِّدة للكوكيستوكين تحرِّك تطور سرطان البنكرياس الغدي المرتبط بالسمنة
عندما يتواصل الوزن الزائد مع البنكرياس
من المعروف أن السمنة تزيد من خطر الإصابة بسرطان البنكرياس، أحد أخطر السرطانات، لكن «الحوار» البيولوجي الذي يربط بين الدهون الزائدة والاورام كان غامضًا. تكشف هذه الدراسة عن مرسال غير متوقع: هرمون هضمي يُسمى الكوكيستوكينين، أو CCK، يُنتَج داخل خلايا صنع الإنسولين في البنكرياس. من خلال تتبع كيف تتغير هذه الخلايا تحت الضغط الأيضي، يوضح المؤلفون كيف أن هرمونًا مقصودًا لمساعدة الجسم يمكنه بدلًا من ذلك أن يغذي السرطان، ويقترحون طرقًا جديدة لاعتراض المرض قبل أن يستشري.
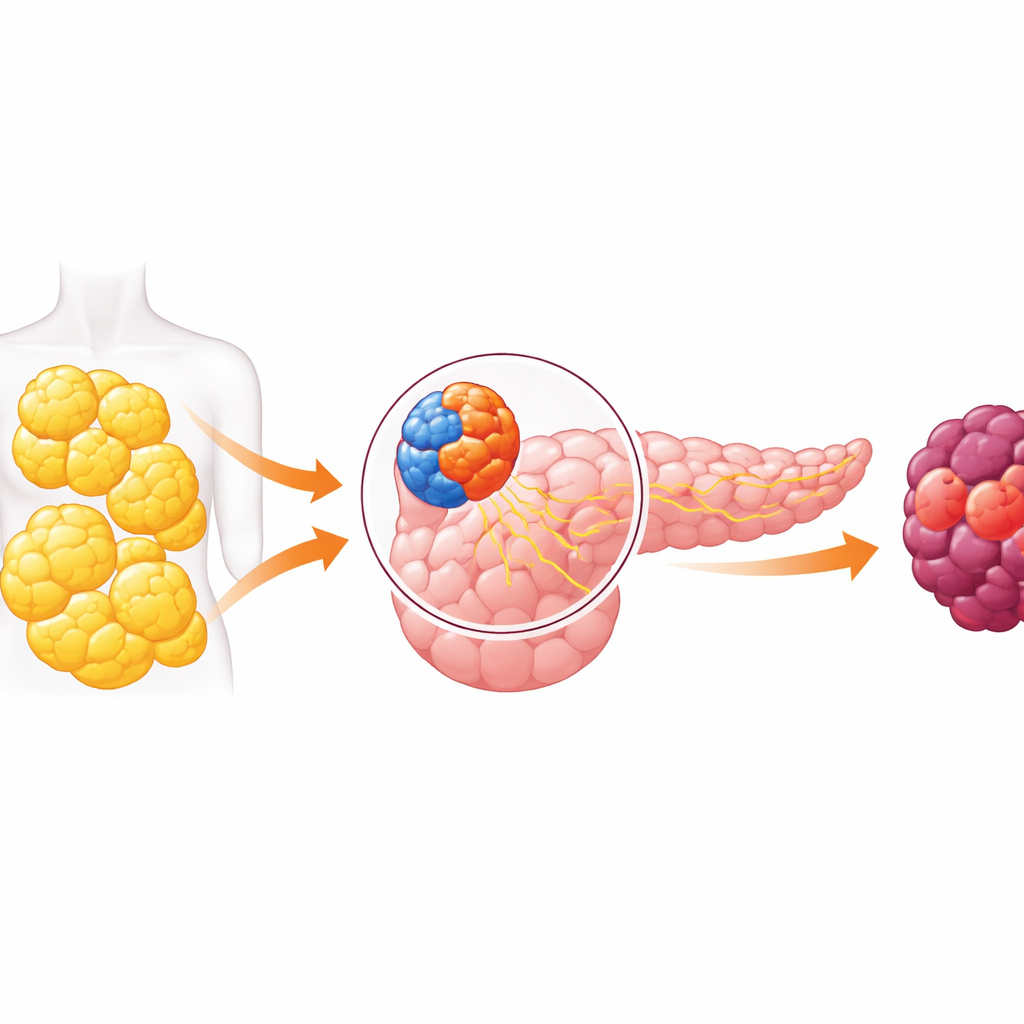
عضو ذو وجهين وحوار خطِر
يؤدي البنكرياس وظيفتين رئيسيتين. فجزءه الصماوي يحتوي على جزر صغيرة من الخلايا التي تفرز هرمونات مثل الإنسولين للتحكم في سكر الدم. أما الجزء الخارجِي فينتج عصائر هضمية ويشمل الخلايا التي غالبًا ما تنشأ منها سرطانات البنكرياس. لسنوات افترض الباحثون أن هذه المقاطع تعمل بمعزل إلى حد كبير. أحدثت الأعمال الحديثة انقلابًا في هذه الفكرة، مبيِّنة أن الإشارات القادمة من الخلايا المفرزة للهرمونات يمكن أن تؤثر في الخلايا الهضمية المجاورة. تغوص هذه الورقة في ذلك التبادل وتجد أن السمنة يمكن أن تدفع الجانب الهضمي من البنكرياس نحو السرطان.
إجهاد في خلايا الهرمون يشعل إشارة جديدة
في حالة السمنة، تتعرض خلايا بيتا المنتجة للإنسولين لضغط مستمر لتلبية الطلب المتزايد على الإنسولين. باستخدام تسلسل الحمض النووي الريبي خلية بخلية وأدوات حسابية متقدمة، تتبع الباحثون خلايا بيتا الفردية بينما تحولت الفئران من نحيلة إلى زائدة الوزن ثم إلى سمنة شديدة. وجدوا أن مجموعة من خلايا بيتا غير الناضجة توسعت وفقدت تدريجيًا هويتها المتخصصة في إنتاج الإنسولين. مع تزايد إجهاد هذه الخلايا، ارتفعت علامات اضطراب طي البروتينات والضرر الخلوي بينما انخفض إنتاج الإنسولين. وبنفس الوقت، بدأت هذه الخلايا تُنتج مستويات عالية من CCK، وهو هرمون مرتبط عادة بالأمعاء ويمكن أن يحفز خلايا الهضم على النمو والتغيير.
من هرمون مساعد إلى وقود للسرطان
لاختبار ما إذا كان هذا الـ CCK المنتج حديثًا مجرد ناتج ثانوي للإجهاد أم محركًا نشطًا للمرض، مهندَس الفريق فئرانًا تجعل خلايا بيتا تنتج CCK إضافيًا حتى بدون السمنة. طورت هذه الحيوانات مراحل ما قبل السرطان في البنكرياس وأورامًا غازية بدرجة مماثلة للفئران السمنة، على الرغم من أنها كانت ذات وزن طبيعي وسكر دم طبيعي. بالمقابل، عندما أزيل الـ CCK بشكل محدد من بنكرياس الفئران السمنة، انخفض عبء الورم بشكل حاد، رغم أن الحيوانات بقيت سمينة وكانت مستويات الإنسولين مرتفعة. عبر نماذج فئران متعددة، تقاربت مستويات CCK في البنكرياس مع كمية الورم، بينما اتجهت مستويات الإنسولين غالبًا في الاتجاه المعاكس. هذا أشار إلى أن CCK — وليس الإنسولين — هو الهرمون المسيطر الذي يربط السمنة بسرطان البنكرياس في هذه النماذج.
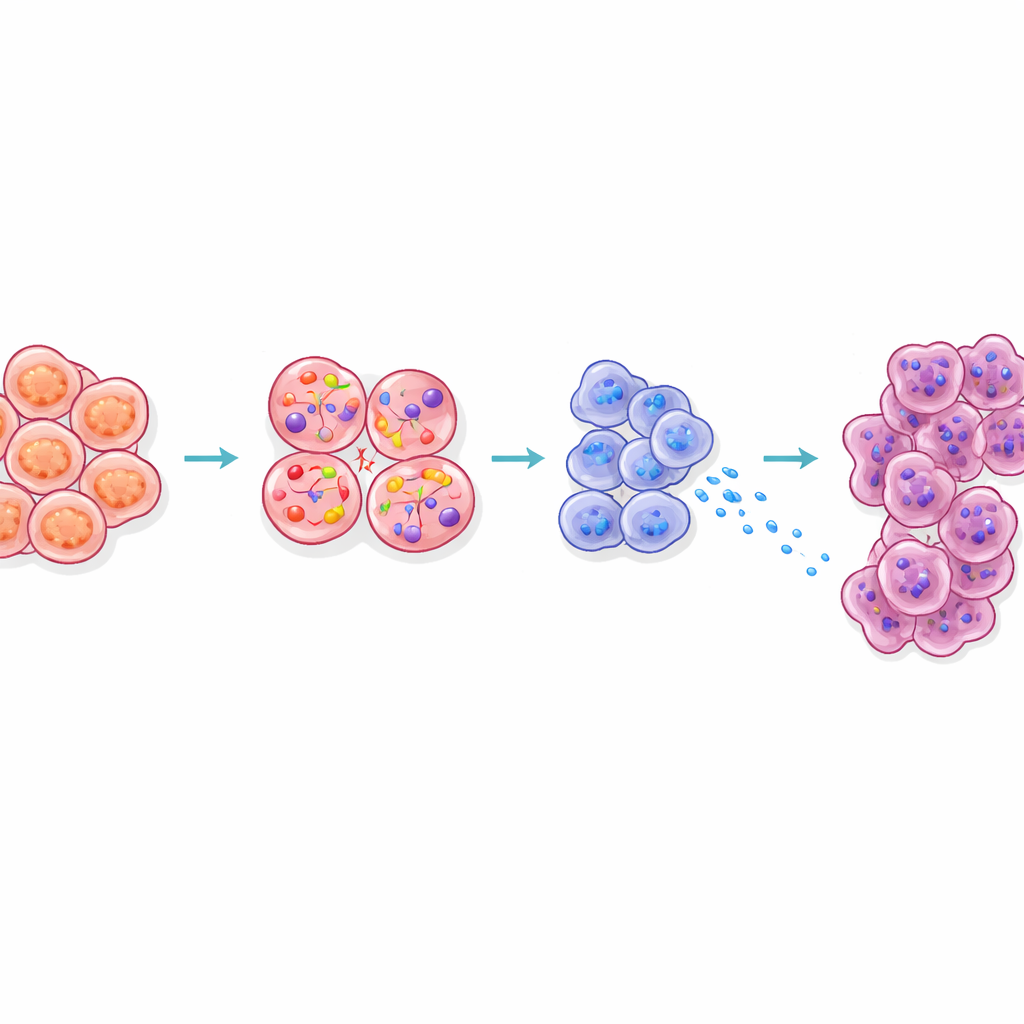
كيف تصل الإشارة وتهيئ الخلايا المجاورة
فحصت الدراسة أيضًا كيف يعيد CCK القادم من خلايا بيتا تشكيل النسيج المحيط. تجلس خلايا الأكيَار، التي عادة ما تفرز إنزيمات هضمية، بجانب الجزر في البنكرياس مباشرة. في الفئران السمنة، أظهرت خلايا الأكيَار المجاورة للجزر علامة إجهاد، وأنتجت مزيدًا من الإنزيمات الهضمية وبروتينات تُسمى Reg، وانتقلت إلى حالات معروفة بأنها أكثر قابلية للتحول إلى سرطان. قلل حجب إشارة CCK في الفئران السمنة من إشارات Reg هذه. كما كشفت التصوير ثلاثي الأبعاد أن الآفات ما قبل السرطانية المبكرة كانت تميل إلى الظهور بقرب غير معتاد من الجزر في الحيوانات السمنة. تقترح هذه النتائج معًا أن CCK المتسرب من خلايا بيتا المضغوطة يخلق «منطقة ساخنة» حول الجزر حيث تُهيأ خلايا الهضم لتصبح أورامًا.
أنماط مشتركة مع داء السكري البشري ومفتاح تحويلي
بمقارنة بيانات الفئران مع نسيج البنكرياس البشري لأشخاص مصابين أو غير مصابين بداء السكري من النمط 2، وجد المؤلفون تشابهاً لافتًا: خرائط خلايا بيتا من المتبرعين المصابين بالسكري تطابقت مع حالات الإجهاد والنضج الأقل نفسها التي رُصدت في الفئران السمنة. ثم استخدموا تحليلًا تنظيميًا للسؤال عما يشغل تشغيل CCK في خلايا بيتا وحددوا مسارًا مستجيبًا للإجهاد يتمركز حول البروتين cJun. عندما عرقلوا المسار العلوي JNK–cJun في الفئران السمنة أو في خلايا شبيهة بخلايا بيتا في طبقٍ زجاجي، انخفضت مستويات CCK، وظهر أن cJun يرتبط بالقرب من منطقة تنظيمية في جين CCK. هذا يوحي بأن الإجهاد المزمن ينشط JNK–cJun، والذي بدوره يحوّل خلايا بيتا إلى نمط إنتاج CCK.
ما معنى ذلك للأشخاص المعرضين للخطر
للقارئ العام، الرسالة المركزية هي أنه، تحت وطأة السمنة والداء السكري، لا تكتفي خلايا الإنسولين في البنكرياس بالتراجع—بل تتكيف بطريقة تشجّع بدون قصد الخلايا المجاورة على تشكيل السرطان. وتفعل ذلك عن طريق تشغيل CCK، هرمون يعمل كإشارة نمو وإجهاد لخلايا الهضم المجاورة، فَيُسهِم في خلق أرضية خصبة للأورام. ونظرًا إلى أن CCK القادم من البنكرياس ليس ضروريًا للحفاظ على ضبط سكر الدم، فقد يكون استهداف هذا المصدر الهرموني المحدد أو مفتاحه المنشط بالإجهاد طريقة ممكنة لتقليل خطر سرطان البنكرياس لدى الأشخاص المصابين بالسمنة أو بداء السكري من النمط 2 من دون المساس بتوازن الهرمونات العام. تعيد هذه الدراسة تأطير سرطان البنكرياس كمرض ناجم عن تواصل مضلل بين جانبي العضو وتبرز مسارات جديدة للوقاية المبكرة.
الاستشهاد: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
الكلمات المفتاحية: سرطان البنكرياس, السمنة, خلايا بيتا, الكوكيستوكين, داء السكري من النمط 2