Clear Sky Science · ar
تشكّل مجال PIN المكوَّن من SMG5-SMG6 أمرٌ أساسي لآلية NMD
كيف تحمي الخلايا نفسها من الرسائل المعيوبة
تقرأ خلايانا باستمرار الرسائل الجينية (mRNAs) لصنع البروتينات. لكن هذه الرسائل أحيانًا تحتوي على إشارات توقف مبكرة تؤدي إلى إنتاج بروتينات مختصرة قد تكون ضارة. يُطلق على العملية التي تدمر مثل هذه الرسائل المعيوبة اسم إزالة mRNA الناجمة عن التوقف غير المنطقي (nonsense‑mediated mRNA decay، أو NMD). تكشف هذه الورقة كيف يتعاون بروتينان رئيسيان، SMG5 وSMG6، فعليًا لقطع الرسائل المعيبة، موضحة لغزًا طويل الأمد في كيفية عمل مراقبة الجودة الخلوية.
اكتشاف الشراكة الخفية
لسنوات، كان العلماء يعلمون أن SMG6 يمكنه قطع الـRNA مباشرة، بينما كان يُعتقد أن SMG5 «ميت تحفيزيًا» ويعمل أساسًا كمساعد أو إطار. ومع ذلك، أظهرت التجارب في الخلايا شيئًا محيرًا: لم تتمكن SMG6 من العمل بشكل صحيح بدون SMG5، وتلاشت آلية NMD إذا غاب أي منهما. استخدم المؤلفون تنبؤات هيكلية حديثة (AlphaFold)، وتجارب كيميائية حيوية ببروتينات نقية، واختبارات جينية في خطوط خلوية بشرية لحل هذا التناقض. تنبأت نماذجهم بأن مناطق الذيل في SMG5 وSMG6، المسماة مجالات PIN، تتلاصقان لتكوّن بنية مشتركة. اقترح أن هذه الوحدة المركبة — التي سميت «cPIN» — هي الآلة الحقيقية للقطع في NMD. 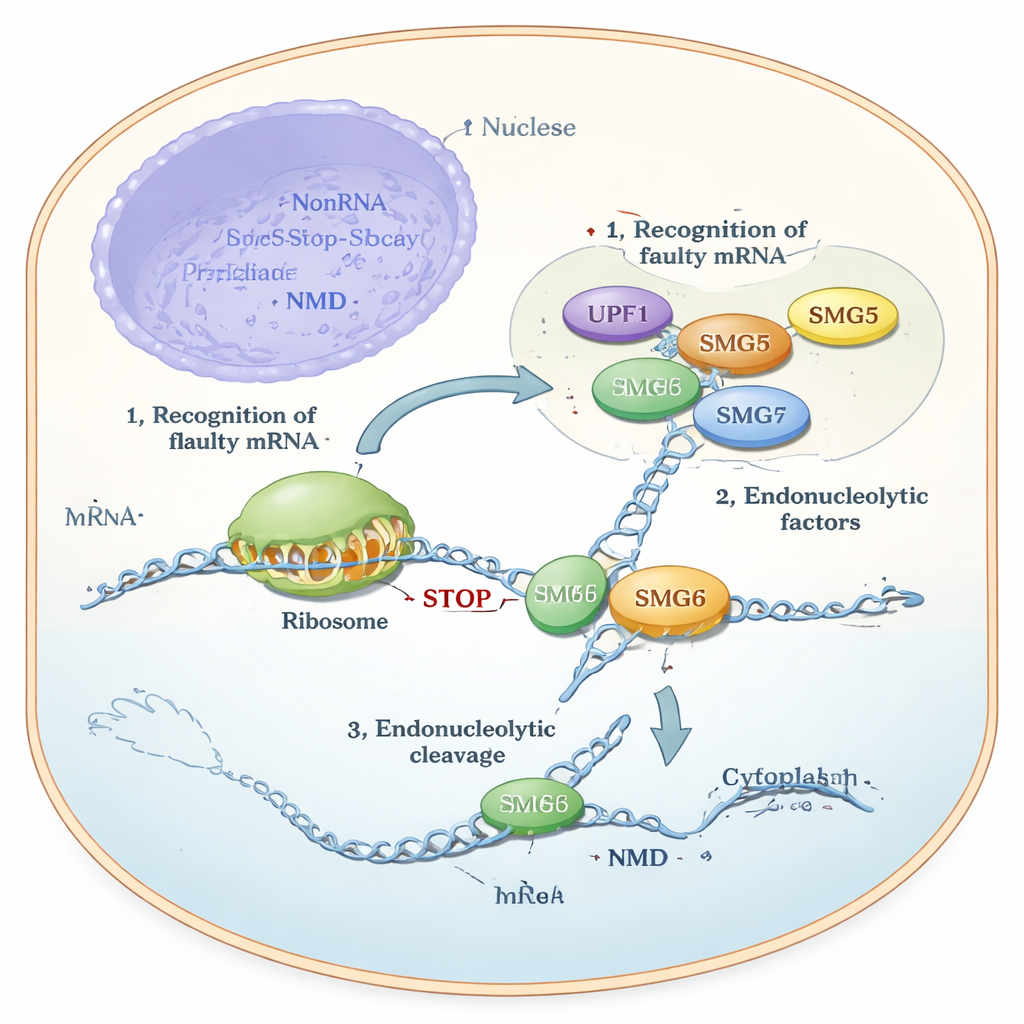
إعادة بناء المقص الجزيئي في أنبوب اختبار
لاختبار التنبؤ، أنتج الفريق شظايا من SMG5 وSMG6 البشريين في بكتيريا ونقّاها. لوحدها، أظهرت SMG6 قدرة ضعيفة فقط على قطع ركيزة RNA مصممة، أما SMG5 وحده فلم يُظهر تقريبًا أي قدرة. لكن عند خلط الشظيتين، ارتفعت قدرة القطع بشكل حاد، حتى في ظروف كانت فيها احتمالات وجود إنزيمات ملوِّثة ضئيلة. ظهر التأثير نفسه على جزيئات اختبار مبنية على RNA خطي ودائري، مما يشير إلى أن التحسين في القدرة على القطع جاء فعليًا من زوج SMG5–SMG6. أظهر التصليب الكيميائي وطيف الكتلة أن البروتينين يقتربان من بعضهما البعض، داعمين فكرة وجود شراكة مباشرة ولو عابرة.
إكمال حافة القطع
أشارت النماذج الهيكلية إلى كيفية تعزيز SMG5 لعمل SMG6 بدقة. يساهم SMG6 بأربعة أحماض أمينية حمضية تحتفظ بأيونات معدنية في قلب موقع القطع، كما هو معتاد لهذه العائلة من الإنزيمات. والمفاجئ أن النماذج وضعت حمضًا أمينيًا حمضيًا إضافيًا من SMG5 بجوارها مباشرة، موسعةً بذلك الجيب التحفيزي فعليًا. وتنبأ بوجود بقايا مشحونة موجبة على SMG5 تلتقط العمود الفقري للـRNA وتساعد في وضعه للقطع. عندما عدَّل الباحثون هذه البقايا الحرجة في SMG5 أو SMG6، فقد المجمع المركب الكثير من قوته القاطعة في المختبر. كما فشلت نفس الطفرات في إنعاش NMD في خلايا بشرية مهندَسة جُهِدت فيها البروتينات الطبيعية، رابطين النموذج الهيكلي بوظيفة خلوية حقيقية. 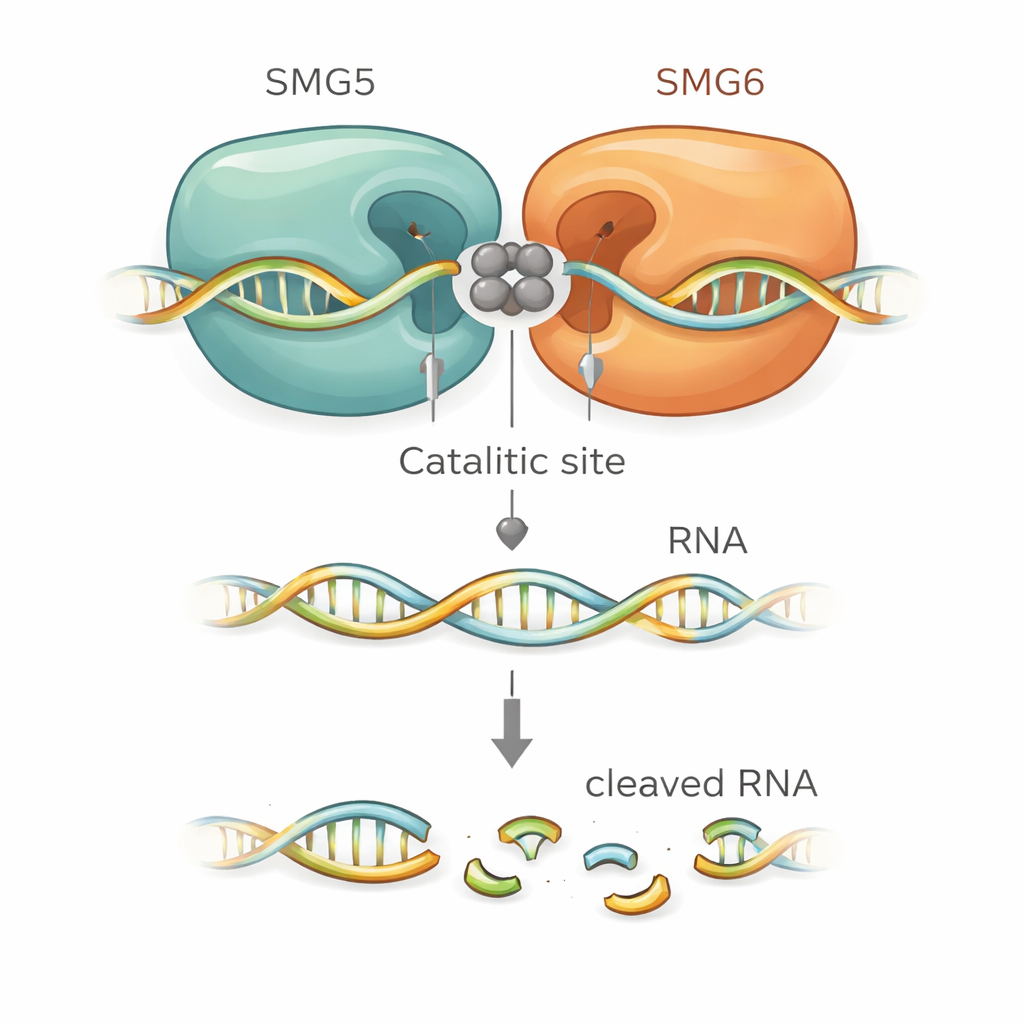
إثبات أن كلا الشريكين ضروريان في الخلايا
لأن الإزالة التامة لـSMG5 أو SMG6 تقتل الخلايا، استخدم الفريق نظام «degron» الذي يمكّنهم من وسم كل بروتين بحيث يمكن تدميره بسرعة بواسطة جزيء صغير. جمعوا هذا التدمير السريع مع تداخل RNA للسماح بالإزالة القريبة من الكاملة لـSMG5 أو SMG6 أو لمُنظِّم مركزي يُدعى UPF1. كشفت تسلسلات RNA على مستوى الجينوم بعد ذلك ما يحدث لـNMD عند فقدان كل عامل. أدت إزالة SMG5 أو UPF1 إلى تغييرات متطابقة تقريبًا في RNAs الخلوية، مع تراكم قوي للنسخ المعيوبة الحساسة لـNMD. وأعطت إزالة SMG6 تأثيرًا مشابهًا إلى حد كبير، وإن كان أخف قليلًا. تُظهر هذه البيانات أن SMG5 وSMG6 ليسا فروعًا اختيارية متوازية للمسار؛ بل إنهما يعملان مع UPF1 كمكونات أساسية لطريق تدهور رئيسي واحد.
لماذا هذا مهم لصحة الخلايا
بعبارة بسيطة، توضح الدراسة أن SMG5 وSMG6 يلتصقان معًا لتشكيل زوج جزيئي واحد قوي من المقصات يقطع الرسائل الجينية المعيبة. يوفر SMG6 معظم النصل، لكن SMG5 يزوّد حافة مفقودة ويساعد في تثبيت الـRNA في مكانه، محولًا قاطعًا ضعيفًا إلى قاطع فعال. يشرح هذا الـ«cPIN» المركب سبب حاجة الخلايا المطلقة لكلٍّ من البروتينين للحفاظ على نظافة رسائلها الـRNA. من خلال توضيح كيفية تفعيل خطوة القص الرئيسية في NMD فقط عند التعرف على الرسائل المعيبة، يقدم العمل صورة أوضح عن كيفية منع الخلايا تراكم بروتينات مختصرة سامة وضبط التعبير الجيني بدقة.
الاستشهاد: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
الكلمات المفتاحية: إزالة الحمض النووي الريبوزي الرسول المحتوي على إيقاف مبكر, مراقبة جودة الـRNA, SMG5 SMG6, مراقبة mRNA, تنظيم التعبير الجيني