Clear Sky Science · ar
العينات الفعالة لمسارات الانتقال واسعة النطاق والت conformations الوسيطة في المجمعات البروتينية تحت الميكروسكوبية
مراقبة البروتينات أثناء الحركة
العديد من الجزيئات التي تحافظ على حياتنا لا تتصرف كقطع ليغو جامدة بقدر ما تتصرف كآلات دقيقة تتغير أشكالها باستمرار. هذه الحركات تغذي عمليات مثل توليد الطاقة، إصلاح الحمض النووي، وإتاحة دخول الفيروسات إلى الخلايا. تجميد الإلكترونيات مثل cryo–EM يمكنها الآن تجميد بعض هذه الأشكال، لكن ليس الخطوات العابرة بينها. يقدم هذا المقال eBDIMS2، طريقة حاسوبية جديدة يمكنها «ملء الإطارات المفقودة» لحركة البروتين حتى بالنسبة للآلات الجزيئية الضخمة التي كانت سابقًا كبيرة ومعقدة جدًا لمحاكاة على كمبيوتر عادي.
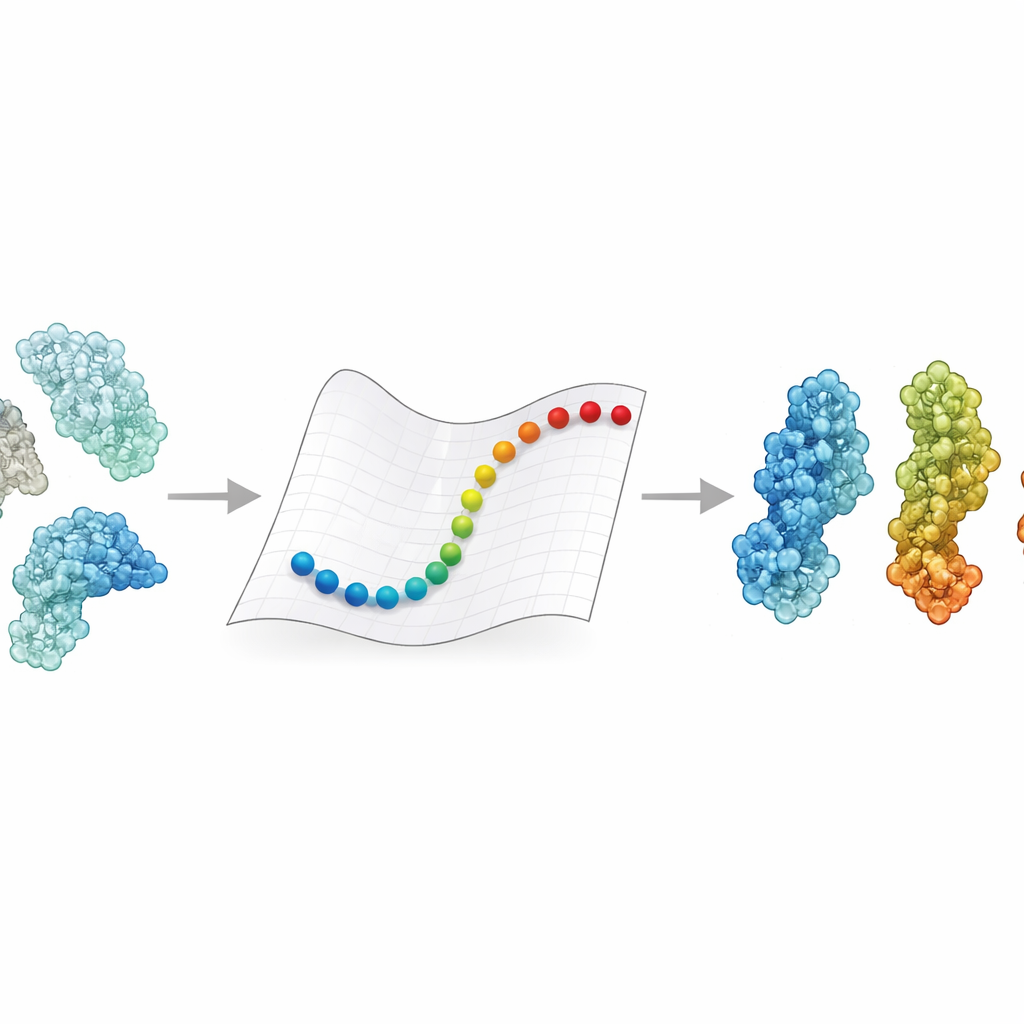
لماذا تهم تغيّرات شكل البروتين
نادراً ما تبقى البروتينات في وضعية واحدة ثابتة. تفتح وتغلق، تلف وتنحني استجابةً لإشارات مثل تغيّر الجهد، الأس الهيدروجيني، أو ارتباط جزيء شريك. هذه التحولات قد تفصل بين كون إنزيم في الحالة الفعّالة أو غيرها، أو تمكن مستقبلًا من التقاط فيروس أو السماح له بالانسلال. التجارب تعطينا لقطات مفصّلة لبعض الأشكال الرئيسية، والمحاكاة الديناميكية الجزيئية يمكن نظريًا ربطها بتتبّع كل ذرة عبر الزمن. لكن تتبع مثل هذه الحركات للمجمعات الضخمة التي تظهر الآن بواسطة cryo–EM، والتي تزن غالبًا مئات الآلاف إلى ملايين الدالتون، يتطلب عادةً حواسب فائقـة وأسابيع من المعالجة. ونتيجة لذلك، بالنسبة للعديد من العمالقة ذات الأهمية الطبية، ما زلنا لا نعرف كيف يتحول أحد الحالات إلى أخرى.
طريق أسرع عبر مناظير البروتين
يأخذ eBDIMS2 طريقًا مختصرًا بتبسيط كيفية تمثيل البروتينات وكيفية حساب حركتها. بدلًا من تتبع كل ذرة، يعامل كل حمض أميني كنقطة واحدة متصلة بنوابض في شبكة مرنة. تلتقط هذه النوابض كيف تميل أجزاء مختلفة من البروتين إلى التحرك معًا. ثم تستخدم الطريقة ديناميكا براونية—قوانين رياضية تحاكي اهتزازات في سائل—لدفع البنية من حالة معروفة تجريبيًا نحو أخرى. والأهم أن eBDIMS2 يركز فقط على التداخلات ذات الأثر الحقيقي، مستخدمًا حدود المسافة والحوسبة المتوازية لتقليل التكلفة. هذا يحسّن مقياس الأداء من نحو تربيعي إلى شبه خطّي بالنسبة لحجم البروتين. عمليًا، يعني ذلك أن الانتقالات لتجمّعات هائلة تقترب من مليوني دالتون يمكن استكشافها في غضون ساعات على جهاز مكتبي، بدلًا من أن تكون شبه مستحيلة الوصول.
فحص المسارات مقابل البروتينات الحقيقية
لمعرفة ما إذا كانت هذه المسارات السريعة منطقية بيولوجيًا، جمع المؤلفون مجموعات مكوّنة من 47 بروتينًا كبيرًا و15 مركبًا إضافيًا، بإجمالي مئات الهياكل التي حُلّت أغلبها بواسطة cryo–EM. استخدموا تحليل المركبات الرئيسية، أداة إحصائية تبرز الطرق السائدة التي يمكن أن يتحرك بها كل بروتين، لتنظيم هذه الهياكل في مناظير تشكيلية مثل مفتوح، مغلق، نشط، أو غير نشط. طُلب من eBDIMS2 بعد ذلك أن يربط أزواج الحالات النهائية عبر هذا المنظر. سُقِطت المسارات الناتجة مرة أخرى على نفس الخرائط قليلة الأبعاد، كاشفةً ما إذا كانت تتبع طرقًا سلسة تمر بالقرب من الوسائط الملاحَظة تجريبيًا. في أكثر من 30% من النظم، مرت المسارات المحاكاة بالقرب—ضمن بضعة أنغسترومات—من هياكل وسيطة لم تُزوَّد كمدخلات. بالنسبة للحالات المتطلبة مثل إنزيم إصلاح الحمض النووي DNA-PKcs أو بروتين السنبلة لفيروس كورونا، تماشت المسارات المجزأة أيضًا بشكل جيد مع محاكاة ذرية أكثر تكلفة بكثير، بما في ذلك ديناميكا جزيئية مستهدفة وجولات متقدمة من العينات المعزّزة.
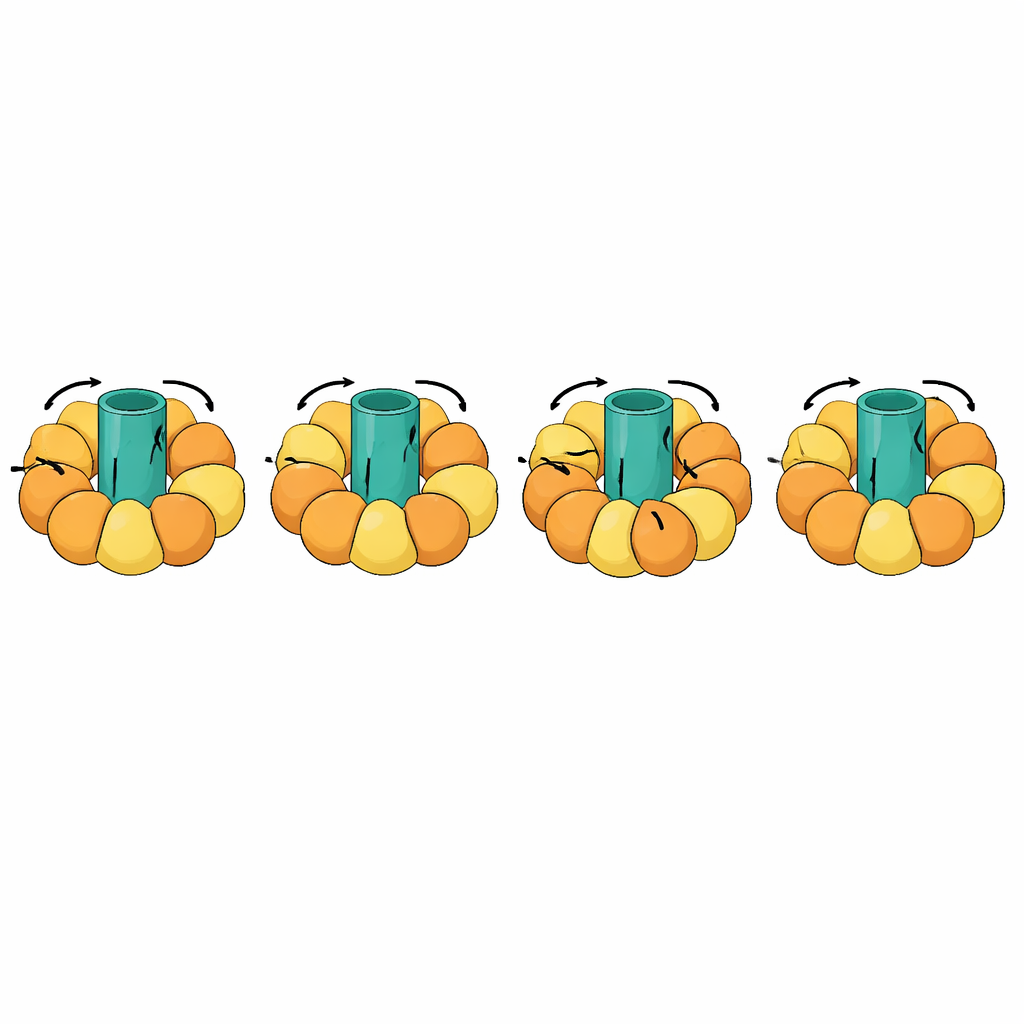
متابعة الآلات الجزيئية العملاقة
أحد أبرز الاختبارات شمل آلات دورانية مثل سينثاز ATP، التي تصنع عملة الطاقة الخلوية بربط دوار دوّار في الغشاء بحركات فتح وإغلاق في الوحدات الفرعية المحيطة. هذه الانتقالات معقّدة للغاية: يجب أن تبقى أجزاء من الجزيء صلبة وتدور كوحدة، بينما تنثني أخرى في دورة منسّقة. يقدم eBDIMS2 معالجة خاصة لمثل هذه القطع شبه الصلبة وللنماذج التجريبية غير المكتملة ذات الأجزاء المفقودة، وكلاهما شائع في cryo–EM. بهذه الميزات، يمكنه محاكاة دورات دورانية كاملة لسينثاز ATP ومجمعات ضخمة أخرى مثل الشابرونات الجزيئية، المستقبلات، والتجمعات الفيروسية. وعلى طول الطريق، تتفادى الهياكل الوسيطة المتولّدة التشوهات الشديدة التي تنتجها بعض الطرق المنافسة، ويمكن تنظيفها لتتحول إلى نماذج ذرية مناسبة لحسابات تصميم الأدوية أو لمحاكاة أطول وأكثر تفصيلًا.
ما الذي يعنيه هذا لعلم الأحياء والطب
تُظهر الدراسة أن eBDIMS2 يمكنه رسم الطرق الرئيسية بين الأشكال البروتينية المعروفة بشكل موثوق لأنظمة كانت خارجة عن نطاق المحاكاة التقليدية. إنه لا يحل محل أفلام ذرية مفصّلة أو يوفر طاقات وتوقيتًا دقيقًا، لكنه يقدم طريقة سريعة ومبنية على قواعد فيزيائية لرسم خرائط كيف قد تتحرك الآلات الجزيئية الكبيرة، باستخدام زوج واحد فقط من الهياكل التجريبية كمدخل. مع امتلاء قواعد البيانات الهيكلية بحالات متعددة لتجمعات بروتينية كبيرة مرتبطة بالسرطان والعدوى وأمراض أخرى، يوفّر هذا النهج أداة في متناول الباحثين لربط النقاط، واقتراح حالات وسيطة معقولة، وتوجيه أين ينظرون بعد ذلك بأساليب أعلى دقة أو في تصميم أدوية موجه.
الاستشهاد: Scaramozzino, D., Lee, B.H. & Orellana, L. Efficient sampling of large-scale transition pathways and intermediate conformations in sub-mesoscopic protein complexes. Nat Commun 17, 2202 (2026). https://doi.org/10.1038/s41467-026-69809-y
الكلمات المفتاحية: ديناميكا البروتين, محاكاة جزيئية, التجميد الإلكتروني, مسارات التّشكل, نمذجة مجزأة