Clear Sky Science · ar
تعديل تفاعلات المعدن-الدعام لتخفيض نترات فعّال عند جهود موجبة
تحويل المياه الملوثة إلى مورد مفيد
تلوث النترات في الأنهار والبحيرات ومياه الصرف الصناعي يشكل مشكلة متنامية للنُظم البيئية وصحة الإنسان، لكنه في الوقت نفسه مورد مهدر. يمكن تحويل نفس النيتروجين الضار بالمياه إلى أمونيا، وهي حجر الزاوية في الأسمدة والوقود والمواد الكيميائية. تستعرض هذه الدراسة طريقة جديدة لتنظيف المياه الملوثة بالنترات مع استعادة الأمونيا باستخدام الكهرباء بكفاءة أعلى من السابق، ما يشير إلى زراعة أنظف، ومعالجة نفايات أكثر ذكاءً، وأشكال جديدة لتخزين الطاقة.
لماذا يشكل فائض النيتروجين مشكلة
تعتمد الزراعة والصناعة الحديثة إلى حد كبير على الأمونيا، التي تُنتَج أساساً بعملية هابر–بوش المكثفة للاستهلاك الطاقي. أثناء الاستخدام والتخلص، يتحول جزء كبير من هذه الأمونيا إلى نترات في مياه الصرف، مما يخل بدورة النيتروجين الطبيعية ويساهم في مشاكل بيئية مثل تكاثر الطحالب وتلوث مياه الشرب. الطرق المتاحة حالياً لإزالة النترات قد تكون مكلفة وقد تقتصر على دفن أو تخفيف المشكلة. التحويل الكهربائي للنترات مرة أخرى إلى أمونيا يوفر وسيلة لتنقية المياه مع إعادة تدوير النيتروجين، لكن معظم الأنظمة الحالية تتطلب طاقة عالية لأنها تعمل عند جهود سالبة قوية.
تصميم سطح محفز أذكى
لمعالجة هذا التحدي، صمّم الباحثون محفزاً جديداً مكوّناً من تجمعات صغيرة جداً من معدن الروثينيوم مثبتة على صفائح رقيقة من هيدروكسيد الكوبالت. استخدموا طريقة بسيطة تسمى «التآكل الذاتي»: رغوة معدنية تذوب ببطء في وجود ملح الروثينيوم والأكسجين، مكونة طبقة هيدروكسيد جديدة بينما تترسب تجمعات الروثينيوم مباشرة فوقها. يمكن تطبيق هذه العملية على معادن مختلفة، لكن الفريق ركّز على دعامات الكوبالت والنيكل والحديد ليرى كيف يؤثر كل منها على الأداء. أكدت الميكروسكوبات والطيفيات أن تجمعات الروثينيوم فائقة الدقة وموزعة بشكل متساوٍ على صفائح الهيدروكسيد، وأنه يحدث انتقال في الإلكترونات بين المعدن ودعمه، مما يضبط بخفة كيفية تفاعل السطح مع النترات والماء.

موازنة الالتصاق والجريان لتحويل أفضل
لكي تسير التفاعل بكفاءة، يجب أن يحدث أمران بتناغم: يجب أن تلتصق جزيئات النترات بسطح المحفز بقوة كافية لتتفاعل، ويجب أن ينفصل الماء عند الواجهة لتزويد ذرات الهيدروجين «النشطة» التي تحول النترات تدريجياً إلى أمونيا. إذا ارتبطت النترات بإحكام شديد، يختنق السطح؛ وإذا كانت الارتباطات ضعيفة جداً، تنسلخ النترات دون أن تُستغل. وبالمثل، يؤدي بطء تفكك الماء إلى حرمان التفاعل من الهيدروجين. أظهرت الاختبارات أن المحفز المعتمد على الكوبالت يحقق هذا التوازن المثالي. بالمقارنة مع نسخ النيكل والحديد، يبدأ التفاعل عند جهد أقرب إلى الجهد المثالي، يصل إلى اختيارية تقارب 100% للأمونيا، ويحقق كفاءة طاقية تقارب 50% عند جهد تشغيل موجب — وهو طلب طاقة منخفض بشكل غير معتاد لهذه الكيمياء. كما يحافظ على نشاط عالٍ لأكثر من 1200 ساعة عند مستويات تيار ذات صلة صناعية، مع إزالة النترات من مياه الصرف المحاكية إلى ما دون حدود مياه الشرب.
الإطلالة على الخطوات الخفية
لفهم سبب تفوّق الكوبالت، راقب الفريق التفاعل في الزمن الحقيقي باستخدام مجسات بصرية وكهروكيميائية، ودعّم الملاحظات بنمذجة حاسوبية. وجدوا أن دعم هيدروكسيد الكوبالت يعيد تشكيل الطبقة الرقيقة من الماء على السطح، مضعفاً شبكة روابط الهيدروجين بحيث تنقسم جزيئات الماء بسهولة أكبر إلى شظايا تفاعلية. في الوقت نفسه، تضبط التفاعلات الإلكترونية بين هيدروكسيد الكوبالت والروثينيوم قوة ارتباط النترات ووسطياتها. تُظهر الحسابات أنه على هذا السطح، تتطلب أصعب خطوة — تحويل شظية شبيهة بالنتروسيل إلى نوع أكثر غنىً بالهيدروجين — طاقة أقل بكثير مقارنة بالإصدارات المدعومة بالنيكل أو الحديد. بعبارة أخرى، يوفر دعْم الكوبالت التوازن المناسب: تُثبت النترات بقوة لكنها لا تُحبس، ويُزوّد الماء الهيدروجين بسرعة، مما يسمح بتتابع الخطوات من النترات إلى الأمونيا بسلاسة.
من تنظيف النفايات إلى الطاقة وإعادة تدوير البلاستيك
بناءً على المحفز الفعّال، جمع المؤلفون بطارية قابلة لإعادة الشحن تقرن معدن الزنك مع اختزال النترات عند الكاثود المصنوع من زوج الكوبالت–الروثينيوم. أثناء التفريغ تُحوَّل النترات إلى أمونيا بينما يتأكسد الزنك، موفِّراً طاقة كهربائية. أثناء الشحن استبدلوا تفاعل تشكل الأكسجين المعتاد بأكسدة ألطف لمركب الإيثيلين غليكول، وهو لبنة بناء يمكن استعادتها من البلاستيك النفاياتي. هذه الحيلة تخفّض الطاقة المطلوبة لإعادة شحن البطارية وترتقي بجزيئات مشتقة من البلاستيك إلى منتجات أكثر قيمة، بينما يمكن أن تُشكِّل الأمونيا المنتجة أملاح أمونيوم. يعمل الجهاز الهجين بثبات عبر دورات عديدة، موضحاً كيف يمكن نسج مكافحة التلوث واستعادة الموارد وتخزين الطاقة في نظام واحد.
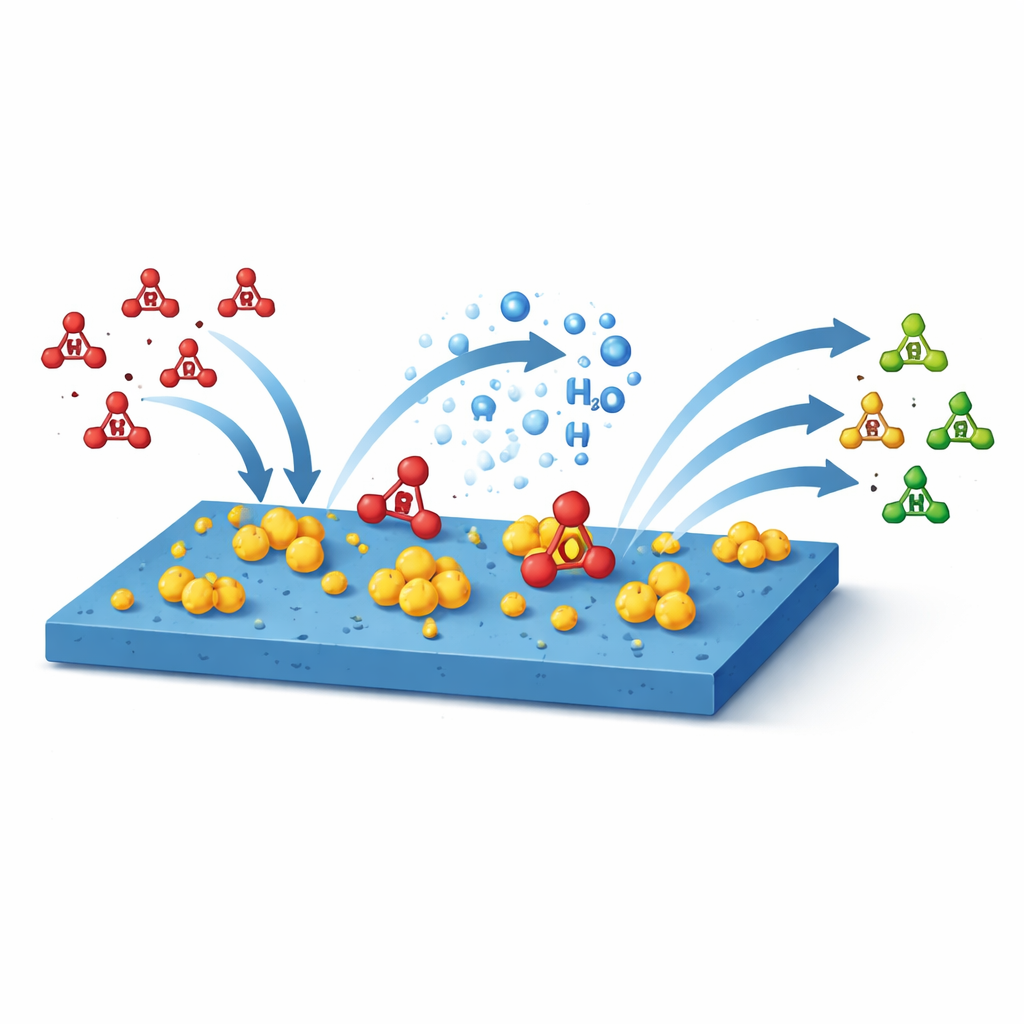
بمصطلحات يسهل الوصول إليها، توضح هذه الدراسة أن الضبط الدقيق لكيفية تفاعل محفز معدني مع مادته الداعمة يمكن أن يحسن بشكل كبير كفاءة تحويل النترات الضارة في الماء إلى أمونيا مفيدة. عبر اختيار دعم لا يمسك النترات بشدة مفرطة ولا يتركها تفلت، ويساعد على تفكك الماء لتغذية التفاعل، بلغ الباحثون كفاءة عالية عند جهود ألطف وحافظوا على الأداء لفترات طويلة. يمكن أن يوجّه نفس مبدأ التصميم — تعديل تفاعلات المعدن والدعم بعناية — تطوير محفزات مستقبلية للعديد من العمليات الكيميائية المستدامة الأخرى.
الاستشهاد: Tang, Y., Wan, Y., Yan, W. et al. Modulated metal-support interactions for efficient nitrate electroreduction at positive potentials. Nat Commun 17, 3006 (2026). https://doi.org/10.1038/s41467-026-69802-5
الكلمات المفتاحية: تلوث النترات, إنتاج الأمونيا, التحفيز الكهربائي, معالجة مياه الصرف, تخزين الطاقة