Clear Sky Science · ar
نظائر الأسيتيل-لايزين المقاومة للتحلل لدراسة أسيتلة البروتينات في المختبر وداخل الخلايا
لماذا تهم العلامات الكيميائية الصغيرة على البروتينات
داخل كل خلية، تُجرى تعديلات دقيقة على البروتينات باستخدام علامات كيميائية صغيرة تعمل كمفاتيح تشغيل/إيقاف أو كمخفتات لشدة نشاطها. واحدة من أهم هذه العلامات تُسمى الأسيتلة، التي يمكنها تغيير سلوك البروتين دون تغيير الشفرة الجينومية الأساسية. كان من الصعب بشكل غير متوقع فهم ماذا تفعل الأسيتلة في موقع محدد على بروتين معين، لأن الخلايا قادرة على إزالة هذه العلامات بسرعة كما تضيفها. تقدّم هذه الدراسة نظيرًا كيميائيًا ذكيًا للأسيتلة لا يمكن إزالته، مما يمنح العلماء وسيلة لتجميد هذه المفاتيح ومراقبة ما يحدث.
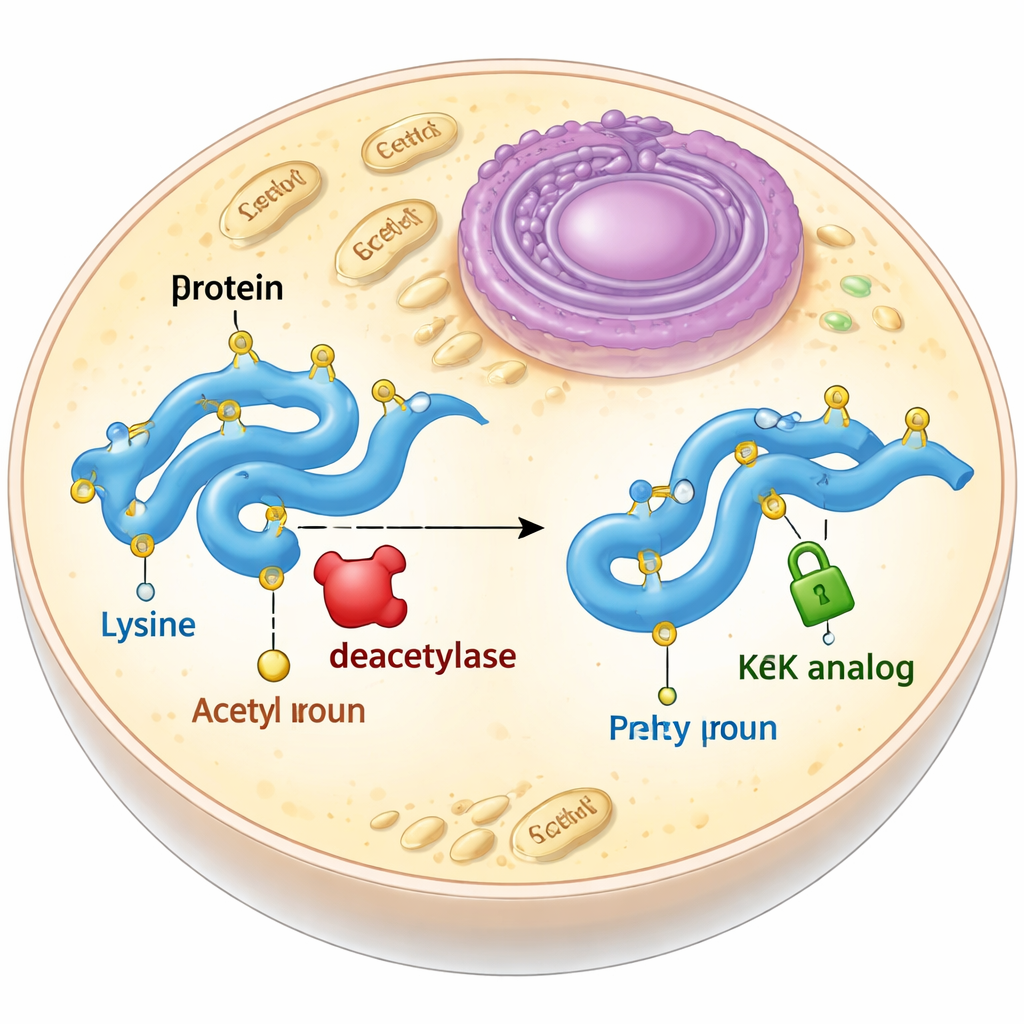
بديل ثابت لعلامة زائلة
تحدث الأسيتلة عادةً على بُنية بناء في البروتينات تُدعى الليزين. عندما تُأسَتِل الليزين، يفقد شحنته الموجبة ويطول سلسلة جانبه قليلاً. غالبًا ما يحاول البيولوجيون محاكاة ذلك عن طريق تغيير الليزين إلى حمض أميني آخر مثل الجلوتامين، الذي لا يكون مشحونًا لكنه أقصر، أو بإضافة أسيتيل-لايزين حقيقي عبر توسيع الشفرة الجينية. لكل منهما عيوب: الجلوتامين لا يعيد تمامًا التغيرات الشكلية التي تحدثها الأسيتلة، والأسيتيل-لايزين الحقيقي يُزال بسرعة بواسطة إنزيمات تُدعى دي-أسيتلاز داخل الخلايا. سعى المؤلفون إلى تصميم واختبار نظائر للأسيتيل-لايزين تحافظ على الحجم والشكل المناسبين لكن لا يمكن إزالتها.
اختبار المحاكيات الكيميائية الجديدة على بروتين نموذجي
ركّز الفريق أولًا على اليوبيكويتين، وهو بروتين صغير معروف يتزيّن بنفسه بالعديد من العلامات المختلفة. باستخدام هندسة جينية متقدمة، وضعوا متباينات ليزين مختلفة في موقع واحد من اليوبيكويتين: أسيتيل-لايزين الطبيعي، ونظيران غير قابلين للإزالة يدعيان TFAcK والكتوليزين (KeK)، وكذلك بدائل شائعة مثل الجلوتامين والألانين والأرجينين. ثم درسوا كيف أثّرت هذه التغييرات على شكل اليوبيكويتين ووظيفته. أظهرت قياسات رنين مغناطيسي نووي عالية الدقة أن الأسيتيل-لايزين وTFAcK وKeK أحدثت تغييرات بنيوية متطابقة تقريبًا، لا سيما حول حلزون مركزي، بينما لم تفعل الجلوتامين والطفرات البسيطة الأخرى ذلك. اختبارات وظيفية باستخدام إنزيم يدعى HDM2 أظهرت أن اليوبيكويتين الحامل للأسيتيل-لايزين أو TFAcK أو KeK تصرّف بشكل مماثل ومختلف عن نسخة الجلوتامين، مما يؤكد أن طول وحجم سلسلة الجانب — وليس الشحنة وحدها — أمور حاسمة.
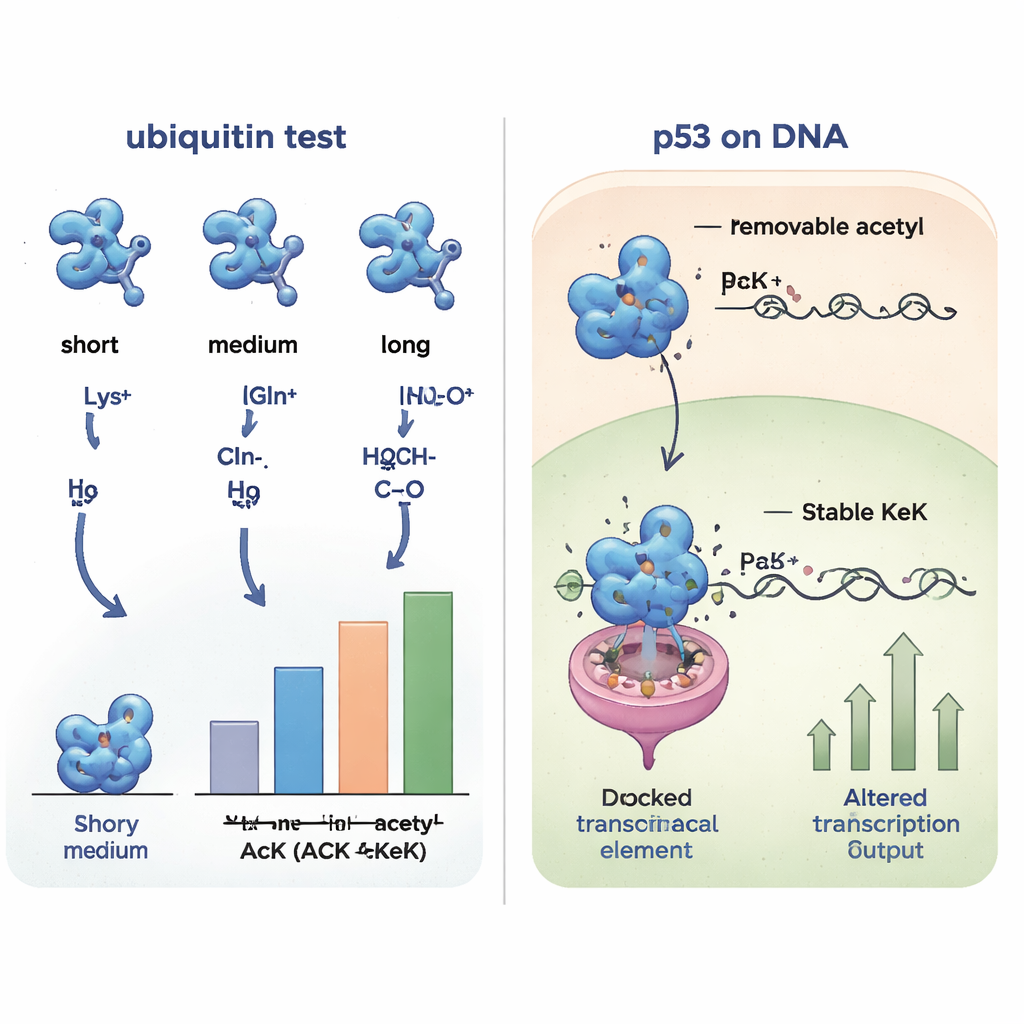
استكشاف شراكات البروتين عبر الخلية
نظرًا لأن تغييرات بنيوية طفيفة يمكن أن تغيّر الشركاء الذين يتعامل معهم البروتين، قارن الباحثون بعد ذلك كيف ارتبطت نسخ اليوبيكويتين المختلفة ببروتينات أخرى من مستخرجات خلايا بشرية. عن طريق اصطياد الشركاء المرتبطين وتحديدهم باستخدام القياس الطيفي الكتلي، وجدوا أن اليوبيكويتين المحتوي على أسيتيل-لايزين أو TFAcK أو KeK شارك أنماط تداخل متشابهة جدًا، بينما الأشكال المحتوية على جلوتامين أو ألانين تجمّعت معًا بدت مختلفة. المتباينات المشحونة موجبًا (الليزين أو الأرجينين) شكلت مجموعة ثالثة. أظهر هذا المقارنة المنهجية أن النظائر غير القابلة للإزالة TFAcK وخاصة KeK تحاكي كلًا من البنية وسلوك الارتباط للأسيتلة الحقيقية بشكل أفضل بكثير من بديل الجلوتامين التقليدي.
تثبيت الأسيتلة على مكبح الورم p53
للاختبار داخل خلايا حية، توجه المؤلفون إلى p53، وهو مكبح ورم أساسي يُطلق عليه غالبًا "حارس الجينوم". يمكن أن تُأسَتِل ليزينات محددة في منطقة ارتباط p53 بالحمض النووي، مغيرةً الجينات التي يشغّلها، مثل تلك التي توقف دورة الخلية أو تحفز موت الخلية. مهندس الفريق خلايا بشرية بحيث يُضمَّن في p53 أسيتيل-لايزين أو TFAcK أو KeK في موضعي ليزين مهمين (120 و164) فقط عندما يُزوَّد الحمض الأميني غير القياسي المقابل. كان بالإمكان إدراج الثلاثة في p53، لكن القياسات التفصيلية أظهرت أنه داخل الخلايا تُزال مجموعات الأسيتيل وTFAcK إلى حد كبير بواسطة دي-أسيتلازات، بينما بقي KeK سليمًا. عند اختبار قدرة p53 على تنشيط جين تقرير وجين p21 الطبيعي، كانت المتباينات الحاملة KeK في هذه المواقع أقل نشاطًا بكثير، وهو ما يتوافق مع توقعات تثبيت الأسيتلة في تلك المواقع، بينما تصرّف الأسيتيل-لايزين وTFAcK أقرب إلى p53 الطبيعي لأنهما تم إزالتهما.
ماذا يعني هذا لدراسة قرارات الخلية
بالمجمل، تُظهر الدراسة أن KeK هو بديل أمين وغير قابل للإزالة للأسيتيل-لايزين: يعيد بدقة التغيرات البنائية وتفضيلات الارتباط والنتائج الوظيفية للأسيتلة، لكنه لا يمكن أن يُمحى بواسطة إنزيمات الخلية. بالنسبة لغير المتخصصين، هذا يعني أن لدى الباحثين الآن وسيلة لـ"تجميد" مفتاح كيميائي عكوس في موقع واحد على بروتين ثم مراقبة كيف يؤثر ذلك على عمليات مثل تنظيم الجينات وقرارات مصير الخلية. ينبغي أن يسهل هذا تفكيك الأدوار المحددة للأسيتلة عن تلك للتعديلات المتداخلة الأخرى، وقد يوضح في النهاية كيف يساهم خلل تنظيم أسيتلة البروتين في أمراض مثل السرطان.
الاستشهاد: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
الكلمات المفتاحية: أسيتلة البروتين, تعديل بعد الترجمة, يوبيكويتين, p53, توسيع الشفرة الجينية