Clear Sky Science · ar
إعادة تشكيل النسخ الجيني الديناميكية في الخلايا الجذعية العصبية البشرية المزروعة تكشف آليات للحفاظ على الرؤية في نموذج فأري لالتهاب الشبكية الصباغي
لماذا حماية البصر المتلاشي مهمة
التهاب الشبكية الصباغي هو مجموعة من الأمراض الوراثية التي تسلب البصر تدريجياً، غالباً ما تبدأ بعتمة الرؤية الليلية وتتقدم نحو العمى القانوني. وبما أن مئات الطفرات الجينية المختلفة يمكن أن تسبب هذه الحالة، فإن علاج كل منها على حدة عبر العلاج الجيني صعب. تستكشف هذه الدراسة نهجاً أكثر شمولية: زرع خلايا جذعية عصبية بشرية — خلايا عصبية غير ناضجة مزروعة مخبرياً — في العين لحماية الخلايا الحسية الضوئية المتبقية. وفهم كيف تتصرف هذه الخلايا المزروعة وتساهم في الحفاظ على الرؤية قد يوجه علاجات مستقبلية ليس فقط لالتهاب الشبكية الصباغي بل أيضاً لاضطرابات تسبب العمى عامة.
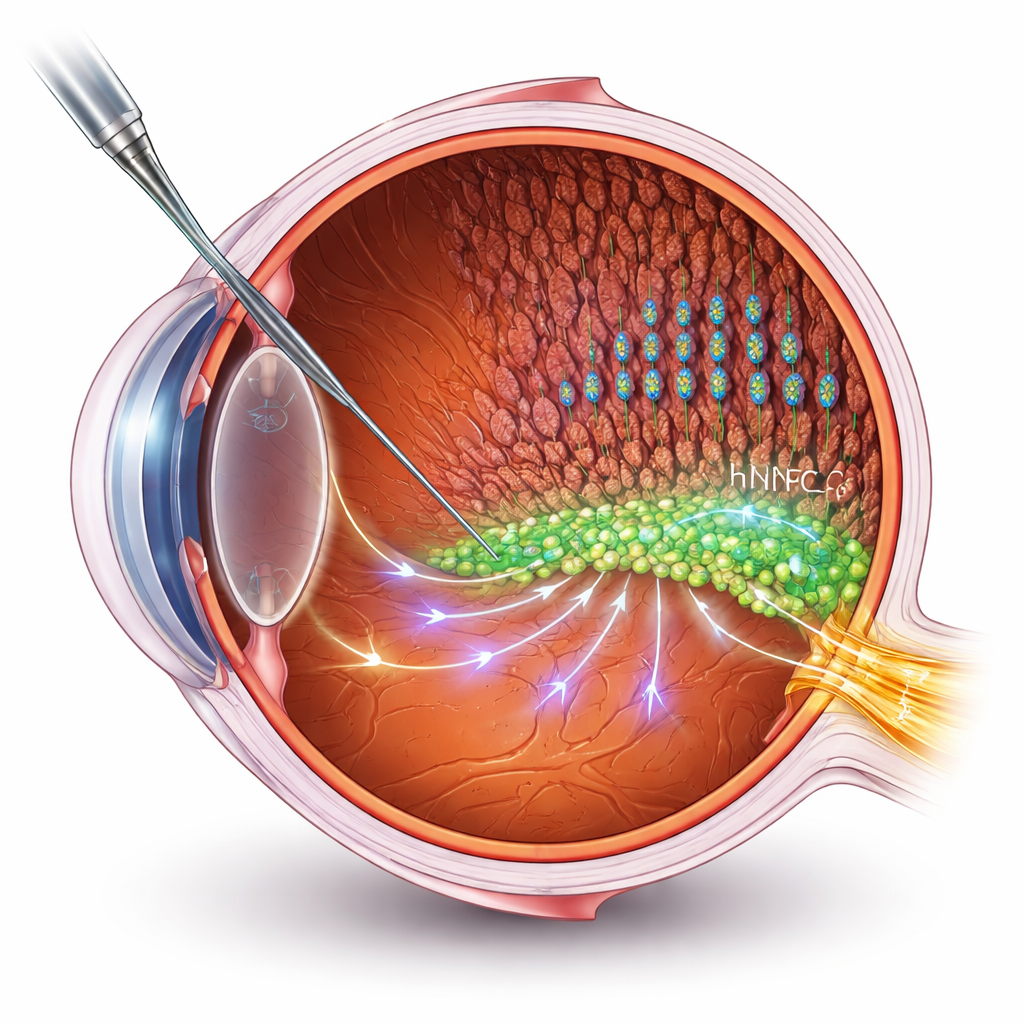
مساعدة الخلايا بدلاً من استبدالها
تهدف العديد من علاجات الخلايا الجذعية إلى استبدال الخلايا الميتة أو التالفة. لكن في أمراض الشبكية المتقدمة، يمثل بناء اتصالات جديدة مع الدماغ عقبة تقنية كبيرة. اتخذ الباحثون هنا مساراً مختلفاً: استخدام الخلايا الجذعية العصبية البشرية (hNPCs) كـ«مساعدين» يدعمون خلايا الشبكية لدى المريض. قاموا بزرع hNPCs في المساحة تحت الشبكية في نموذج فأري معروف لالتهاب الشبكية الصباغي، ثم قيَّموا الرؤية باستخدام تسجيلات كهربائية واختبارات سلوكية. حافظت الجرذان المعالجة على وظائف بصرية أفضل وطبقات فوتوريسبتيفية أكثر سلامة — القضبان والمخاريط التي تلتقط الضوء — مقارنةً بالحيوانات غير المعالجة، رغم استمرار التدهور التدريجي.
كيف تتغير الخلايا المزروعة داخل العين المريضة
لمعرفة ما يحدث على المستوى الجزيئي، استخدم الفريق تسلسل RNA على مستوى الخلية الواحدة، تقنية تحدد الجينات النشطة في آلاف الخلايا الفردية. تتبعوا الخلايا المزروعة في نقطتي زمن تقريبتين، مرحلتين مبكرة ومتأخرة بعد الزرع. بدلاً من التحول إلى فوتوريسبتورات جديدة، نضجت معظم الخلايا المزروعة إلى خلايا دعم شبيهة بالنجمات (astrocyte-like)، بينما أبدت نسبة أصغر علامات للخلايا النخاعية المغلفة (oligodendrocytes) أو الخلايا العصبية غير الناضجة. مع مرور الوقت استقرت هذه الخلايا، متبنية ميزات توحي بأنها متأقلمة للنجاة في بيئة ضاغطة ومتدهورة وللتفاعل عن قرب مع خلايا الشبكية المجاورة.
إشارات وقائية، أيض، وإزالة الحطام
أنتجت hNPCs خليطاً غنياً من البروتينات الوقائية المعروفة بالعوامل التغذوية. من بينها MANF وMYDGF المرتبطة ببقاء الخلايا، وتقليل الإجهاد التأكسدي، وخفض الالتهاب، بالإضافة إلى عوامل أخرى مثل ميدكين وبليوتروفتين التي تدعم نمو وحركة الخلايا العصبية. بدا أن هذه الجزيئات تؤثر على الطُعم نفسه وعلى الشبكية المحيطة. في الجرذان المعالجة، أظهرت القضبان والمخاريط أنماط تعبّر جينية أقرب إلى الضوابط السليمة، مع دعم محسن للإشارات البصرية وصيانة الخلايا. كما عززت الخلايا المزروعة مسارات معنية بإزالة الحطام الخلوي وتكييف الأيض، ما يشير إلى أنها تساعد الفوتوريسبتورات على مواجهة متطلبات الطاقة والنواتج السامة التي تتراكم أثناء المرض.
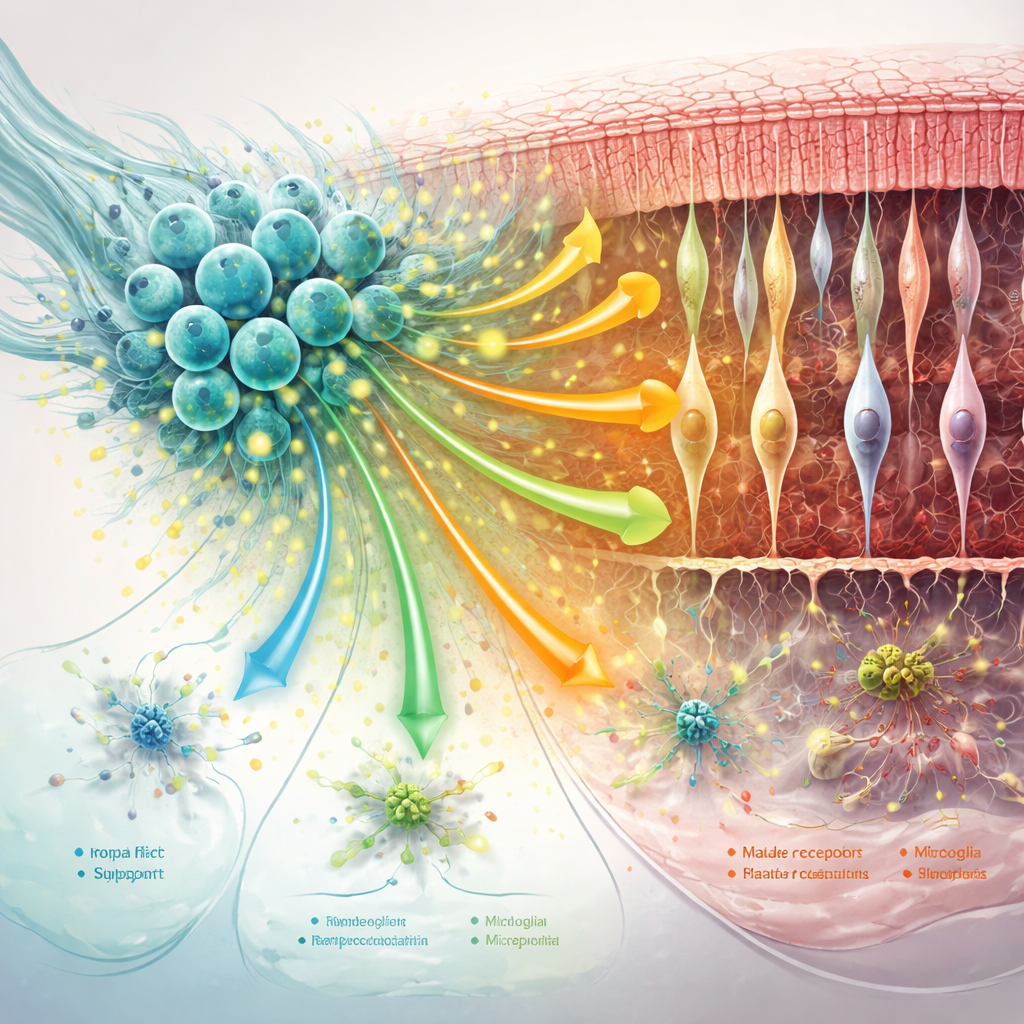
تهدئة خلايا الدعم وإعادة تشكيل البيئة الشبكية
يلعب نظام الدعم في الشبكية — خلايا مولر، والمايكروغليا، والمصفوفة البروتينية المحيطة — دوراً كبيراً في تفاقم أو إبطاء التنكس. وجدت الدراسة أن علاج hNPC خفف من العلامات الأساسية للتغيرات «التفاعلية» الضارة في خلايا مولر وحوّل المايكروغليا بعيداً عن حالات التهابية مفرطة، خاصة في المراحل المبكرة. في الوقت نفسه، تقويت إشارات التواصل التي تساعد على استقرار المشابك، ولصق الخلايا معاً، والحفاظ على الهيكل الداعم حول الفوتوريسبتورات. ومع تقدم المرض تلاشت بعض هذه الفوائد: ضعف الاتصال الخلوي العام، وانخفاض بعض المسارات الوقائية — بما في ذلك إشارات مرتبطة بـMANF —، وتبنت خلايا الدعم ملفات تعبيرية أكثر تركيزاً على الإجهاد والمناعة.
ماذا يعني هذا لعلاجات العين المستقبلية
لغير المتخصص، الخلاصة هي أن الخلايا الجذعية العصبية البشرية المزروعة يمكن أن تعمل كـ«المستجيبين الأوائل» في موقع التحلل الشبكي. إنها لا تعيد بناء الشبكية من الصفر، لكنها تفرز جزيئات وقائية، وتعدّل الأيض، وتخفف الالتهاب الضار، وتساعد على الحفاظ على البنية المحلية سليمة، وكل ذلك يبطئ فقدان البصر. ومع ذلك، تتلاشى هذه الفعالية مع مرور الوقت عندما تصبح البيئة أكثر عدائية ويضعف الحوار بين الطعم وخلايا المضيف. يقترح المؤلفون أن تعزيز عوامل رئيسية مثل MANF وتحسين صحة شبكية المضيف — ربما عبر هندسة جينية للطعم أو علاجات مركبة — قد يكون ضرورياً لتحويل التخفيف المؤقت إلى حفاظ طويل الأمد على البصر.
الاستشهاد: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
الكلمات المفتاحية: التهاب الشبكية الصباغي, علاج بالخلايا الجذعية, تنكس الشبكية, حماية عصبية, تسلسل RNA على مستوى الخلية الواحدة