Clear Sky Science · ar
توسط TCL1A: خلل مثيلي في الحمض النووي في الزُرَيبات المائية المتكررة مع طفرات ممرِضة في NLRP7
لماذا هذا مهم لصحة النساء
في بعض حالات الحمل يحدث خلل مبكّر جداً، فتتحول الكتلة إلى نسيج مشيمي غير طبيعي بدلاً من جنين نامٍ. تُعرَف هذه الحالة بالزرَيبة المائية، ويمكن أن تتكرر لدى بعض النساء وفي أحيانٍ تتطوّر إلى سرطان. تتعمق هذه الدراسة في سبب وراثي رئيسي لهذه الحالات النادرة لكن الخطيرة وتكشف كيف يمكن لخلل واحد في آلية حماية موجودة في البويضة أن يعطل «العلامات» الكيميائية التي تُوجّه التطور السليم.
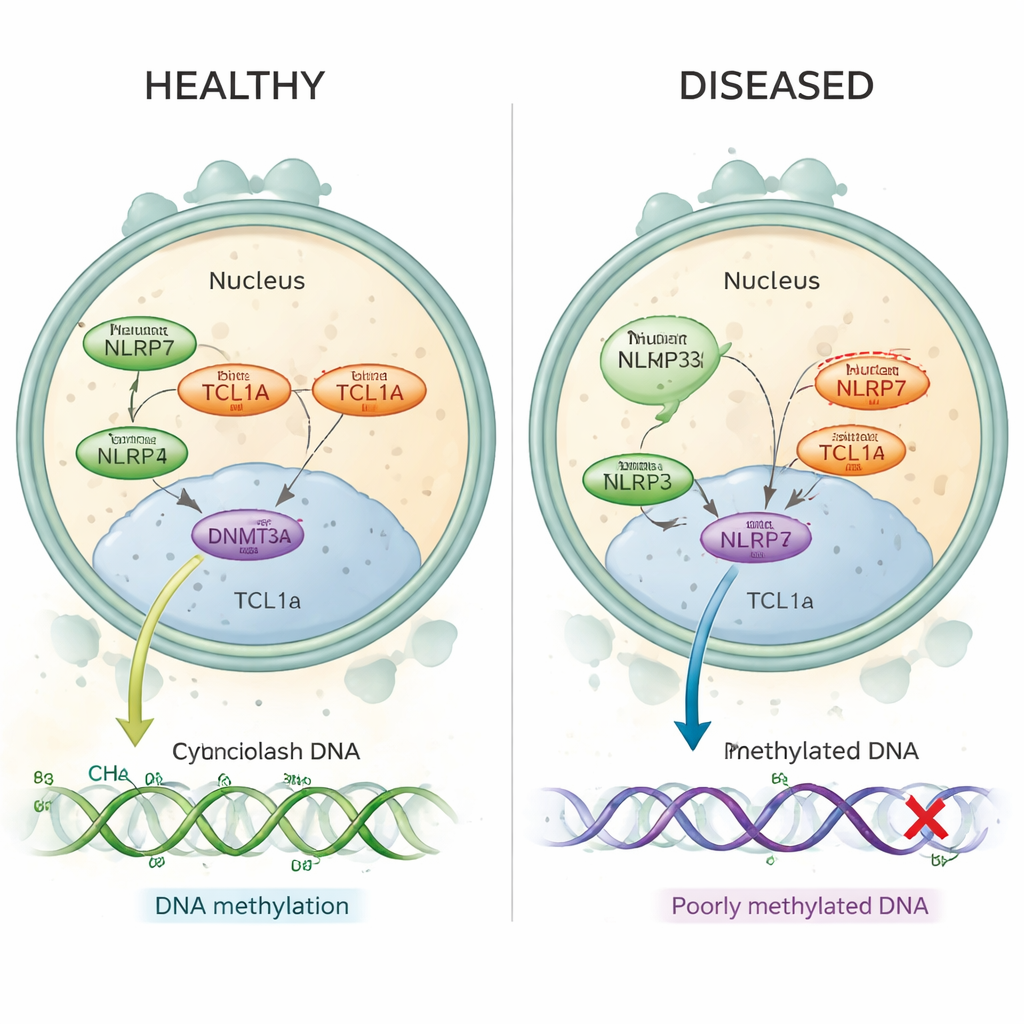
مشكلة حمل متأصلة في البويضة
الزرَيبة المائية المتكررة هي اضطراب تُعاني فيه النساء من حالات حمل مولرية متكررة، غالباً دون وجود حالات حمل طبيعية بينها. وُجد أن العديد من هذه الحالات ناجمة عن تغيّرات ضارة في جين يُدعى NLRP7، الذي ينشط في البويضة قبل وبعد الإخصاب مباشرة. في هؤلاء النساء، تخلو مناطق مهمة من الحمض النووي والتي يفترض أن تحمل «بصمات» أمومية من علامات المثيلة الطبيعية—وهي وُسَمات كيميائية صغيرة تساعد على تشغيل أو إيقاف الجينات في الوقت المناسب. حتى الآن، لم يفهم العلماء كيف يمكن لبروتين موجود في سيتوبلازم البويضة، مثل NLRP7، أن يتحكم في مثيلة تحدث على الحمض النووي داخل النواة.
البحث عن شريك مفقود
لحل هذا اللغز، فحص الباحثون بويضات بشرية مرفوضة وأجنة في مراحل بدائية جدًا من عيادات الخصوبة. سحبوا NLRP7 وشركاءه المعروفين من هذه الخلايا وحددوا بروتينات أخرى ترتبط به. برز بروتين واحد: TCL1A، المعروف بالفعل في سرطانات الدم كبروتين يمكن أن ينتقل إلى النواة ويتداخل مع إنزيمات مثيلة الحمض النووي المسماة DNMT3A وDNMT3B. يوجد TCL1A بوفرة غير عادية في البويضات البشرية، ما يوحي بدور مهم له هناك. أظهرت اختبارات التفاعل التفصيلية أن TCL1A يرتبط بقوة وبشكل محدد مع NLRP7، وليس مع بروتينات قريبة الصلة، وأن هذا المركب مُدمَج في بنية أكبر خاصة بالبويضة تُسمى المركب الأمّي تحت القشري.
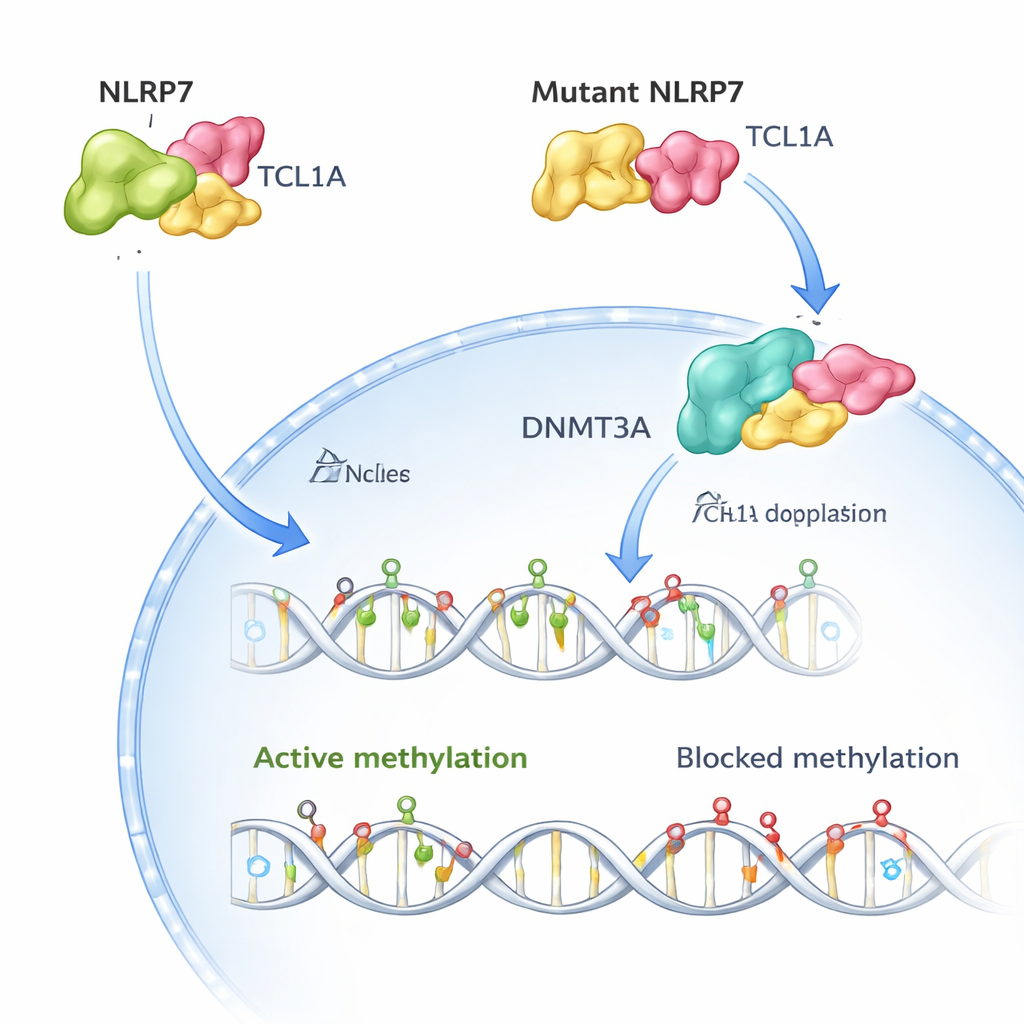
رؤية العناق الجزيئي
استخدم الفريق بعدها المجهر الإلكتروني المجمد لتصوير البنية ثلاثية الأبعاد لمركب NLRP7–TCL1A. وجدوا أن جزيئتين من NLRP7 تتزاوجان، ولكل واحدة منهما قبضة على ثنائي TCL1A على سطح منحني من تكرارات نمطية. يفسّر هذا الترتيب سبب تجمع العديد من التغيرات المسببة للمرض في NLRP7 على ذلك السطح: تعديل نقاط تلامس رئيسية يُضعف أو يدمر العناق مع TCL1A. عندما أعاد الباحثون تكوين أكثر من 50 متغيرًا معروفًا من مرضى في خلايا، فقد تسببت معظم النسخ المرتبطة بالزرَيبات المتكررة في إزعاج استقرار NLRP7 أو تقليل كبير في قدرته على ربط TCL1A.
كيف تُزعزع البروتينات المتموضعة بشكل خاطئ علامات الحمض النووي
في البويضات البشرية السليمة، يوجد كل من NLRP7 وTCL1A في الغالب في السيتوبلازم، مع وصول كمية صغيرة فقط من TCL1A إلى النواة. تُظهر الدراسة أن NLRP7 يعمل فعلاً كحارس بوابة: عندما يستطيع NLRP7 احتجاز TCL1A يبقى TCL1A خارج النواة. عندما يُطفأ هذا الاحتجاز بسبب طفرات في NLRP7 ولا يعود قادرًا على الارتباط جيدًا، يتسرب TCL1A إلى النواة. هناك يرتبط بـ DNMT3A، الإنزيم الرئيسي الذي يضع علامات المثيلة الجديدة في البويضات، ويخفف من نشاطه. في نماذج خلايا جذعية تكتسب عادة المثيلة أثناء نضوجها، أدى إنتاج كميات مفرطة من TCL1A إلى فقدان دراماتيكي في المثيلة عبر الجينوم، بينما أعاد التعبير المشترك مع NLRP7 هذا الخلل جزئيًا. تدعم هذه النتائج تصورًا بسيطًا: يحافظ NLRP7 الطبيعي على «فرامل» المثيلة (TCL1A) محبوسة في السيتوبلازم حتى تتمكن DNMT3A من وسم الحمض النووي بشكل صحيح؛ أما NLRP7 المعطوب فيسمح لتلك الفرملة بالانزلاق إلى النواة وعرقلة العملية.
من الآلية إلى التشخيص
بعيدًا عن تفسير كيفية نشوء حالات الحمل المولرية المتكررة، تقترح الدراسة طريقة عملية لتقييم ما إذا كان تغيير جديد في NLRP7 لدى مريضة ضارًا بالفعل. يقارن المؤلفون ثلاث طرق—اختبارات مختبرية لارتباط NLRP7–TCL1A، وتنبؤات حاسوبية، وأدوات تصنيف جينية قياسية—ويظهرون أن فقدان ربط TCL1A يتوافق بشكل وثيق مع المتغيرات المسببة للمرض. كما يكشفون عن متغير ضار لم يكن معترفًا به سابقًا، L766R، في عائلات تعاني من زُرَيبات متكررة، مؤكِّدين أنه يضعف البروتين ويوجّه TCL1A إلى النواة بشكل خاطئ.
ما معناه ببساطة
تكشف هذه الورقة سلسلة تفاعلات جزيئية وراء اضطراب حمل نادر لكنه مدمّر. باختصار، تحمل بويضات النساء المتأثرات بروتين «حارس» معطوب، NLRP7، يفشل في إبقاء شريكه TCL1A خارج النواة. وبمجرد دخوله، يتداخل TCL1A مع الإنزيم الذي يضع الوسم الكيميائي الحيوي الضروري على الحمض النووي. دون تلك الوسوم، ينمو المشيماء المبكر على نحو غير طبيعي ولا يتكوّن جنين. من خلال تتبّع هذه المسار خطوة بخطوة، توضح الدراسة لماذا يمكن لتغيّرات وراثية معينة لدى الأمهات أن تخرب حالات الحمل بشكل متكرر وتفتح الطريق لإرشاد جيني وتشخيص أدق للنساء المصابات بالزرَيبة المائية المتكررة.
الاستشهاد: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
الكلمات المفتاحية: مثيلة الحمض النووي, الزرَيبة المائية المتكررة, NLRP7, TCL1A, الطبع الجيني الجينومي