Clear Sky Science · ar
منطقة N-Myc MB0-MBI تتفاعل بشكل محدد وديناميكي مع الفص الأمامي لـ Aurora kinase A
لماذا يهم هذا لعلاج السرطان
تعتمد العديد من الأورام الطفولية العدوانية على بروتين يسمى N-Myc للحفاظ على تكاثر الخلايا السرطانية. يصعب استهداف N-Myc مباشرة بالأدوية لأنه يتصرف أكثر كقطعة معجنات رخوة بدلاً من شكل صارم يمكن لمفتاح أن يناسبه. تكشف هذه الدراسة، بتفصيل غير مسبوق، كيف يتمسك N-Myc ببروتين آخر، الإنزيم Aurora kinase A (AurA)، لتعزيز نشاطه ومساعدة خلايا السرطان على البقاء. من خلال رسم خريطة هذه الشراكة، يكشف الباحثون عن طريقة واقعية لتفكيكها باستخدام جزيئات صغيرة.
مُسبب فوضى مرن يجد شريكًا صلبًا
ينتمي N-Myc إلى عائلة MYC التي تعمل كمفاتيح رئيسية تتحكم في نمو الخلايا والتمثيل الغذائي والانقسام. عندما يُنتج بكميات زائدة، تتحول هذه المفاتيح إلى محركات قوية للسرطان، لا سيما في أورام الجهاز العصبي مثل الورم العصبي النخاعي عالي المخاطر لدى الأطفال. خلافًا للعديد من الإنزيمات أو المستقبلات، لا يطوي N-Myc نفسه إلى شكل ثلاثي الأبعاد ثابت؛ إنه «بروتين مضطرب جوهريًا» يتهدل ويتغير شكلَه باستمرار. تمنحه هذه المرونة قابلية تكيّف لكنها تجعله أيضًا من الصعب استهدافه بالعقاقير. بالمقابل، يُعد AurA إنزيمًا مُنظمًا جيدًا يساعد في تنظيم انقسام الخلية. أظهرت أعمال سابقة أن AurA يساعد في استقرار N-Myc في الخلايا الورمية وأن البروتينين يتفاعلان جسديًا، لكن طبيعة ونِطاق نقاط التماس الدقيقة وأهميتها ظلت غير واضحة.
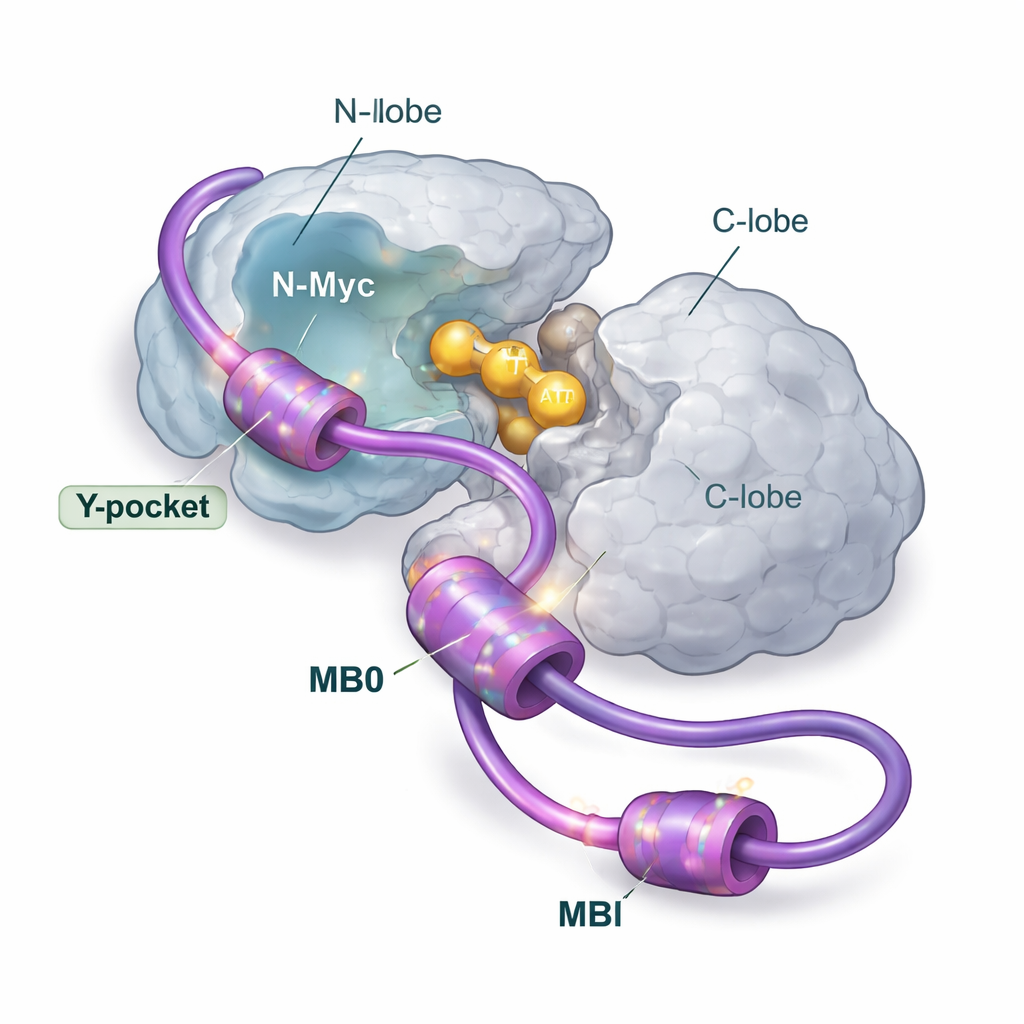
نقاط تماس متعددة، منصة هبوط رئيسية واحدة
باستخدام مجموعة واسعة من الأساليب الهيكلية والبيوفيزيائية، بما في ذلك الرنين المغناطيسي النووي، وتشتت الأشعة السينية، والطيف الكتلي، والحراريات، والنمذجة الحاسوبية، يحلل المؤلفون كيف يتجمع N-Myc وAurA في المحلول. ركزوا على الطرف الأمامي لـ N-Myc، الذي يحتوي على منطقتين محفوظتين تُسميان MB0 وMBI. هذه القِطع القصيرة غنية بالمكونات العطرية (مثل الفينيل ألانين والتيروزين والتريبتوفان) التي تميل إلى الالتصاق بالجيوب الشحمية على بروتينات الشريك. تُظهر النتائج أن N-Myc يرتبط بـ AurA بشكل أساسي بنسبة 1:1، مع عمل MB0 وMBI كمناطق التماس الأساسية. ويتضح أن قطعة أخرى من N-Myc التي كانت محط اهتمام في هياكل البلورة السابقة تلعب دورًا ثانويًا فقط عندما تكون منطقة MB0–MBI الكاملة حاضرة.
مصافحة ديناميكية تُفعّل الإنزيم
بدلًا من الانقفال في وضع واحد ثابت، يبقى N-Myc غير منظم إلى حد كبير عند ارتباطه بـ AurA. تشير البيانات إلى مركب «غائم»: أجزاء متعددة من N-Myc تتناوب على لمس بقع مختلفة في الفص الأمامي لـ AurA، خصوصًا أخدود معروف باسم الجيب Y وحلقة قريبة تربط الإشارات بموقع النشاط. رغم هذا التراخي، فإن التأثير واضح—ارتباط MB0 وMBI يثبت الفص الأمامي لـ AurA ويزيد من نشاط الكيناز الخاص به، مما يعني أنه ينقل مجموعات الفوسفات إلى أهدافه بكفاءة أكبر. عندما استبدل الباحثون منهجياً البقايا العطرية الرئيسية في MB0 وMBI بالألانين، أصبح مركب N-Myc–AurA أضعف، وقل استقرار الإنزيم، وانخفض نشاطه. يبيّن هذا أن «مراسي» عطرية محددة في سلسلة N-Myc المرنة ضرورية لتفعيل AurA.
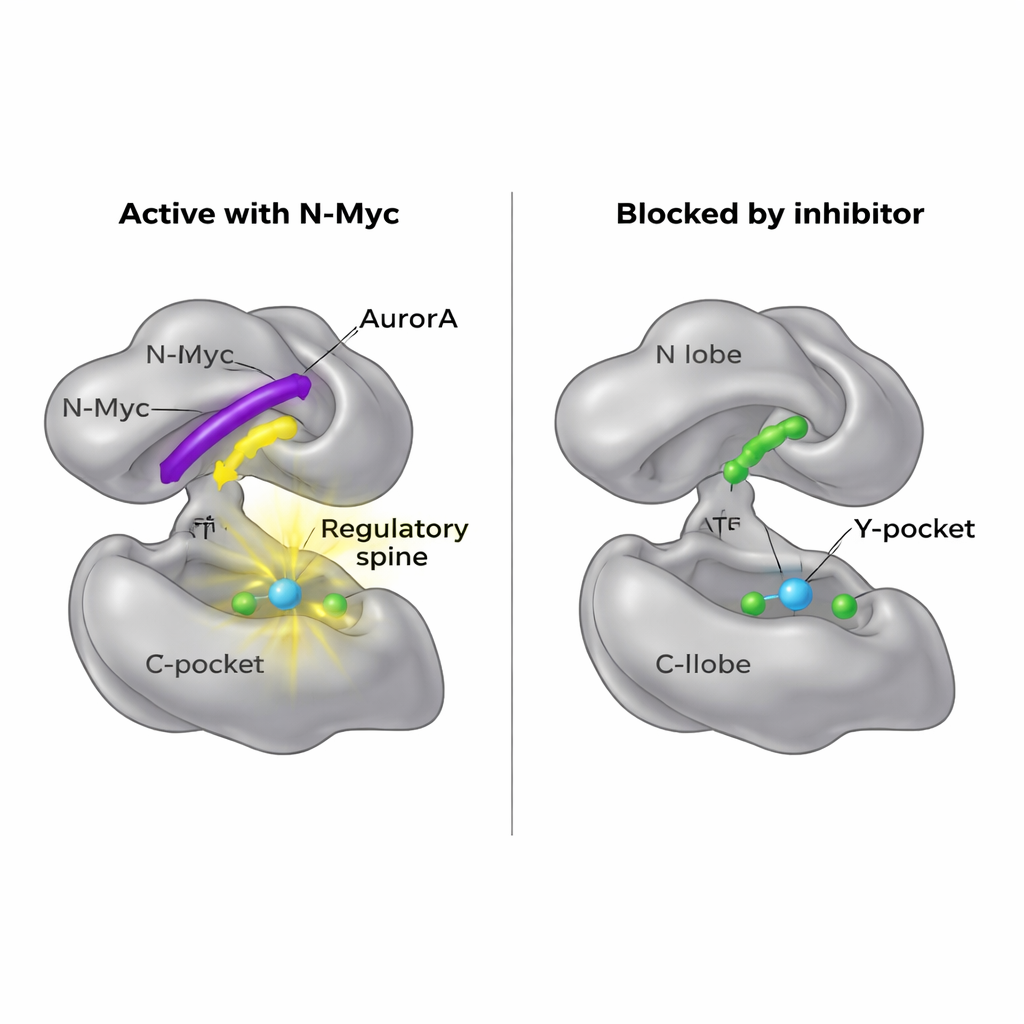
فتح منفذ دوائي جديد
نظرًا لصعوبة استهداف N-Myc ذاته دوائيًا، تساءل الباحثون عما إذا كان بالإمكان بدلاً من ذلك حجب موقع ارتباطه على AurA. كشفت خرائطهم الهيكلية أن MB0 وMBI تشغلان نفس المنطقة العامة في الفص الأمامي التي يستخدمها بروتين شريك آخر، TPX2، لتنشيط AurA. ومن المعروف أن جزيئًا صغيرًا يسمى AurkinA يحشر نفسه في الجيب Y ويزحزح TPX2. في تجارب الارتباط، نافس AurkinA بفعالية N-Myc على الفص الأمامي لـ AurA أيضًا، مانعًا ارتباط شِظايا N-Myc1–69 وN-Myc1–100. يُظهر هذا أن سطح الفص الأمامي، وخاصة الجيب Y، هو بقعة صالحة للاستهداف الدوائي تتحكم ليس فقط في منظمات تقليدية مثل TPX2 بل أيضًا في بروتينات سرطانية مضطربة الجوهر مثل N-Myc.
ما معنى هذا للعلاجات المستقبلية
تعيد هذه الدراسة تأطير شراكة N-Myc–AurA كمحضن ديناميكي متعدد التماس متركز حول الفص الأمامي لـ AurA، بدلًا من أن يكون موقع ارتباط جامدًا واحدًا. للقراء غير المتخصصين، الرسالة الأساسية هي أن بروتينًا سرطانيًا بلا شكل ثابت مثل N-Myc يمكن التعامل معه بشكل غير مباشر عن طريق استهداف رقعة راسية على إنزيمه الشريكي. من خلال إظهار أن المركبات الموجودة التي ترتبط بالفص الأمامي قادرة على إبعاد N-Myc عن AurA، تفتح الدراسة طريقًا واضحًا نحو أدوية تعطل هذه التفاعلات بشكل انتقائي. قد تُضعف مثل هذه العوامل دعمًا حاسمًا لـ N-Myc في أورام الأطفال عالية المخاطر وتوفر، مع تطوير إضافي، مسار علاج جديدًا لأسراب من السرطانات التي اعتُبرت طويلاً «غير قابلة للعلاج».
الاستشهاد: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
الكلمات المفتاحية: N-Myc, Aurora kinase A, بروتينات مضطربة جوهريًا, ورم عصبي نخاعي, مثبطات تداخل البروتين–بالبروتين