Clear Sky Science · ar
أدوية محبوسة داخل مركب دوائي تتيح فك التقييد الضوئي المتزامن لأكسيد النيتريك والمخدرات لتسكين جراثيمي
مكافحة الجراثيم والألم معاً
العدوى البكتيرية لا تهدد صحتنا فحسب؛ بل تسبب أيضاً ألماً شديداً. العلاجات التقليدية عادة تستهدف الجراثيم لكنها تترك المرضى يعتمدون على مسكنات منفصلة قد تنتهي مفعولها بسرعة أو تسبب آثاراً جانبية. تقدم هذه الدراسة دواءً يتحكم به الضوء يهدف إلى قتل البكتيريا وتخفيف الألم في خطوة موحّدة ومنسقة، مقدماً لمحة عن رعاية عدوى أذكى وأكثر راحة.
فكرة دواءً مزدوج الوظيفة
بنى الباحثون منهجهم حول التتركاين، مخدر موضعي مألوف يُستخدم لتخدير الجلد والأعصاب. ربطوا كيميائياً أكسيد النيتريك، جزيء غازي صغير معروف بخصائصه القوية المضادة للبكتيريا والمضادة للالتهاب، بالتتركاين. وبهذا تشكّل «بريدروج» اسمه TTC-NO يكون خاملاً إلى حد كبير حتى يتم تفعيله. ثم جُهِز TTC-NO مع جزيء مساعد حساس للضوء داخل فقاعات بوليمرية دقيقة تُدعى ميصِلات يمكنها التنقّل في بيئات مائية مثل الدم أو سائل الأنسجة. 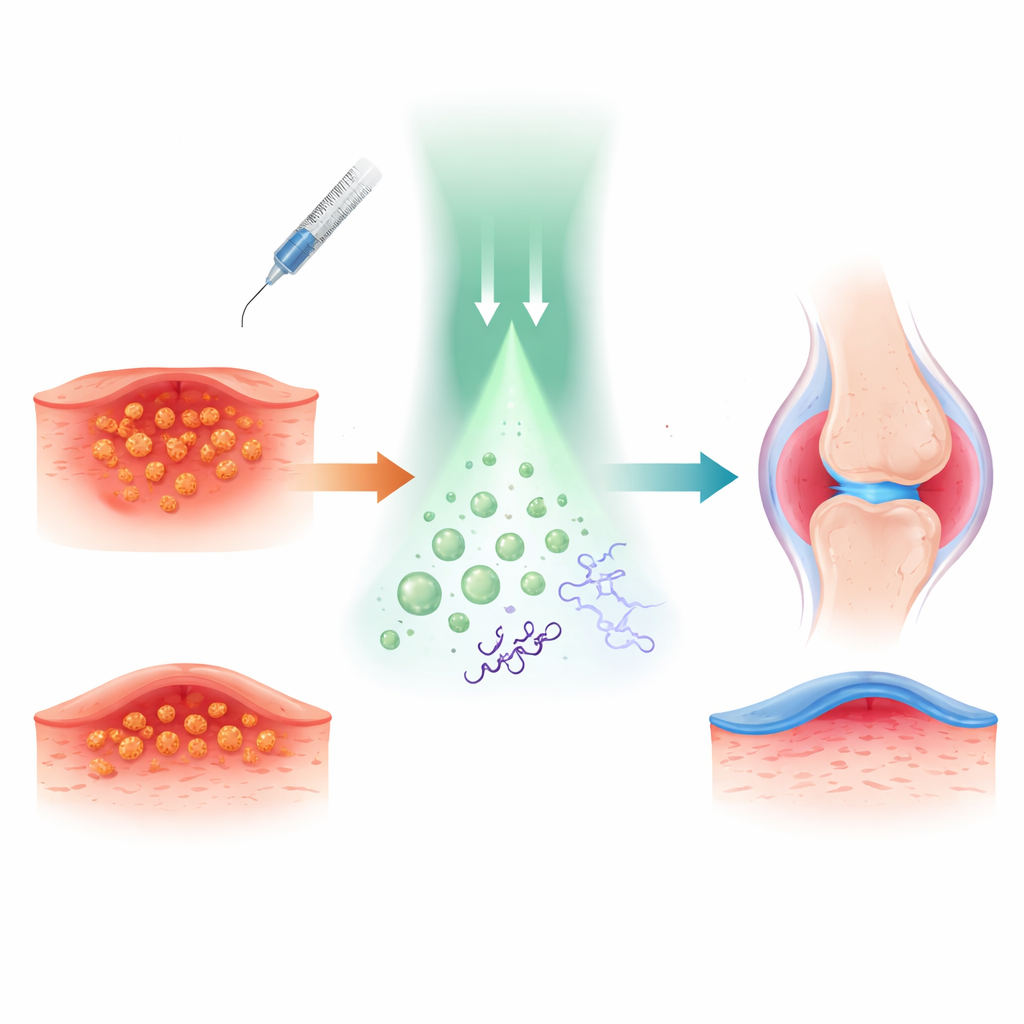
تشغيل الدواء بضوء لطيف
لفهم كيفية عمل مفتاح الضوء هذا، درس الفريق الكيمياء في المحلول. أظهروا أن فوتوكاتاليست قائم على الإريديوم يمكنه نقل إلكترون إلى TTC-NO عند تعرضه للضوء الأخضر. يؤدي ذلك إلى إضعاف رابطة محددة، مما يحرر أكسيد النيتريك ويعيد التتركاين إلى صورته الفعّالة. أكدّت قياسات باستخدام الطيفية والكروماتوغرافيا أن TTC-NO يتحول تقريباً بالكامل إلى تتركاين وأكسيد النيتريك تحت هذه الشروط، بينما يبقى دون تغيير أساساً في الظلام. عندما حُوصرت المادتان داخل الميصِلات، بقيت الجسيمات مستقرة بحجم يقارب 80 نانومتراً، ولم تُطلَق محتوياتها إلا عند الإشعاع، مما يثبت أن مفهوم «دواء محبوس داخل دواء» يمكن التحكم به من خارج الجسم بواسطة الضوء.
مساعدة جروح المصابة على الالتئام بشكل أسرع
انتقل الفريق بعد ذلك إلى فئران ذات جروح جلدية أُصيبت عمداً بالمكورات العنقودية الذهبية المقاومة للميثيسيلين (MRSA)، وهي جرثومة إشكالية في المستشفيات. تلقت بعض الجروح علاجات معيارية مثل مضاد حيوي أو عامل نمو، بينما عولجت أخرى بميصِلات TTC-NO، مع أو بدون ضوء. عند تشغيل الضوء، قلّل نظام TTC-NO بشكل حاد عدد البكتيريا، هدّأ الالتهاب، شجع نمو أوعية دموية جديدة، وعزّز ترسيب الكولاجين، وكلها أمور أساسية للالتئام السليم. أغلقت الجروح المعالجة بهذه الطريقة أسرع وأكثر اكتمالاً من تلك التي أعطيت تتركاين وحده أو الميصِلات المحفوظة في الظلام، وكانت نتائجها قابلة للمقارنة مع مضاد حيوي في مقدمة العِلاج. والأهم أن فحوصات السلامة لم تظهر أضراراً كبيرة للأعضاء أو كيمياء الدم.
تخفيف الألم وتهدئة إشارات الأعصاب
لأن العدوى وإصابة الأنسجة تنشّط مسارات الألم بشدة، قاس العلماء بعناية سلوكيات مرتبطة بالألم في نفس نموذج الجرح. رفع التتركاين التقليدي مؤقتاً القوة المطلوبة لتحفيز استجابة ألم لكنه زال خلال ساعات قليلة. بالمقابل، وفّرت ميصِلات TTC-NO المفعلة بالضوء تخفيفاً للألم يستمر حتى 12 ساعة. كشفت دراسات مجهرية لعقد عصبية قرب الحبل الشوكي وتسجيلات نشاط في قشرة الإحساس في الدماغ أن العلاج المدمج قلّل من إطلاق أعصاب الإحساس بالألم طويلة بعد فناء تأثير التتركاين النقي. أشارت تجارب إضافية إلى أن طول مدة الفعالية الإضافية يعود إلى خفض الحمل البكتيري والالتهاب بواسطة أكسيد النيتريك، وليس فقط إلى تخدير الأعصاب.
حماية المفاصل المؤلمة المصابة
اختبر الباحثون النظام أيضاً في فئران تعاني من التهاب مفاصل قيحي، عدوى شديدة بالمكورات المقاومة داخل مفصل الركبة تسبب تورماً وفقداناً للعظم وألماً شديداً. قلّلت ميصِلات TTC-NO المفعلة بالضوء عرض المفصل، خفضت أعداد البكتيريا، وحمت بنية العظم كما ظهر في فحوصات مسح عالية الدقة. انخفضت مستويات جزيئات الالتهاب الضارة في الدم، بينما ارتفعت جزيئات الإشارة الواقية. سلوكياً، استطاعت الفئران المعالجة تحمل ضغط ميكانيكي أقوى على المخلب المصاب وتحركت بحرية أكبر في ساحة مفتوحة، ما دلّ مجدداً على تخفيف ألم طويل الأمد مقارنة بالتتركاين وحده. عكست قياسات الأعصاب والدماغ هذه المكاسب السلوكية، مشيرة إلى كبح واسع لمسارات الألم دون سُمّية محلية أو جهازية واضحة. 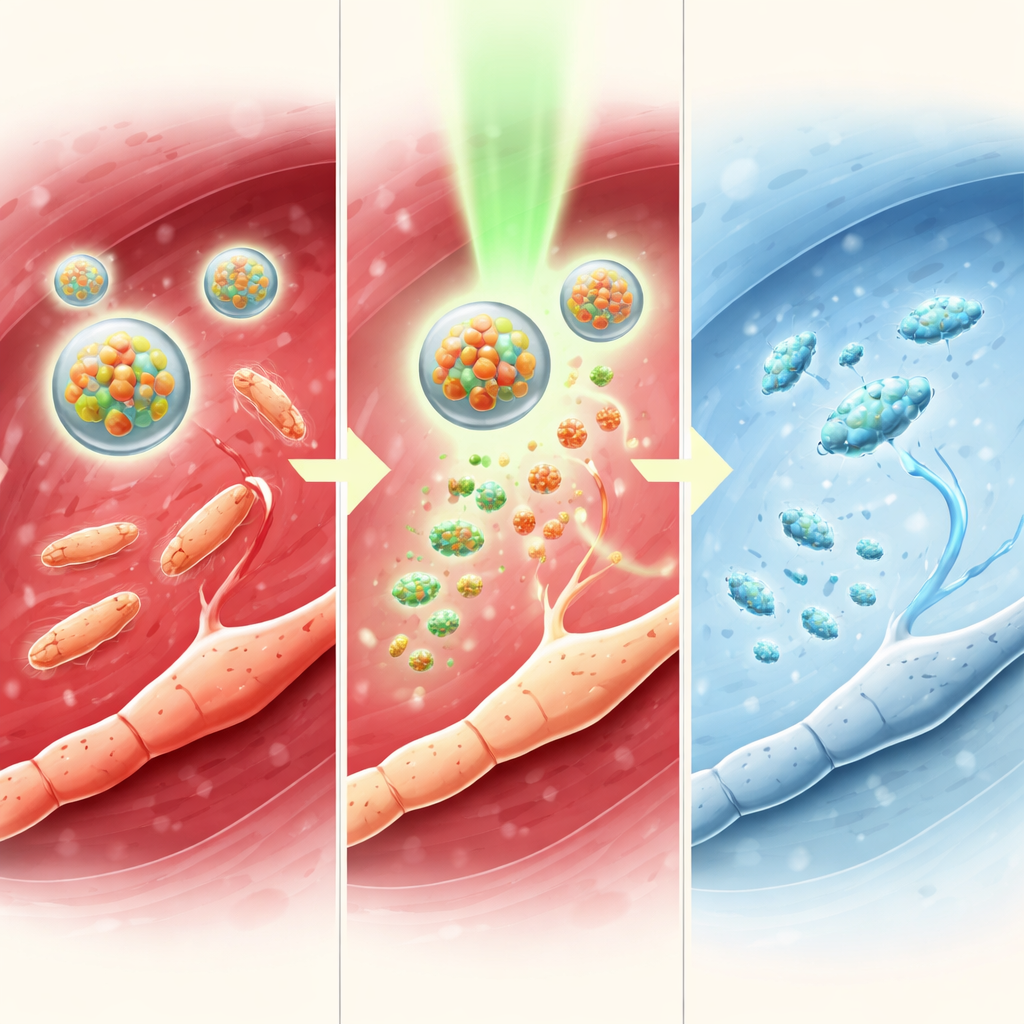
ماذا قد يعني هذا للمرضى
مجتمعة، تُظهر النتائج نظاماً نانويّاً واحداً مفعل بالضوء يمكنه كلاً من إزالة العدوى البكتيرية المستعصية وتقليل الألم المرتبط بها بشكل كبير. من خلال «حبس» مخدر كيميائياً داخل بنية مطلِقة لأكسيد النيتريك وتغليفه في ميصِلات، يحقق المؤلفون إطلاقاً محلياً ومؤقتاً لمادتين مفيدتين عند الطلب باستخدام ضوء مرئي لطيف. في نماذج حيوانية للجروح الجلدية وعدوى المفاصل، يسرّع هذا التصميم الشفاء ويمدّد تخفيف الألم إلى ما هو أبعد مما يقدمه المخدر الموضعي التقليدي. ورغم أنّه لا يزال أمامه الكثير من الاختبارات قبل الاستخدام البشري، تبرز الدراسة كيف أن الأدوية الذكية والقابلة للتبديل قد تجعل علاجات العدوى في يومٍ ما أكثر فعالية وراحة.
الاستشهاد: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
الكلمات المفتاحية: علاج بأكسيد النيتريك, أدوية مفعّلة بالضوء, تسكين ألم ضد البكتيريا, طب نانوي, التهابات MRSA