Clear Sky Science · ar
جذب مزدوج لجزيئيْن من CCM2 إلى KRIT1 يكبح التعبير عن KLF4
لماذا تحتاج أوعية الدم في الدماغ إلى رقابة دقيقة
تسير أوعية الدم في الدماغ على حبلٍ رفيع: يجب أن تكون قوية بما يكفي لعدم التسرب، وفي الوقت نفسه مرنة للاستجابة لاحتياجات الجسم. عندما يفشل هذا التوازن، قد يتكوّن لدى الأشخاص تشوّهات كهفية دماغية — مجموعات من الأوعية الدموية الهشة على شكل فقاعات قد تنزف وتسبب نوبات صرع أو سكتات. تكشف هذه الدراسة عن مصافحة جزيئية غير معروفة سابقًا بين ثلاثة بروتينات تساعد على إدامة استقرار الأوعية الدماغية، وتبيّن كيف أن كسر هذه المصافحة يمكن أن يقود إلى المرض.
حراس صحة الأوعية
تعتمد الخلايا الباطنة للأوعية الدموية على مجموعة من مفاتيح التحكم الرئيسية، تُدعى KLF2 وKLF4، للتحكم في الجينات التي تحافظ على قوة وهوية الأوعية. إذا ارتفعت فعالية هذه المفاتيح كثيرًا، تصبح الأوعية غير طبيعية ومعرضة للتلف. يُعرف بروتينان آخران، KRIT1 وCCM2، بكونهما يحرسان هذا النظام. الأشخاص الذين يرثون نسخًا معطوبة من أيٍّ منهما يكونون في خطر مرتفع للإصابة بالتشوّهات الكهفية الدماغية. ومع ذلك، لم يفهم العلماء حتى الآن بالضبط كيف يتعاون KRIT1 وCCM2 للتحكم في KLF4.
فريق مكوّن من ثلاثة — مفاجأة
استخدم الباحثون خلايا شبيهة بالخلايا الباطنة البشرية المزروعة في المختبر وخفّضوا بشكل انتقائي كمية CCM2 أو KRIT1 باستخدام أدوات جينية. عندما نُزعت أي من البروتينين، ارتفعت مستويات KLF4 بشكل كبير، بما يتناغم مع ما يُرى في نماذج حيوانية والمرضى. أعاد استعادة CCM2 أو KRIT1 الطبيعيين KLF4 إلى مستوياته، لكن فقط إذا كانت البروتينات المستعادة لا تزال قادرة على الالتصاق ببعضها. من خلال هندسة تغييرات دقيقة في المناطق التي تتفاعل فيها CCM2 وKRIT1، أظهر الفريق أن هذا الاتصال الفيزيائي ضروري لمنع ارتفاع KLF4. تضع هذه التجارب شراكة KRIT1–CCM2 في صميم نظام التحكم بهذا العامل النسخي القوي.
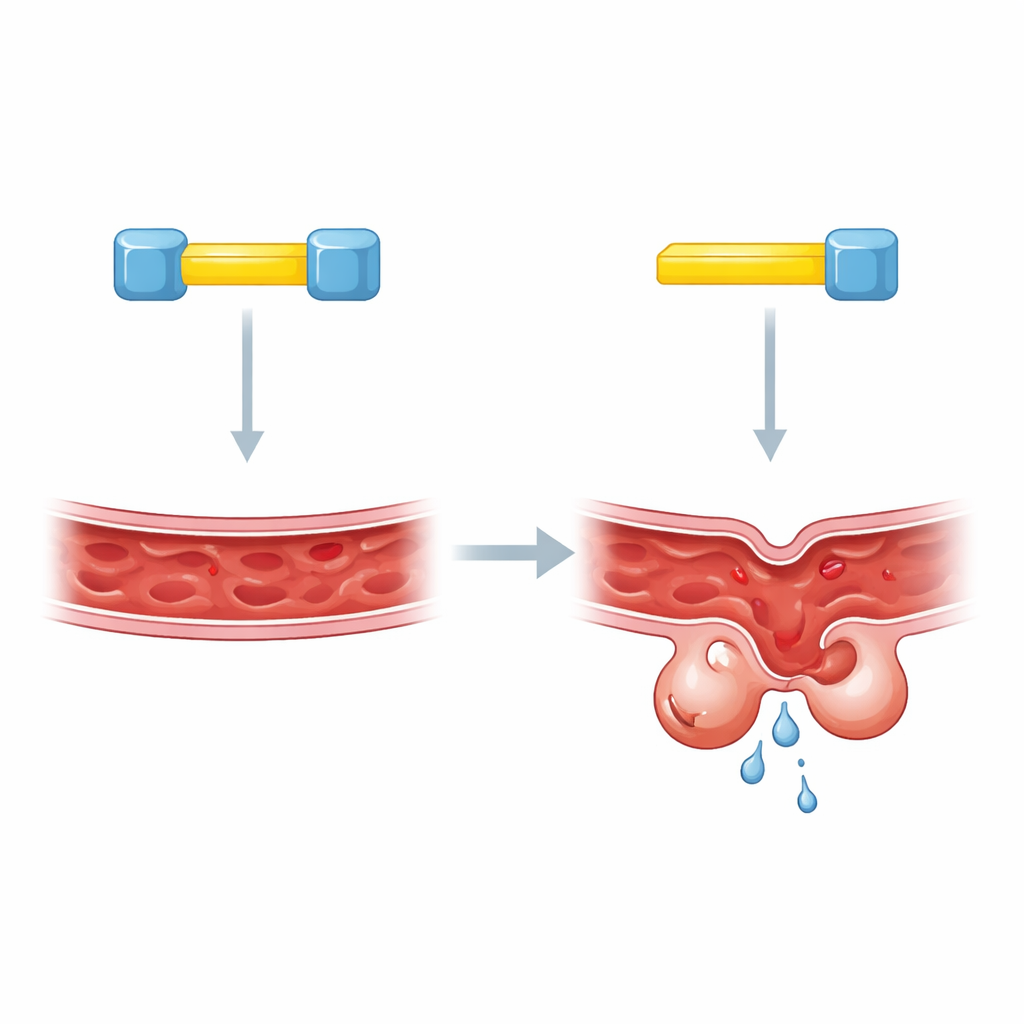
قفلان على مفتاح واحد
للتعمق أكثر، ركز المؤلفون على مقاطع قصيرة داخل KRIT1 تعمل كمواقع رسو جزيئية. أشارت أعمال سابقة إلى أن CCM2 يرتبط بـ KRIT1 عند أحد هذه المواقع، لكن طرقًا مختلفة أعطت إجابات متضاربة حول أي موقع بالضبط. تكشف الدراسة الجديدة أن الالتباس نشأ لأن الصورة الحقيقية أكثر تعقيدًا: يحمل KRIT1 موقعين رسوّ متقاربين، وكلاهما مطلوبان. عندما تعطّل أي من الموقعين، ظل مستوى KLF4 مرتفعًا بشكل غير طبيعي، تمامًا كما لو كان KRIT1 مفقودًا تمامًا. أظهرت اختبارات كيميائية حيوية في خلايا مهندسة أن بروتين KRIT1 واحدًا يمكنه أن يربط جزيئيْ CCM2 منفصلين في آن واحد، مما يشير إلى تجمّع ثلاثي غير متوقع.
رؤية المشبك الجزيئي بتفصيل أدق
نقّى الفريق لاحقًا أجزاءً ذات صلة من CCM2 وKRIT1 وفحص كيف تتجمع في المحلول وفي البلّورات. أشارت قياسات كتلة المجمع إلى أن نسختيْن من منطقة رئيسية في CCM2 ترتبطان بشريط واحد من KRIT1 يحمل زوج مواقع الرسو. أكدت لقطات بنيوية عالية الدقة هذا الترتيب 2:1: يخترق ببتيد KRIT1 ممتد بين نطاقيْ CCM2، مع تأصّل كل موقع رسو في جيب مماثل على جزيء CCM2 مختلف. يساعد مقطع حلزوني قصير بين مواقع الرسو في وضع نطاقيْ CCM2 جنبًا إلى جنب، مكونًا بنية مُناسبة تشبه المشبك. لم يُسجل من قبل لمثل هذه العائلة من وحدات البروتين هذا النوع من الارتباط المزدوج — نطاقيْ ارتباط يقفلان على مواقع متتالية على شريك واحد.
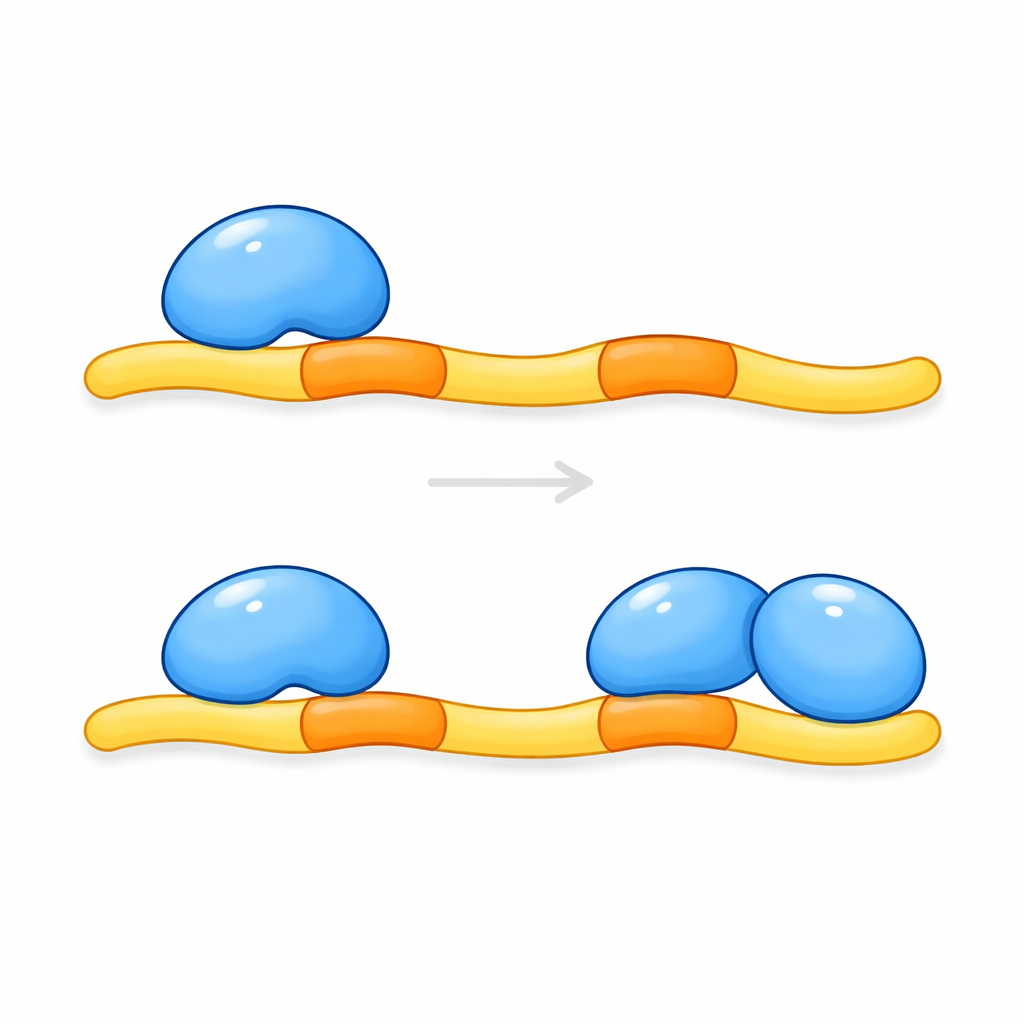
دلالات للمرض الدماغي وما بعده
تبيّن هذه النتائج أن KRIT1 لا يقتصر على ربط جزيء CCM2 واحد فقط؛ بل يعمل كركيزة تستقطب زوجًا من بروتينات CCM2. فقط عندما تُشغَل موقعي الرسو الاثنين على KRIT1 يمكن للمجمع أن يقيد إنتاج KLF4 بشكل صحيح ومن ثم يساهم في منع نمو أوعية هشة. لذا فإن الطفرات في KRIT1 التي تعطل أيًا من موقعي الرسو من المتوقع أن تضعف هذا المشبك الوقائي وقد تفسر بعض أشكال التشوّهات الكهفية الموروثة. ونظرًا لأن العديد من البروتينات البشرية الأخرى تحمل دواعم رسو مزدوجة مماثلة، فإن هذه الدراسة تلمّح أيضًا إلى مبدأ أوسع: قد يكون الارتباط المزدوج بواسطة أزواج من النطاقات ذات الصلة طريقة شائعة تضبط بها الخلايا شبكات الإشارة. إن فهم هذا التفاعل الثلاثي الشركاء قد يوجّه في نهاية المطاف استراتيجيات لتثبيت الأوعية الدموية لدى الأشخاص المعرضين لخطر النزف الدماغي.
الاستشهاد: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
الكلمات المفتاحية: تشوّهات الكهف الدماغية, الخلايا البطانية, KRIT1, CCM2, KLF4