Clear Sky Science · ar
أجسام مضادة صغيرة (نانوبودي) مبنية على IgG تثبطان في آنٍ واحد النشاط التحسسي والإنزيمي للمسبب المهيمن في سم نحلة العسل
لماذا تهم حساسية لسعة النحل
بالنسبة لمعظم الناس، تكون لسعة نحلة العسل مؤلمة لكنها قصيرة الأمد. بالنسبة لآخرين، يمكن أن تُحفّز رد فعل مهدد للحياة يشمل الجسم بأكمله يُسمى التأقن (anaphylaxis). العلاج الوقائي الرئيسي الحالي، وهو التحسيس بعلاج السم (venom immunotherapy)، ينجح مع كثير من المرضى لكنه يستغرق سنوات، ويتطلب حقنًا متكررة، وقد يسبب بدوره آثارًا جانبية تحسسية. تستكشف هذه الدراسة طريقة جديدة وأكثر تحديدًا لحماية الأشخاص شديدة الحساسية لسم نحلة العسل عن طريق تعطيل مكوّن سمّي رئيسي قبل أن يسبب الضرر.
المخلّ المشكلة الرئيسي في سم النحل
سم نحلة العسل مزيج من جزيئات مختلفة، لكن بروتينًا واحدًا يُدعى فوسفوليباز A2 (أو Api m 1) يبرز بوصفه المستأجر المهيمن. إنه المسبب التحسسي الرئيسي لمرضى حساسية نحلة العسل وموجود تقريبًا لدى جميعهم. لـ Api m 1 دور مزدوج: يَتلف أغشية الخلايا، مساهماً في الألم والالتهاب في موضع اللدغة، كما أنه هدف أساسي للأجسام المضادة المسببة للحساسية المعروفة باسم IgE. عندما يرتبط Api m 1 بـ IgE المثبت على خلايا المناعة مثل الخلايا البدينة والقاعديات، يمكن أن يحدث سلسلة من التفاعلات تؤدي إلى الإفراز المفاجئ للمواد الالتهابية وفي الحالات الشديدة إلى التأقن.
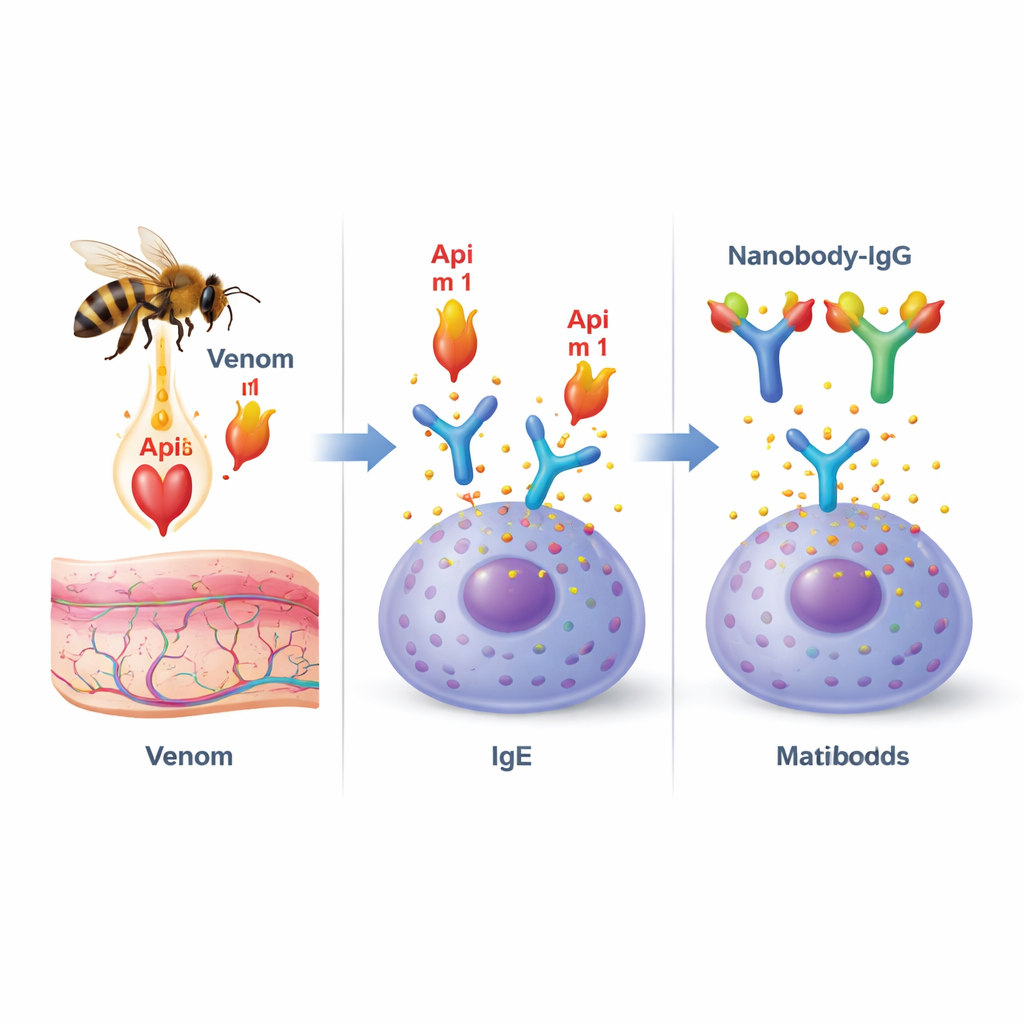
تصميم أجسام مضادة صغيرة لحجب المسبّب
توجّه الباحثون إلى "نانوبوديز"، وهي شظايا أجسام مضادة صغيرة ومستقرة اكتشفت في الأصل في حيوانات الجماليات (camélid). وبسبب صغر حجمها وشكلها الممدود، تُعد النانوبوديز جيدة بشكل خاص في الانزلاق إلى الأخدودات والجيوب على سطح البروتينات. عزل الفريق نانوبوديز محددة لـ Api m 1 من مكتبة مناعية واختار اثنين من المرشحين المتميزين، سُمّيا AM1‑1 وAM1‑4. أظهر العمل البنيوي التفصيلي باستخدام البلورة بالأشعة السينية أن هذين النانوبودين يثبّتان على جانبي Api m 1 المتقابلين ولا يتداخلان مع بعضهما. يجلس أحد النانوبوديز، AM1‑1، مباشرة فوق المركز النشط للإنزيم، مما يوحي بأنه قد يمنع وظيفة Api m 1 المسببة لتلف الأغشية، بينما يَرست AM1‑4 في جيب منفصل على سطح البروتين.
تحويل النانوبوديز إلى حاجزين فعّالين
لتحويل هذه الرابطات الصغيرة إلى أدوية طويلة الأمد، قام العلماء بربط كل نانوبودي بقطعة الذيل (منطقة Fc) من IgG1 البشري، مكونين جزيئات تشبه الأجسام المضادة الأكبر ذات ثبات أفضل في مجرى الدم. كما هندسوا نسخة "ثنائية التخصص" تحمل كلًا من AM1‑1 وAM1‑4 في جزيء واحد شبيه بـ IgG. أظهرت الاختبارات المعملية أن هذه الاندماجات نانوبودي‑IgG تلتصق بـ Api m 1 بألفة عالية جدًا، وعندما تكون حاضرة، يمكنها تقليل ارتباط IgE من دم مرضى حساسية نحلة العسل بـ Api m 1 بشكل قوي. في تجارب خلوية، قللت هذه الاندماجات من تنشيط القاعديات، خلايا المناعة التي تستجيب عادةً بقوة عند تعرضها لـ Api m 1 في الأفراد التحسسيين.
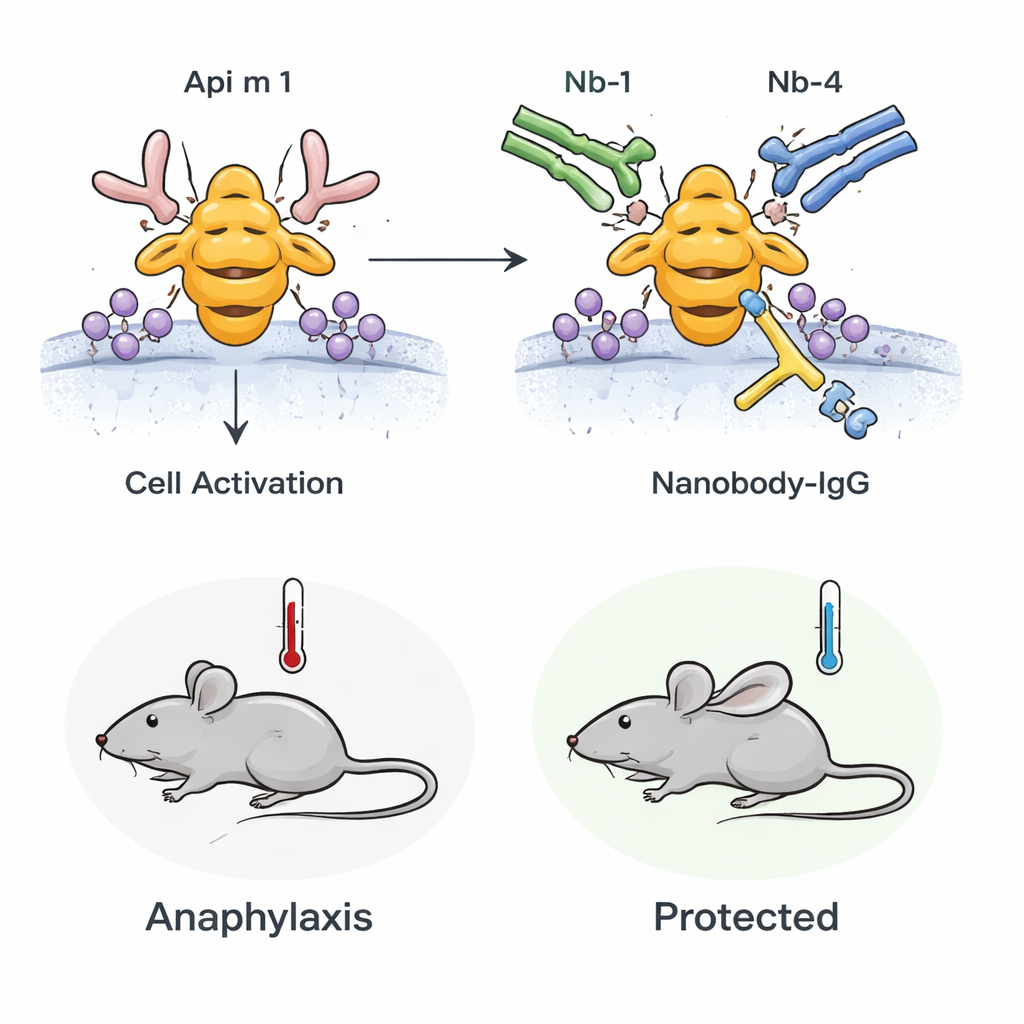
من الأنابيب إلى الكائنات الحية
سأل الفريق بعد ذلك عما إذا كان هذا التأثير الحاجب سيصمد في كائن حي. استخدموا فئرانًا مُحسَّسة لسم نحلة العسل بحيث تتفاعل أجهزتها المناعية مع Api m 1 بطريقة تحاكي الحساسية البشرية. عندما تعرضت هذه الفئران لتحدٍ بمادة Api m 1، طوّرت علامات التأقن بما في ذلك انخفاض درجة حرارة الجسم ومؤشرات تنشيط الخلايا البدينة في الدم. ومع ذلك، إذا نُسّقت الفئران بعلاج مُسبق بالنانوبودي‑IgG ثنائي التخصص، فقد تقلص كل من انخفاض الحرارة وتنشيط الخلايا البدينة بشكل ملحوظ. يبرهن هذا أن أجسامًا مانعة مسبقة الوجود وذات ألفة عالية يمكنها خفض الاستجابة التحسسية الجهازية لـ Api m 1 في الجسم الحي.
ماذا قد يعني هذا للأشخاص المصابين بحساسية سم النحل
تُظهر الدراسة مجتمعة أن جزيئات IgG المبنية بعناية على أساس نانوبودي قادرة على حجب الأعمال التحسسية والإنزيمية لـ Api m 1، المسبب الرئيسي في حساسية سم نحلة العسل، في آن واحد. بالنسبة للمرضى، يفتح هذا الاحتمال أمام تحصين سلبي موسمي: بضع حقن من مثل هذه الأجسام المضادة خلال الأشهر التي تكثر فيها لسعات النحل قد توفر حماية مؤقتة من التفاعلات الشديدة، دون الالتزام الطويل والمخاطر المرتبطة بالعلاج التقليدي بالتحسيس بالسم. وبينما هناك حاجة إلى مزيد من العمل لتوسيع النهج ليشمل مكونات سمية أخرى ولتفحص السلامة والفعالية في البشر، فإن استراتيجية النانوبودي هذه تقدم وسيلة دقيقة جديدة لحماية الأفراد المعرضين للخطر من لسعات النحل الخطرة.
الاستشهاد: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
الكلمات المفتاحية: حساسية سم النحل, نانوبوديز, المناعَة السلبية العلاجية, فوسفوليباز A2, الوقاية من التأقُّن