Clear Sky Science · ar
كثافة شحنة المعدن المائي كواصف عالمي يشرح اختلافات الآليات في تنشيط البيريودات لتحلل الملوثات
تنظيف المياه بكيمياء ذكية
تتسلل العديد من الأدوية والمواد الكيميائية الصناعية عبر محطات معالجة المياه التقليدية وتصل إلى الأنهار وماء الشرب. تستكشف هذه الدراسة طريقة واعدة لتحطيم مثل هذه الملوثات عن طريق عامل مؤكسد شائع، البيريودات، وتُظهر أن خاصية بسيطة لأيونات المعادن في الماء يمكنها التنبؤ بمدى—وكيفية—عمل هذه الكيمياء بأمان وكفاءة. فهم هذه القاعدة قد يساعد المهندسين في تصميم نظم معالجة أنظف وأكثر فعالية لمياههاتِ العالم الواقعي المختلفة.
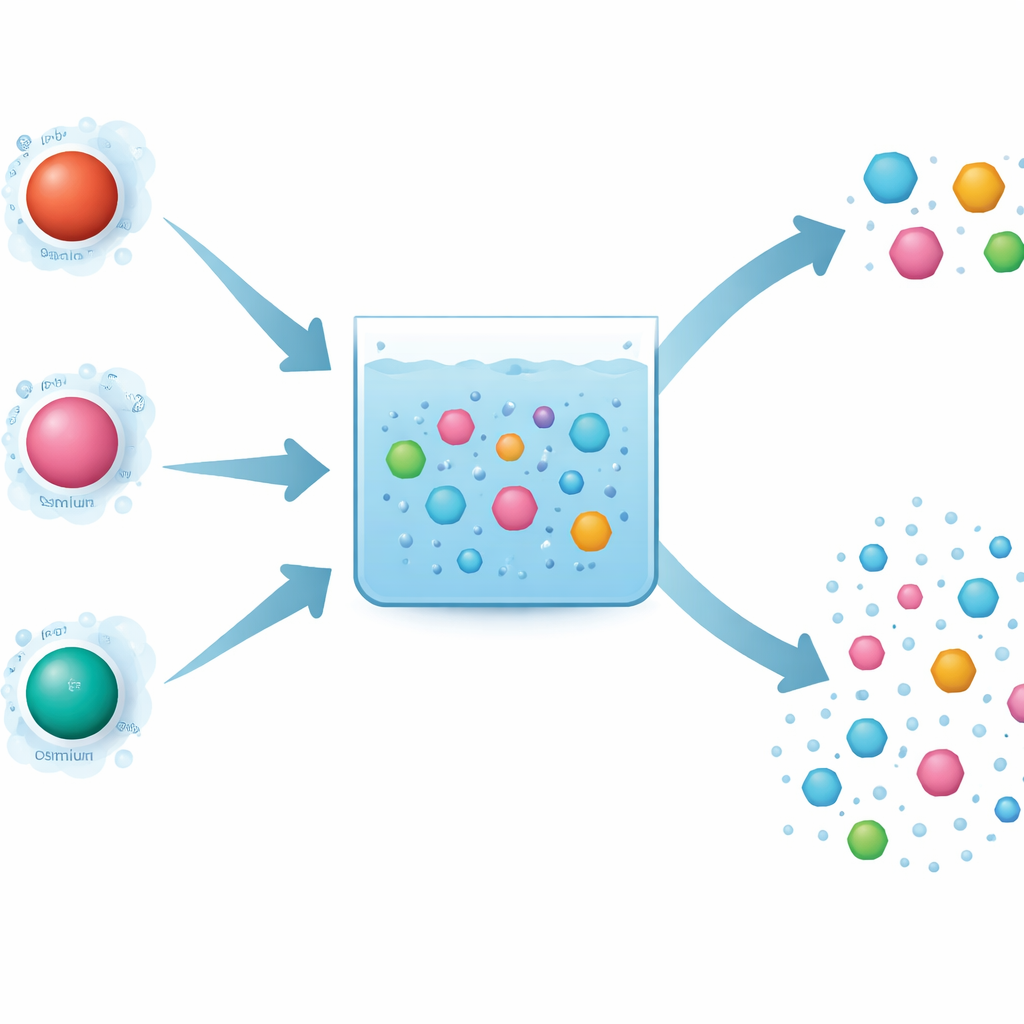
لماذا يهم اختيار المعدن في تحلل الملوثات
تستخدم عمليات الأكسدة المتقدمة أنواعاً تفاعلية قوية لتفكيك الجزيئات العضوية. البيريودات هو أحد هذه المواد المؤكسدة، ويمكن «تفعيله» بواسطة أيونات المعادن المذابة. قارن المؤلفون ثلاثة معادن قريبة الصلة—الحديد، الروثينيوم، والأوزميوم—التي تنتمي إلى نفس عمود الجدول الدوري وقد يُتوقع أن تتصرف بشكل مماثل. يمكن لجميعها تنشيط البيريودات والمساعدة في تدمير ملوث اختبار، الكاربامازيبين. ومع ذلك أظهرت التجارب اختلافات لافتة: عمل الروثينيوم بسرعة كبيرة، كان الحديد أبطأ، وجاء الأوزميوم في المنتصف. والأمر الأكثر إرباكاً أن الأوزميوم أزال مجموعة واسعة من الملوثات دون تحيز كبير، بينما كان الحديد والروثينيوم انتقائيين، مهاجمين بعض المركبات بسهولة أكبر بكثير من غيرها.
مساران كيميائيان مختلفان جداً
لفهم ما وراء هذه الفروق، تتبع الفريق أنواع المؤكسدات قصيرة العمر التي ظهرت في كل نظام معدن–بيريودات. مع الحديد والروثينيوم، كانت الوحدات السائدة هي «معدن–أكسجين» التي تعمل كأدوات دقيقة، ناقلة ذرة أكسجين مباشرة إلى مواقع محددة على الملوث. كانت هذه المسارات تميل إلى تكوين منتجات إبكسيد—هياكل حلقيّة تضيف ذرة أكسجين واحدة—مما يدل على أن التفاعل انتقائي إلى حد ما. في نظام الأوزميوم، مع ذلك، كان الفاعلون الرئيسيون هم جذور الهيدروكسيل، وشظايا شديدة التفاعل تهاجم أي جزيء عضوي قريب تقريباً، مما يؤدي إلى منتجات مهدرجة بالأكسجين وشظايا صغيرة ناتجة عن فتح الحلقات. أكدت الاختبارات باستخدام مجسات كيميائية وطيفية التقاط الدوران أن جذور الهيدروكسيل والأنواع المؤكسدة الأكسجينية المرتبطة بها، وليس وحدات أوزميوم–أكسجين ذات التكافؤ العالي، هي التي تقود معظم تدمير الملوثات عندما يكون الأوزميوم موجوداً.
كيف تشكّل شروط المياه التفاعلات
فحص الفريق أيضاً كيف يؤثر الرقم الهيدروجيني ومكونات المياه الطبيعية على هذه العمليات. بالنسبة للأوزميوم، ازداد إزالة الملوثات مع قلوية الماء، حيث يجعل تنسيق أيونات الهيدروكسيد الإضافية حول المعدن من الأسهل تحرك الإلكترونات وتكوّن الجذور. ومع ذلك، عند جرعات عالية من المعدن أو المؤكسد، يختنق نظام الأوزميوم «ذاتيًا» حيث تُمسح الجذور الجديدة بمواد زائدة بدل أن تتفاعل مع الملوثات. كان للمادة العضوية الطبيعية، التي كثيراً ما تتداخل مع تفاعلات الأكسدة، تأثير ضئيل بشكل مدهش على تحلل المدفوع بالأوزميوم، مما يوحي بأن مسار الجذور يظل قوياً في المياه الواقعية. بالمقابل، عمل الحديد والروثينيوم بأفضل صورة في الشروط الحمضية، وكبتت المادة العضوية الطبيعية نشاطهما بقوة عن طريق امتصاص مؤكسدات المعدن–الأكسجين الأساسية.
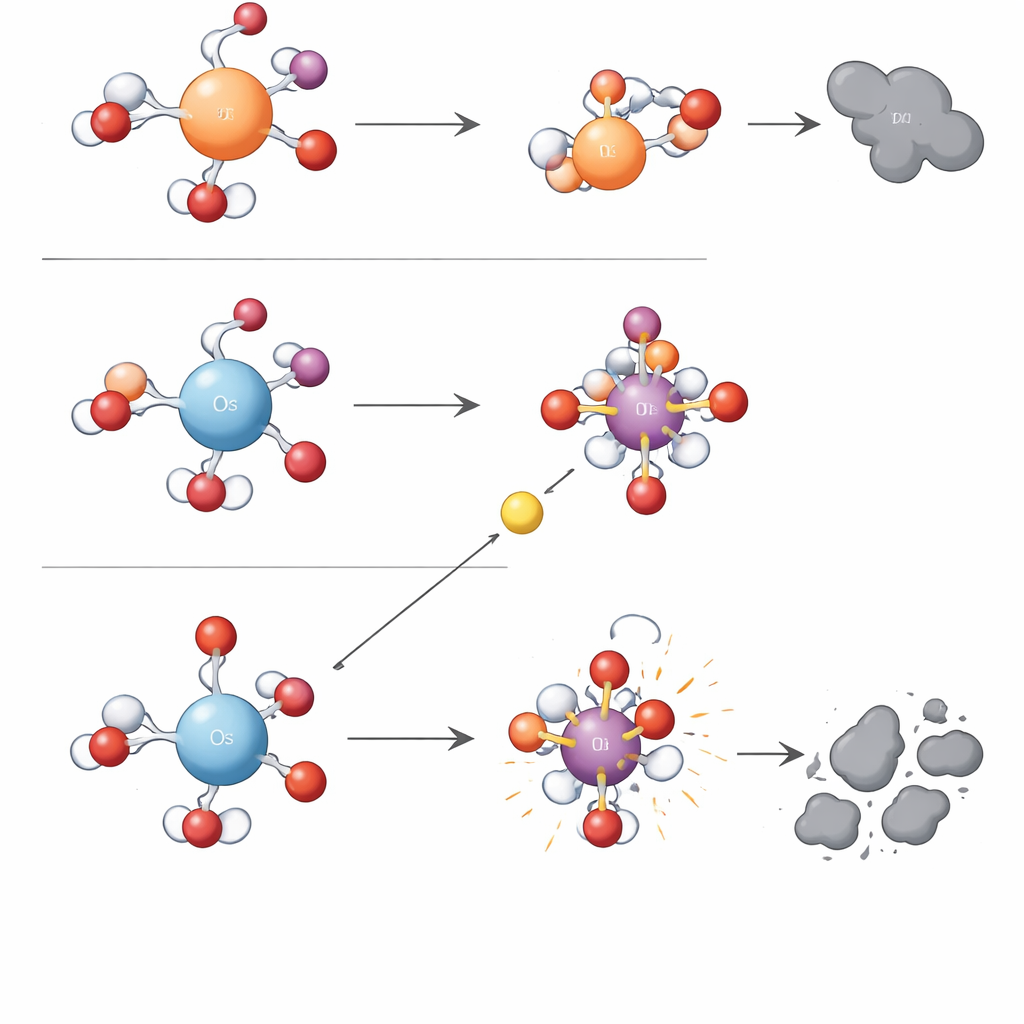
قاعدة شحنة بسيطة وراء كيمياء معقدة
للانتقال بعيداً عن التجربة والخطأ، لجأ الباحثون إلى حسابات كميّة‑كيميائية. وجدوا أن ميزة إلكترونية واحدة—كثافة الشحنة الموجبة لمركز المعدن المائي—يمكنها تفسير الانقسام بين نوعي التفاعل. يحمل الأوزميوم في الماء شحنة موجبة مركزة أعلى من الحديد أو الروثينيوم. هذا المركز الموجب القوي يلتصق بشدة بذرة الأكسجين المرتبطة به، مما يجعل وحدة المعدن–أكسجين مستقرة لكن متمهلة في نقل الأكسجين المباشر. في الوقت نفسه، يخفض السحب القوي على جزيئات الماء والأيونات حاجز الطاقة للخطوات أحادية الإلكترون التي تكسر في النهاية رابطة الأكسجين في البيريودات وتطلق جذور الهيدروكسيل. المعادن ذات كثافة الشحنة الأقل، مثل الحديد والروثينيوم، تحتفظ بالإلكترونات أكثر إحكاماً، مما يفضّل تشكيل واستخدام مؤكسدات المعدن–الأكسجين الانتقائية بدلاً من الجذور الحرة. يسمي المؤلفون هذه الفكرة المنظمة «آلية التحكم بكثافة الشحنة»، ويُظهرون أنها تبرر أيضاً الاتجاهات المبلغ عنها لمعادن أخرى مثل المنغنيز.
تصميم معالجة مياه أفضل من خلال مقبض واحد
من خلال ربط مجموعة من الملاحظات المعقدة بواصف بسيط واحد—كثافة شحنة المعدن المحاط بالماء—يقدّم هذا العمل خريطة طريق لتخصيص عمليات الأكسدة المتقدمة. ينبغي أن تفضّل المعادن ذات كثافة الشحنة العالية التفكك الواسع القائم على الجذور للخلائط الملوثة المعقدة، لا سيما في المياه القلوية أو الغنية بالمواد العضوية. المعادن ذات كثافة الشحنة المنخفضة مناسبة أكثر عندما يكون مطلوباً أكسدة انتقائية وأقل قسوة، على سبيل المثال لتحويل ملوثات محددة دون التفاعل المفرط مع كل ما هو موجود. من الناحية العملية، يعني هذا أن الكيميائيين والمهندسين يمكنهم فحص أو تصميم محفزات لتنقية المياه عن طريق ضبط مدى تمسك مراكز المعادن بالشحنة في بيئتها المائية، بدلاً من تحسين كل نظام بالتجربة وحدها.
الاستشهاد: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
الكلمات المفتاحية: عمليات الأكسدة المتقدمة, تنشيط البيريودات, معالجة المياه, تحفيز المعادن الانتقالية, جذور الهيدروكسيل