Clear Sky Science · ar
سير عمل بروتيوميكي كيميائي عالي الإنتاجية لتوصيف ديناميكيات السيتروجينيل
لماذا يهم تغيير لبنات بناء البروتين
تُعدِّل خلايانا باستمرار سلوك البروتينات عبر إضافة تغييرات كيميائية صغيرة بعد تصنُّعها. أحد هذه التعديلات، المسمّى السيتروجينيل، يغيّر بشكل طفيف شحنة حمض أميني شائع ويمكن أن يعيد تشكيل كيفية طي البروتينات أو تلاصقها مع الحمض النووي أو تفاعلها مع جزيئات أخرى. ترتبط هذه التعديلات الصغيرة بشكل متزايد بأمراض المناعة الذاتية والالتهابات والسرطان ووظائف الدماغ—إلا أنها صعبة الرصد بشكل ملحوظ. تقدم هذه الدراسة سير عمل مختبري عالي الإنتاجية يجعل من الممكن أخيراً رسم خريطة السيتروجينيل عبر آلاف البروتينات، كاشفاً متى وأين يظهر في الأنسجة وخلايا المناعة.
مفتاح خفي على البروتينات
يحدث السيتروجينيل عندما تُعدِّل إنزيمات تسمى PADs حمض الأرجينين الأميني كيميائياً، فتُزال شحنته الموجبة. هذا التغيير الظاهر متناهي الصغر يمكن أن يرخّي تعبئة الحمض النووي، ويغيّر صلابة البروتينات الهيكلية، أو يبدّل كيفية تعرف الجهاز المناعي على أنسجتنا. ارتبط السيتروجينيل غير الطبيعي بمرض الروماتويد واضطرابات التنكس العصبي والالتهابات الفيروسية والسرطان. ومع ذلك، فإن البروتينات السيتروجينيلية نادرة وسهلة الخلط مع تعديلات أخرى أكثر شيوعاً، لذلك غالباً ما تفشل طرق مطيافية الكتلة القياسية في رصدها. والنتيجة أن الباحثين امتلكوا رؤية مجزأة فقط لـ "السيتروجينوم"—المجموعة الكاملة من البروتينات السيتروجينيّة.
استراتيجية وسم-ثم-التقاط ذات خطوتين
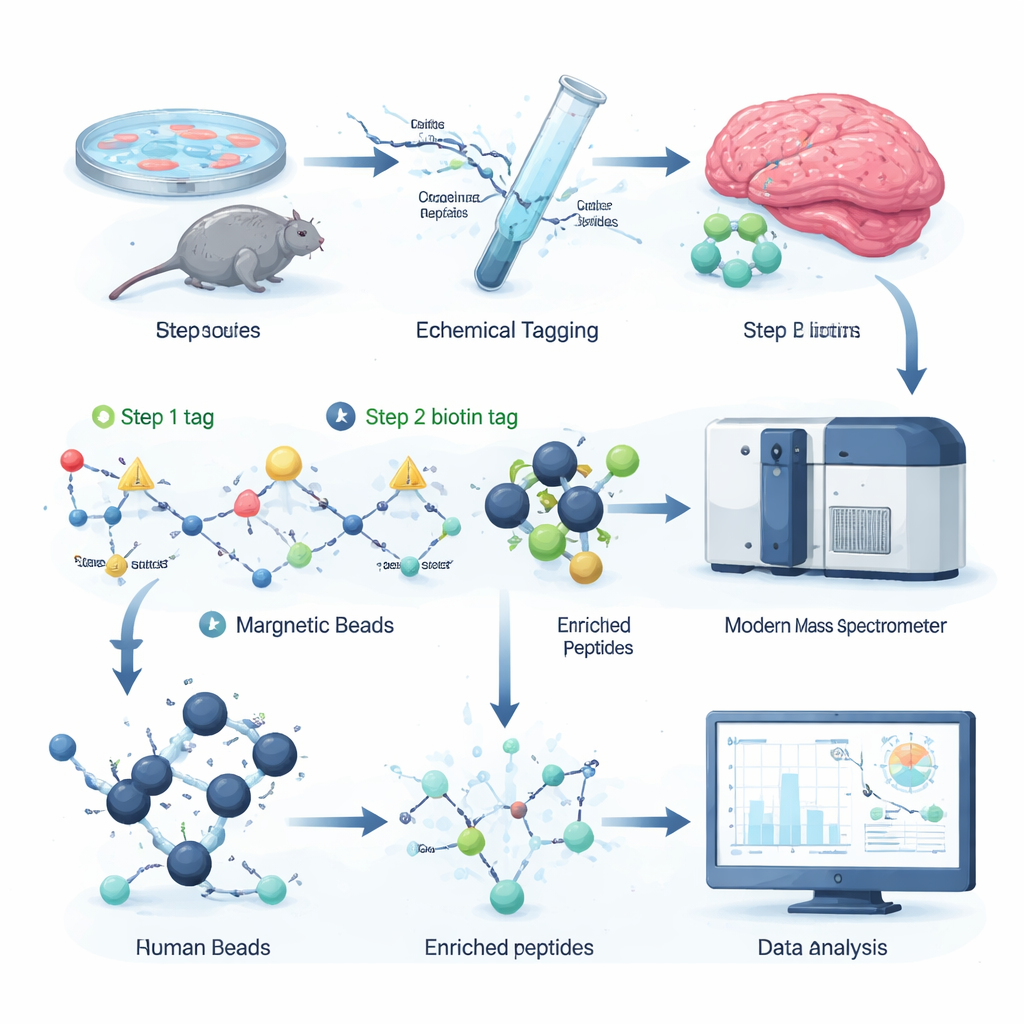
ابتكر المؤلفون استراتيجية وسم كيميائية تربط بشكل انتقائي "مقبضاً" قابلاً للإزالة إلى مواقع السيتروجينيل على الببتيدات، وهي قطع البروتين التي تُحلل بمطيافية الكتلة. في الخطوة الأولى، يتعرف جزيء تفاعلي صغير على السيترولين ويضع علامة دقيقة. في الثانية، يُضاف وسم بيونين أكبر عبر تفاعل تثبيت (click)، ما يسمح بسحب الببتيدات الموسومة من خليط معقّد باستخدام خرز الستربتافيدين، وهو أداة بيوكيميائية شائعة. ثم يزيل علاج كيميائي لطيف الجزء الضخم من الوسم، تاركاً تحولاً كتلته صغيراً ومحدداً يمكن لمطياف الكتلة اكتشافه بسهولة. وبما أن جميع الكواشف متاحة تجارياً وأن البروتوكول بأكمله يتناسب مع صفيحات 96 بئراً، فالسير العمل سريع وقابل للتوسعة ومتوافق مع إعدادات البروتيوميكس الموجودة.
رؤية أوسع للسيتروجينوم
بإضافة ببتيدات سيتروجينيّة معروفة إلى مستخلصات خلوية وتخفيفها بشكل منهجي، أظهر الفريق أن استراتيجية الإثراء لديهم تعزّز إشارة الببتيدات السيتروجينيّة بأكثر من عشرة أضعاف، حتى عندما تمثل أقل من واحد في الألف من الجزيئات. في العينات المعقّدة، ارتفع عدد المواقع السيتروجينيّة المكتشفة وشدات قياسها بشكل كبير بعد الإثراء. عند تطبيق الطريقة على نسيج دماغ فأر، كشفت عن ضعفين إلى ثلاثة أضعاف عدد مواقع السيتروجينيل المتميزة مقارنةً بمنهج سابق متقدم، بما في ذلك العديد على بروتين المايلين الأساسي الذي يعزل الألياف العصبية، وعلى بروتينات مشاركة في التواصل المشبكي. وهذا يشير إلى أن السيتروجينيل قد يؤثر على كل من كيفية إرسال الخلايا العصبية للإشارات وكيفية الحفاظ على توصيلات الدماغ.
خلايا مناعية تطلق شبكات بروتينية لزجة
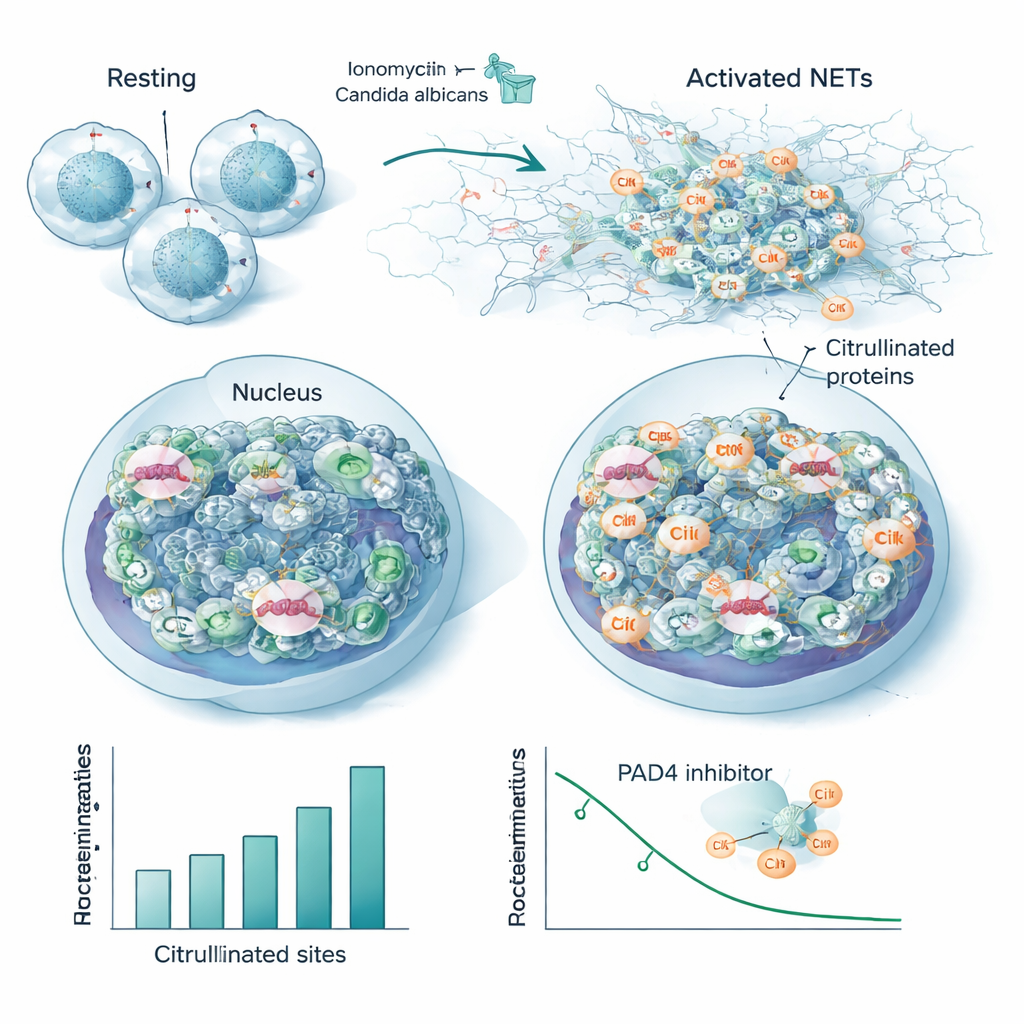
الخلايا المتعادلة (العدلات)، وهي نوع من خلايا الدم البيضاء في الصف الأول للدفاع، يمكنها مهاجمة المهاجمين عبر إطلاق شبكات لزجة من الحمض النووي والبروتينات تُسمى شبكات العدلات خارج الخلية (NETs). تعتمد تشكيلات NET على PAD4، إنزيم يسيتروجينيل يرخّي الكروماتين حتى يستطيع الحمض النووي أن ينساب للخارج. باستخدام سير العمل الجديد، تتبع الباحثون كيف تغيّر السيتروجينيل في العدلات البشرية المعرضة لجرعات متزايدة من منشط كيميائي. رصدوا ما يصل إلى 1700 شظية ببتيد سيتروجيني عبر 580 بروتيناً، مع مئات المواقع التي ارتفعت أو انخفضت بطريقة معتمدة على الجرعة بينما بقيت مستويات البروتين الشاملة ثابتة. أظهرت الهيستونات—البروتينات التي تعبّئ الحمض النووي—سيتروجينيل واسع الانتشار، وليس فقط عند بضعة مواقع كلاسيكية، وكانت متغيّرات الهستون الرابط H1 متعدلة بشكل خاص. كما أصبحت البروتينات الهيكلية مثل منظمات الأكتين واللَّامين B، الذي يشكّل الغلاف النووي، سيتروجينيّة بكثافة، مما يشير إلى تليين منسق لكل من الكروماتين والهياكل الخلوية أثناء إطلاق NETs.
بصمة سيتروجينيل أساسية في العدوى
لمحاكاة عدوى حقيقية، حفّز الفريق العدلات بخميرة كانديدا ألبكانز المقتولة بالحرارة، وهي مسبّب فطري شائع. على الرغم من أن هذا أثار عدداً أقل من المواقع المعدّلة بالمقارنة مع المنشط الكيميائي القوي، فإن الغالبية العظمى من البروتينات والمواقع السيتروجينيّة تداخلت بين المصدرين. يحدّد هذا التداخل "سيتروجينوماً أساسياً" محفوظاً مرتبطاً بتكوّن NETs، ويشمل العديد من البروتينات النوكليوية والسيتوهيكلية وعدداً من المستضدات الذاتية المعروفة—وهي الأهداف نفسها للأجسام المضادة في أمراض المناعة الذاتية. عندما أضاف الباحثون دواءً يثبط PAD4، فقدت العديد من هذه المواقع سيتروجينيلها بطريقة معتمدة على الجرعة، ما يربطها مباشرة بنشاط الإنزيم ويقترح أنها قد تكون مؤشرات حساسة على تثبيط PAD4.
ما الذي يعنيه هذا للصحة والمرض
بتحويل تعديل غامض إلى إشارة قابلة للقياس، يجعل هذا السير العمل من الممكن رسم خريطة أماكن وزمان حدوث السيتروجينيل في الأنسجة والاستجابات المناعية ونماذج المرض. للقراء غير المتخصصين، الرسالة الأساسية هي أن السيتروجينيل يعمل كشبه مفتاح خافت جزيئي على البروتينات، والقدرة على رؤية أنماطه بتفصيل عالٍ قد تساعد في تفسير كيف تبدأ أمراض المناعة الذاتية، وكيف تعيد العدوى تشكيل خلايا المناعة، وكيف تتغير بروتينات الدماغ مع مرور الوقت. وقابلية الطريقة للتوسيع واعتمادها على معدات مختبرية قياسية يعني أنه يمكن تبنّيها على نطاق واسع، فاتحاً الباب لاكتشاف أهداف دوائية جديدة، وتشخيصات دقيقة، وفهم أعمق لكيفية تسبب التعديلات الكيميائية الصغيرة في عواقب بيولوجية كبيرة.
الاستشهاد: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
الكلمات المفتاحية: السيتروجينيل, أمراض المناعة الذاتية, شبكات العدلات خارج الخلية, مطيافية الكتلة, تعديل بعد الترسيخ