Clear Sky Science · ar
مرجع عام محدد بواسطة قمم الإجماع لتحليل بيانات ATAC-seq على مستوى الخلية الواحدة
لماذا يهم رسم خريطة لأبواب الحمض النووي المفتوحة لدينا
كل خلية في جسمك تحمل تقريبًا نفس الحمض النووي، ومع ذلك تتصرف خلايا الدماغ والخلايا الدموية والخلايا الورمية بشكل مختلف تمامًا. سبب رئيسي في ذلك هو أن أجزاءً معينة فقط من الحمض النووي تكون معرضة و"مفتوحة" للاستخدام في أي وقت. تقنيات الخلية الواحدة الجديدة قادرة الآن على قياس هذه الانفتاحات عبر الجينوم، لكن حتى الآن افتقرت إلى خريطة مرجعية مشتركة — شيء شبيه بأطلس معياري — لمقارنة النتائج بين التجارب والمختبرات. تبني هذه الدراسة مثل هذه الخريطة، المسماة cPeaks، وتوضح كيف يمكنها أن توضح رؤيتنا لأنواع الخلايا والتطور والسرطان.
تحويل تجارب متعددة إلى خريطة مشتركة واحدة
بدأ المؤلفون بجمع 624 تجربة عالية الجودة قاست الكروماتين المفتوح — الأجزاء المتاحة من الحمض النووي — عبر أكثر من 40 عضوًا بشريًا. في كل تجربة، كانت البرامج الحاسوبية قد أشارت بالفعل إلى "قمم" حيث كان الحمض النووي مكشوفًا بشكل خاص. بدلاً من التعامل مع كل مجموعة بيانات بشكل منفصل، قام الفريق بتراكب قوائم القمم هذه على طول الجينوم ودمج المناطق المتداخلة بعناية. ثم فحصوا عدد مرات استدعاء كل موضع صغير داخل هذه المناطق المدمجة كمنطقة مفتوحة عبر التجارب، محولين كل منطقة إلى شكلٍ مميز يعكس مدى تكرار ظهورها. عندما احتوت منطقة مدمجة فعليًا على عدة مواقع مفتوحة متقاربة، قاموا بتقسيمها إلى وحدات أبسط متعددة. أصبحت هذه الوحدات — نحو 1.4 مليون في المجموع — قمم الإجماع الملاحظة، أو cPeaks، كفهرس مرجحي محتمل لتاحة الكروماتين البشري. 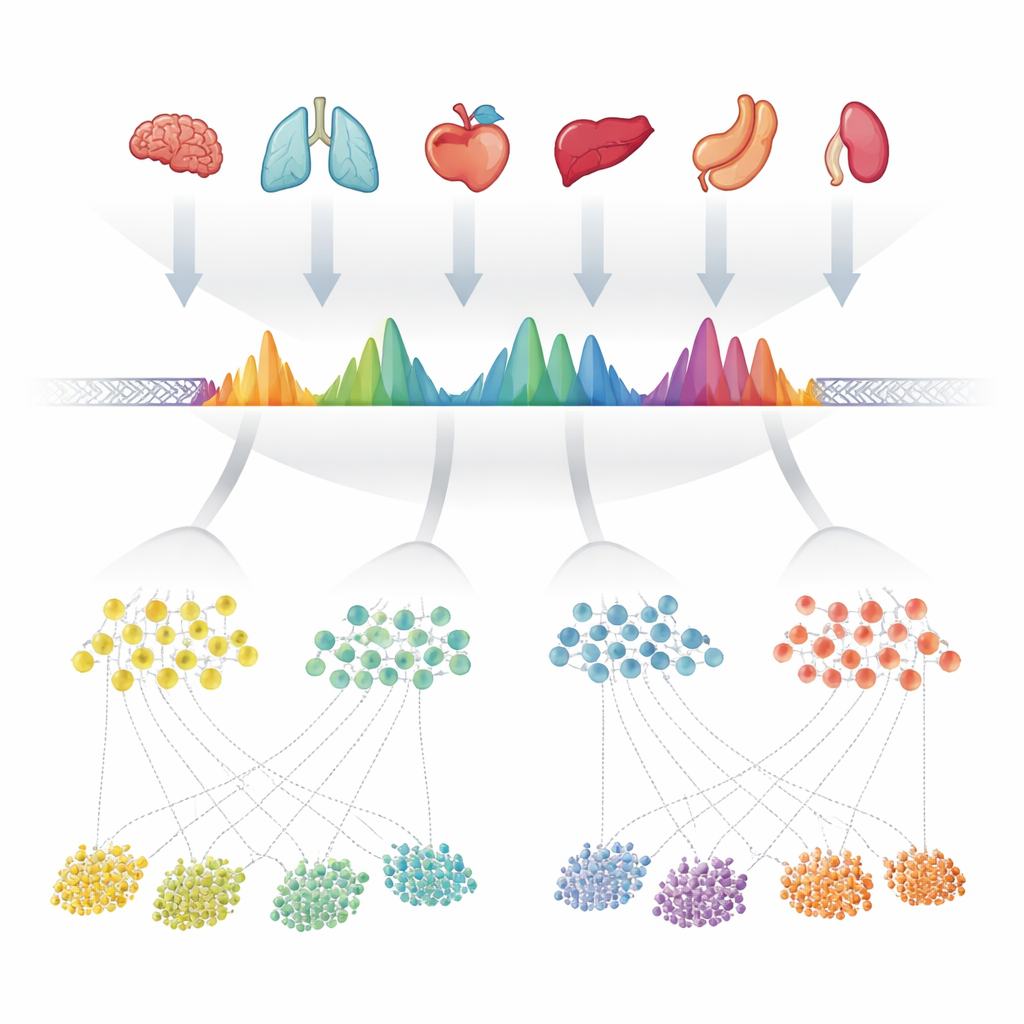
بصمة مستقرة عبر الأنسجة والتقنيات
لكي تكون مرجعًا مفيدًا، يجب أن تمثل هذه cPeaks سمات جينومية حقيقية وقابلة للتكرار، لا شذوذًا في عينات أو برامج محددة. اختبر المؤلفون ذلك بإعادة إنشاء مناطقهم المدمجة باستخدام عينات من الدم فقط، وأنسجة صلبة فقط، وقواعد بيانات عامة منفصلة، وحتى طرق مخبرية مختلفة لفحص الحمض النووي المفتوح. في كل حالة، أنتجت المواقع الجينومية نفسها أشكال قمم متشابهة بشكل ملحوظ، وتداخلت معظم مجموعات بيانات الخلية الواحدة التي فحصوها بأكثر من 90% من قممها مع فهرس cPeak. تراكمت القراءات من العديد من الأعضاء بدقة حول مراكز cPeaks، ما أظهر أن هذه المناطق تلتقط بشكل موثوق أماكن انفتاح الكروماتين. بالمقارنة مع مجموعات مرجعية سابقة مبنية على تقنيات ذات صلة، غطت cPeaks المزيد من الحمض النووي المتاح الذي تلتقطه تجارب ATAC-seq، والتقطت تقريبًا نفس قدر الإشارة التي تُعرّف فيها قمم جديدة في كل مجموعة بيانات — رغم كونها ثابتة وقابلة لإعادة الاستخدام.
تعليم شبكة عصبية لإيجاد المناطق المفقودة
حتى المئات من العينات الموجودة لا تغطي كل نوع خلية محتمل. لتمديد خريطتهم إلى مناطق لم تُرَ بعد، لجأ الفريق إلى التعلم العميق. دربوا شبكة عصبية تلافيفية أحادية البُعد على تسلسلات الحمض النووي: كانت الأمثلة الواقعة داخل cPeaks الملاحظة تُستخدم كإيجابيات، بينما استُخدمت مناطق خلفية عشوائية كسلبيات. تعلم النموذج التمييز بين هاتين الحالتين بدقة عالية، مما يوحي أن cPeaks تحمل أنماط تسلسلية قابلة للتمييز. عندما أخفى الباحثون عمدًا قممًا خاصة بنسيج واحد في كل مرة، استعادتها الشبكة من التسلسل وحده، بما في ذلك مواقع نادرة خاصة بأنسجة معينة. ثم مرروا نافذة صغيرة عبر بقية الجينوم، مقوّمِين كل مقطع وأضافوا نحو 280,000 منطقة جديدة ذات درجات عالية إلى الفهرس كـ cPeaks متوقعة، محسنين خصوصًا التغطية في الأنسجة الممثلة تمثيلًا ناقصًا في البيانات الأصلية.
ربط المناطق المفتوحة بالجِينات وأنواع الخلايا والخلايا النادرة
مع مرجع أغنى بين أيديهم، سأل المؤلفون عن وظيفة هذه المناطق. تقع العديد من cPeaks بالقرب من مواقع بدء ونهاية الجينات أو تتداخل مع عناصر تنظيمية معروفة مثل المروجات والمحسّنات ومواقع ارتباط بروتينات معمارية مثل CTCF. مجموعة فرعية صغيرة متاحة في كل تقريبًا مجموعة بيانات؛ تميل هذه cPeaks الطويلة "الخادمة" إلى الجلوس في مناطق المروج الأساسية للجينات اللازمة لصيانة الخلية الأساسية. صنّف الفريق أيضًا cPeaks بحسب مدى حدة وثبات حوافها عبر العينات، وهو ما يعكس مدى إحكام تغليف الحمض النووي القريب في نيكليوسومات. المناطق ذات الحدود المحددة بدقة تكون مُثرية لعائلات معينة من عوامل النسخ المعروفة بإعادة تشكيل الكروماتين ودفع التطور. عندما استخدمت cPeaks كمجموعة ميزات لتحليل مجموعات بيانات خلية واحدة متعددة، حسّنت من دقة تسمية أنواع الخلايا، وكانت مفيدة بشكل خاص في تحديد أنواع الخلايا النادرة والأنواع الفرعية الدقيقة التي كانت مجموعات القمم السابقة أو الشبكات الجينومية البسيطة تميل إلى طمسها معًا.
متابعة التطور والسرطان بلغة مشتركة
تتضح قوة المرجع الموحد عند مقارنة سياقات بيولوجية مختلفة للغاية. باستخدام cPeaks، أعاد المؤلفون تحليل بيانات خلية واحدة من شبكية العين البشرية النامية، وأطالس كبيرة للأنسجة الجنينية والبالغة، وعدد من السرطانات. تمكنوا من إعادة بناء المسارات التطورية ورؤية أن نسبة cPeaks ذات الحدود الحادة، أو "الموضوعة جيدًا"، تميل إلى الارتفاع خلال المراحل الانتقالية، ثم تنخفض بينما تستقر الخلايا في هويات مستقرة. ظهر نمط مماثل عبر مراحل الورم: أظهرت السرطانات المتوسطة نسبة أعلى من هذه المناطق المهيكلة، ما يلمح إلى إعادة تشكيل تنظيمية مكثفة. في ورم مبيضي واحد، ساعدت cPeaks في الكشف عن فرعين متميزين من خلايا السرطان مع تغيّرات مختلفة في عدد نسخ الحمض النووي، مما يبيّن كيف يمكن للمرجع أن يكشف تعقيدًا خفيًا في المرض.
ماذا يعني هذا لأبحاث الجينوم المستقبلية
بالنسبة لغير المتخصصين، يمكن التفكير في cPeaks كمجموعة معيارية من الإحداثيات التي تشير إلى الأماكن التي من المرجح أن يكون فيها الجينوم مفتوحًا ونشطًا عبر العديد من أنواع الخلايا البشرية. بمحاذاة تجارب الكروماتين الجديدة على مستوى الخلية الواحدة مع هذه الخريطة المشتركة، يمكن للباحثين مقارنة النتائج عبر الدراسات، واكتشاف الحالات الخلوية النادرة أو الانتقالية بسهولة أكبر، وبدء بناء نماذج واسعة النطاق لتنظيم الجينات — تمامًا كما مكّنت فهارس الجينات المعيارية ظهور أطالس الرنا الخلوي المفرد. إن فهرس cPeak الحالي هو مسودة أولية ستنمو مع ورود بيانات جديدة، لكنه يوفر بالفعل لغة مشتركة لوصف تاحة الكروماتين، مقربًا إيانا من رؤية موحَّدة لكيفية توجيه تغليف الحمض النووي للتطور والصحة والمرض. 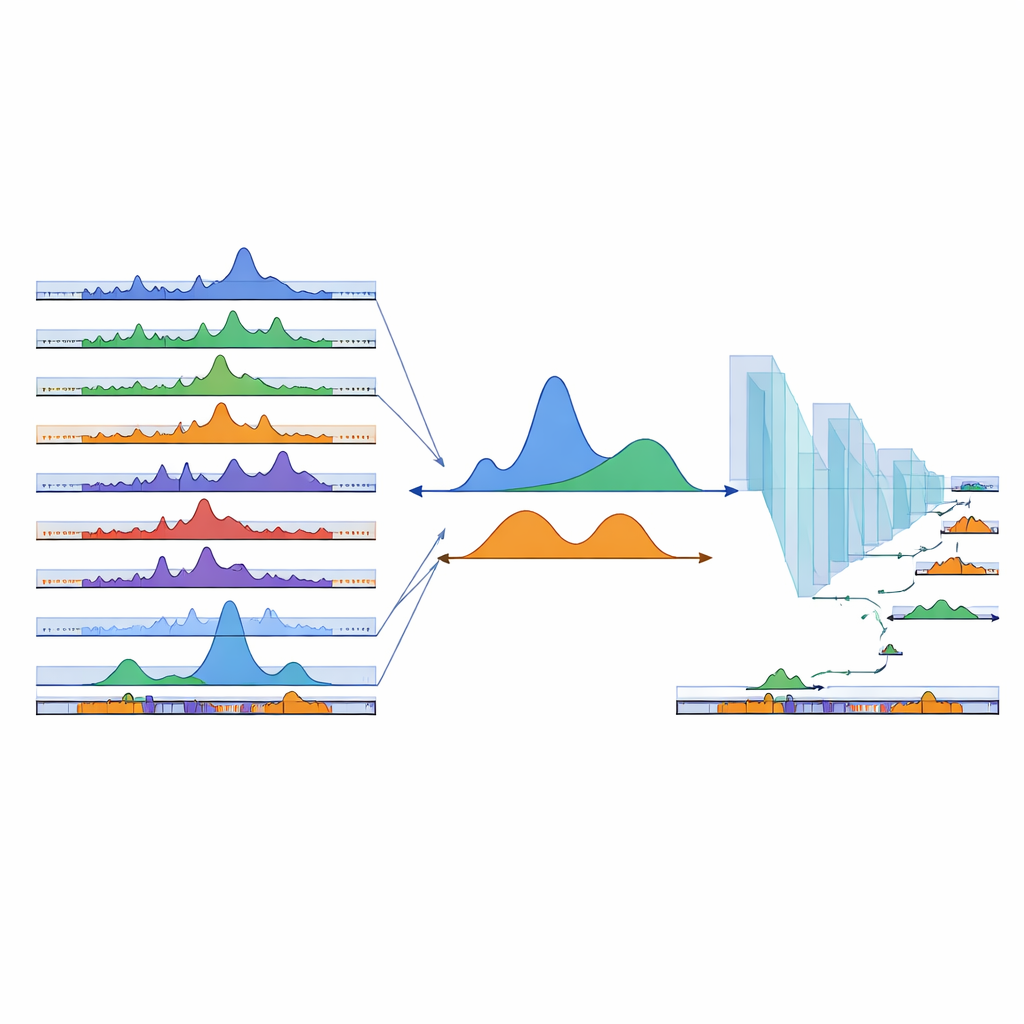
الاستشهاد: Meng, Q., Wu, X., Chen, W. et al. A generic reference defined by consensus peaks for single-cell ATAC-seq data analysis. Nat Commun 17, 2522 (2026). https://doi.org/10.1038/s41467-026-69461-6
الكلمات المفتاحية: تاحة الكروماتين, ATAC-seq خلية مفردة, قمم الإجماع, تنظيم الجينات, التعلم العميق في علم الجينوم