Clear Sky Science · ar
الاستهداف الثلاثي لـ STING وTGF-β وPD-L1 يعزز إشارة CXCL16–CXCR6 لاستجابة مضادة للورم قوية
تحويل الأورام الباردة إلى ساخنة
غيّر العلاج المناعي للسرطان مسار العلاج لبعض المرضى، ومع ذلك لا تزال العديد من الأورام تقاوم هذه الأدوية القوية. تستكشف هذه الدراسة سبب مقاومة بعض السرطانات لأدوية «نقاط التفتيش» المناعية الحديثة وتقترح هجومًا ثلاثي الاتجاهات أذكى يوقظ دفاعات الجسم، ويجذب خلايا T القاتلة المتخصصة، ويحافظ على نشاطها داخل الورم نفسه.
لماذا الأدوية المناعية الحالية غير كافية
تستهدف معظم العلاجات المناعية المعتمدة مكبحًا واحدًا على الخلايا المناعية، مثل مسار PD-1/PD-L1. تحاول فئة أحدث من الأدوية أن تذهب أبعد من ذلك من خلال حجب TGF-β أيضًا، وهي جزيئة تقمع المناعة بشدة في السرطانات المتقدمة. أحد هذه الأدوية، YM101، يجمع بين حجب TGF-β وPD-L1 في جسم مضاد واحد وأظهر وعدًا في الفئران. لكن حتى في حيوانات متطابقة وراثيًا، لم تتقلص بعض الأورام سوى القليل. بالمقارنة بين الأورام المستجيبة والمقاومة، وجد الباحثون أن العلاج الناجح ارتبط بتنشيط قوي للمناعة «الخلقية» بشكل خاص عبر مسار يُسمى STING، الذي يستشعر الحمض النووي الشاذ ويطلق إشارات إنذار شبيهة بمضاد الفيروسات.
إضافة رافعة ثالثة: مسار STING
بافتراض أن ضعف التنشيط الخلقي كان القطعة المفقودة، جمع الفريق بين YM101 ومنشط STING شبيه بالحبوب يُدعى MSA-2 عبر عدة نماذج أورام في الفئران، بما في ذلك الأورام «الباردة» الصعبة العلاج عادة. النهج الثلاثي — تفعيل STING بالإضافة إلى حجب TGF-β وPD-L1 — قلص الأورام بفعالية أكبر، ووسع فترة البقاء، وغالبًا ما حمى الفئران من نمو الورم مجددًا بعد إعادة التحدي، مما يشير إلى ذاكرة مناعية طويلة الأمد. تفوَّق هذا على الاقتران التقليدي لمنشط STING مع حجب PD-L1 وحده، وحتى عزز علاج منبه STING عندما حُجب TGF-β فقط، كاشفًا أن TGF-β نفسه يعمل كمكبح رئيسي للمناعة المدفوعة بـ STING. 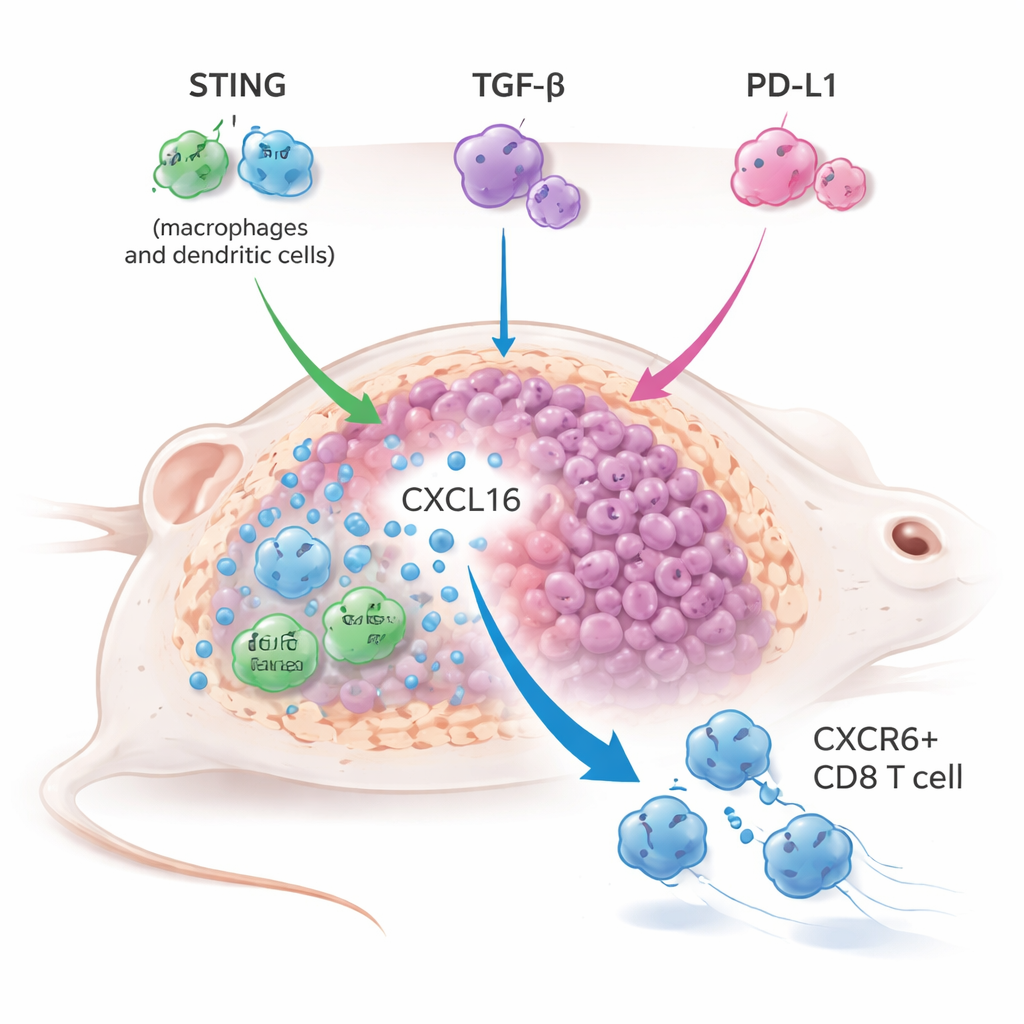
تجنيد فرقة قاتلة متخصصة
لفهم كيفية عمل هذه الاستراتيجية الثلاثية، استخدم الباحثون تسلسل الرنا المفرد الخلية وتوصيفًا مناعيًا مفصلًا للأورام المعالجة. اكتشفوا توسعًا لافتًا لشريحة معينة من خلايا T القاتلة تتميز بالمستقبل CXCR6. كانت خلايا CD8+ CXCR6+ هذه مسلحة تجهيزًا عاليًا، مع تعبير كبير عن الغرانزيمات والبيرفورين والجزيئات الالتهابية، وأظهرت علامات قوية على التنشيط والانقسام. في الوقت ذاته، زادت البلاعم المرتبطة بالورم والخلايا التغصنية من إنتاج كيموكين يُدعى CXCL16، الذي يرتبط بـ CXCR6 ويساعد في احتجاز هذه الخلايا التائية داخل الورم. عندما انقطع الوصل CXCL16–CXCR6 — إما بحجب CXCL16 أو بحذف جيني لـ CXCR6 في الخلايا التائية — فقد العلاج المشترك غالبية قوته المضادة للورم، مما يثبت أن هذا المحور مركزي لنجاح العلاج.
كيف يُشغَّل التسلسل الإشاري
بالغوص أعمق، سأل الفريق كيف يعزز تفعيل STING وحجب TGF-β معًا CXCL16. في خلايا مناعية بشرية وفأرية، زادت منبهات STING بشدة من CXCL16 والسيتوكين المضاد للفيروسات IFN‑β، بينما قلّل TGF-β المضاف كلاهما بشكل حاد. أظهر الباحثون أن STING يحفز إشارة IFN‑I، التي تنشط عامل النسخ STAT1؛ ثم يرتبط STAT1 مباشرة بمنطقة التحكم في جين CXCL16، مما يشغله. يعطل TGF-β هذه السلسلة من خلال التدخل في خطوة رئيسية من إشارات STING، على الأرجح عبر بروتين يسمى HDAC4 وأنواع الأكسجين التفاعلية، مما يقلل تنشيط IRF3 وإنتاج IFN‑β وCXCL16 لاحقًا. يزيل حجب TGF-β هذا المكبح، مما يسمح لمنبهات STING بإشعال مسار STAT1–CXCL16 في الخلايا النخاعية بالكامل وبالتالي تزويد خلايا T CXCR6+ بالإشارات التي تحتاجها للبقاء والقتال داخل الورم.
بناء دواء دقيق واحد
لجعل هذا النظام المعقد أكثر عملية ومركزًا على الورم، صمّم الباحثون جزيئًا واحدًا من «الجسم المضاد الرابِط المنشط للمناعة» أطلقوا عليه Y101S. يجمع هذا الجزيء بين جسم مضاد مزدوج الحجب لـ TGF-β/PD-L1 ومنشط STING مرتبط بواسطة رابط قابل للانفصال. يتوجه Y101S إلى الخلايا النخاعية الموجبة لـ PD-L1 في الورم، يُدخَل إلى داخلها، ثم يطلق دواء STING داخل هذه الخلايا. في عدة أنواع سرطانية للفئران، ضاهى Y101S أو تجاوز فعالية إعطاء YM101 بالإضافة إلى منبه STING حر بجرعة عالية، على الرغم من أنه يحمل فقط جزءًا ضئيلاً من جرعة STING تلك. عزز خلايا البلاعم والخلايا التغصنية الموجبة لـ CXCL16، وسع خلايا CD8+ CXCR6+، أحدث ذاكرة مناعية دائمة، وركّز الإشارات الالتهابية في الأورام مع حماية الأعضاء السليمة، مع ملف أمان ملائم في الفئران. 
ماذا يعني هذا لعلاج السرطان في المستقبل
لغير المتخصصين، الرسالة الأساسية هي أن مهاجمة السرطان بمفتاح أو مفتاحين من النظام المناعي قد لا تكون كافية — خاصة عندما تقوم الأورام بكتم أنظمة الإنذار المبكرة. تظهر هذه الدراسة أن الجمع بين تفعيل STING وحجب TGF-β وPD-L1 يمكن أن يعيد تشكيل بيئة الورم، ويجذب ويستمر في دعم مجموعة متخصصة من خلايا T القاتلة، ويحقق استجابات أعمق وأكثر ديمومة في نماذج ما قبل السريرية. يجسّد الجسم المضاد–الدواء ثلاثي الاستهداف Y101S هذه الاستراتيجية في دواء واحد موجه ويوفر خريطة طريق للعلاجات المناعية من الجيل القادم الموجهة إلى الأورام التي تقاوم حاليًا أدوية نقاط التفتيش القياسية.
الاستشهاد: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
الكلمات المفتاحية: العلاج المناعي للسرطان, مسار STING, حجب TGF-بيتا, جسم مضاد ضد PD-L1, خلايا T CXCL16 CXCR6