Clear Sky Science · ar
ملح كبريتات الغوانيدينيوم الديناميكي لامتصاص ثاني أكسيد الكربون الانتقائي مع انعطاف ضغط سالب
ملح ذكي يجذب ثاني أكسيد الكربون من الغاز
خفض ثاني أكسيد الكربون (CO2) من المداخن والهواء مركزي لبطء تغير المناخ، لكن معظم طرق الالتقاط الحالية تستهلك طاقة كبيرة ومعقدة. تقدم هذه الدراسة مادة بسيطة إلى حد ما—ملح عادي يُدعى كبريتات الغوانيدينيوم—يتصرف بطريقة استثنائية عند تعرضه لثاني أكسيد الكربون. فهو لا يكتفي بامتصاص كميات كبيرة من الغاز، بل يقوم بذلك عبر تأثير «ضخ ذاتي» مدمج يمكنه فعلاً خفض ضغط الغاز داخل حيز مغلق، فاتحاً إمكانيات جديدة لأجهزة مدمجة لالتقاط ثاني أكسيد الكربون والتحكم بالضغط.
لماذا يهم هذا الملح من أجل هواء أنظف
يُصنع كبريتات الغوانيدينيوم (GS) من مكونات رخيصة ومتوفرة ويمسك ببنيته روابط هيدروجينية، وهي نفس الجاذبيات اللطيفة التي تشكل الماء والحمض النووي. وبما أن هذه الروابط مرنة، يمكن لبنية البلورة أن تعيد ترتيب نفسها عندما تتعرض للحرارة أو ضغط الغاز. اكتشف المؤلفون أن GS يمكن أن يوجد في ثلاث حالات صلبة على الأقل، تُسمى الطور α والطور β والطور γ، والتي تختلف في الاستقرار وكمية الفراغ الداخلي. تحت ظروف معتدلة، يمكن لهذه الأشكال أن تستضيف CO2 بشكل انتقائي مع تجاهل النيتروجين، مما يشير إلى أن هذا الملح المتواضع قد ينافس المواد المسامية المتطورة المستخدمة لفصل الغازات.
كيف يغير المادي شكله لاحتجاز مزيد من الغاز
في قياسات دقيقة لكمية CO2 التي يمتصها الملح عند ضغوط مختلفة، وجد الفريق أن الشكل β من GS يقوم بسلوك نادر. في البداية، لا يدخل تقريباً أي CO2؛ فجواته الداخلية الصغيرة تكون مغلقة فعلياً حتى يتجاوز ضغط الغاز عتبة «بوابة». بمجرد الوصول إلى هذه النقطة، يبدأ CO2 بالتسرب إلى جيوب معزولة داخل البلورة. ومع ارتفاع الضغط أكثر، تزداد كمية CO2 الممتصة تدريجياً—إلى أن يصل الضغط إلى قيمة حرجة، حيث يخضع المادي لتحول مفاجئ وأعمق إلى طور γ الأكثر انفتاحاً ذو المسام الأكبر القادر على استضافة مزيد من جزيئات CO2.
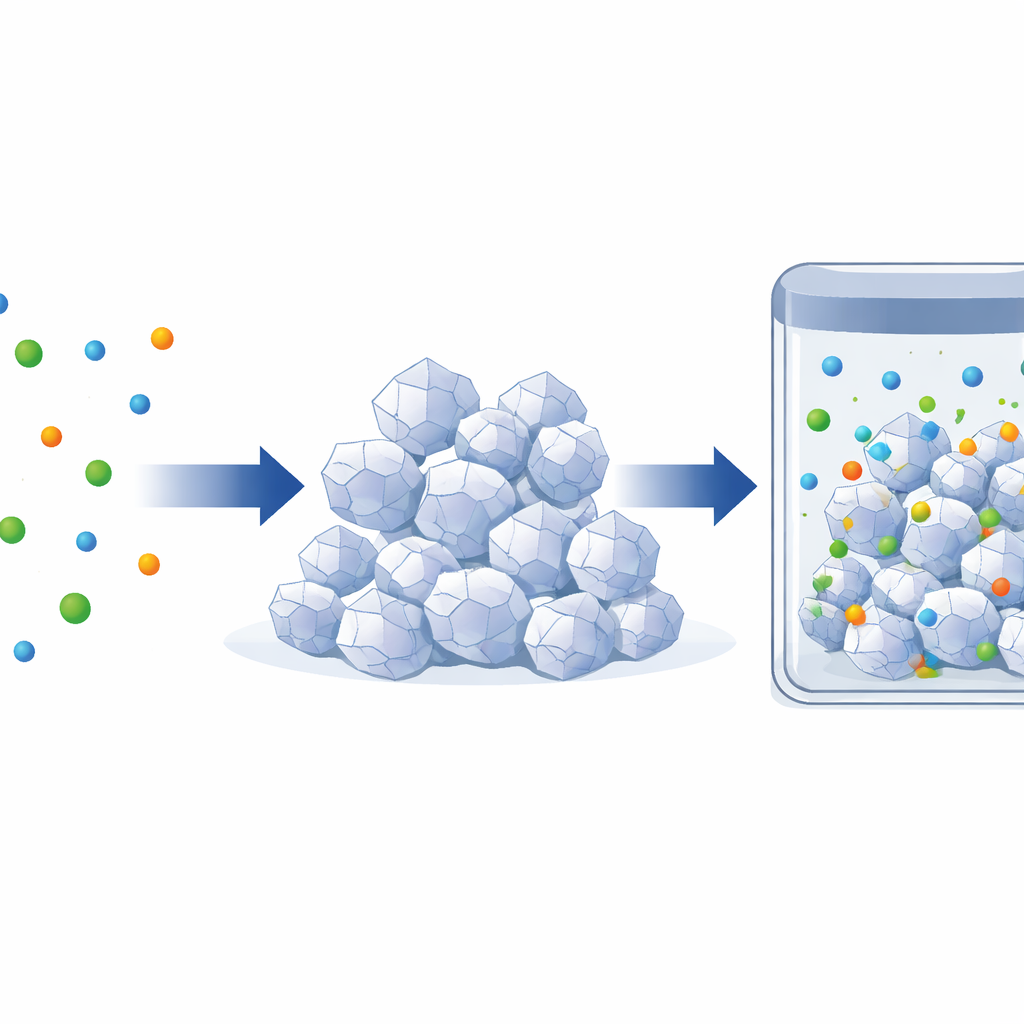
هبوط غريب في الضغط مع تفسير بسيط
في خلية اختبار مغلقة، تؤدي تلك القدرة الإضافية المفاجئة إلى تأثير معاكس للحدس يسميه المؤلفون انعطاف الضغط السالب. بدلاً من أن يرتفع الضغط في الخلية مع ضخ المزيد من CO2، ينخفض مؤقتاً. السبب هو أن إعادة هيكلة البلورة الداخلية تعمل كفتح غرف تخزين مخفية: يمتص الملح كمية إضافية من CO2 بسرعة أكبر من تزويد الغاز، فتختفي جزيئات CO2 من الطور الغازي الحر بسرعة أكبر من تعويضها، مما يخفض الضغط الكلي مؤقتاً. هذا عكس ظاهرة سابقة معروفة باسم طرد الغاز السالب، حيث يدفع الإطار الغاز نحو الخارج ويزيد الضغط. هنا، المادي «يبتلع» الغاز ويخفض الضغط بفعالية.
نظرة تحت غطاء البلورة
لفهم هذه القفزات الغريبة في السلوك، جمع الباحثون بين قياسات بالأشعة السينية ومحاكيات حاسوبية ترسم مشهد الطاقة لتراص البلورات الممكن. أكدوا أن α‑GS هو الشكل الأكثر استقراراً في الوضع الساكن، وβ‑GS أعلى طاقة قليلاً، وγ‑GS هو الأكثر انفتاحاً لكنه الأقل استقراراً ما لم يتواجد CO2. أظهرت الحسابات أنه مع امتلاء المسام بالمزيد من CO2، يصبح γ‑GS مفضلاً من الناحية الطاقية، مما يدفع التحول من β إلى γ. كشفت المحاكاة أيضاً حركات «تنفس» قصيرة في بنية β، حيث تتصل قنوات صغيرة لحظياً بالجيوب المعزولة، مما يسمح لثاني أكسيد الكربون بالانتشار وإطلاق التحول الشامل.
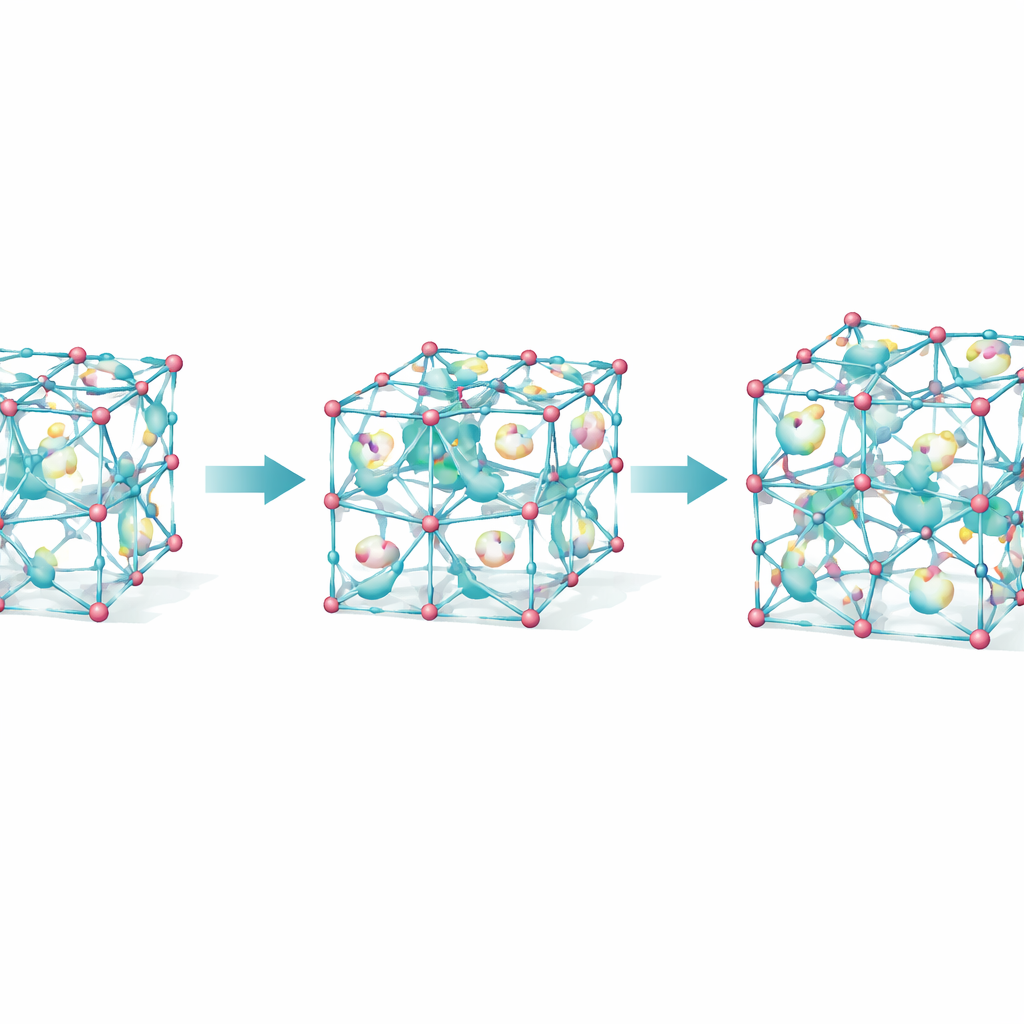
من فضول مخبري إلى إسفنج عملي لثاني أكسيد الكربون
يتجاوز العمل كونه فضولاً في فيزياء الغاز الصلب. يحمل الطور γ المحمّل بـCO2 نحو 17 بالمئة من وزنه في الغاز (حوالي 4.2 مليمول لكل غرام عند درجات قريبة من التجمد وضغوط يومية) ويطلقه نظيفاً عند تسخينه بلطف، دون التكلفة الطاقية الثقيلة لغليان الماء في محاليل الأمينات التقليدية. يظل الملح مستقرًا خلال العديد من دورات الالتقاط والإطلاق ويفضل CO2 بشدة على النيتروجين في الغازات المختلطة، وهو مطلب أساسي لمعالجة غازات المداخن في العالم الحقيقي. بعبارة بسيطة، يتصرف هذا الملح الديناميكي كإسفنجة تكيفية تفتح وتعيد تشكيل نفسها وحتى تخفض الضغط مؤقتاً لامتصاص CO2، مما يقدم مساراً واعداً نحو أنظمة أبسط وأكثر كفاءة لالتقاط وتخزين ونقل هذا الغاز المسبب للاحتباس الحراري.
الاستشهاد: Zhao, L., Zhao, C., Liu, C. et al. Dynamic guanidinium sulfate salt for selective carbon dioxide adsorption with negative pressure inflexion. Nat Commun 17, 2628 (2026). https://doi.org/10.1038/s41467-026-69433-w
الكلمات المفتاحية: التقاط ثاني أكسيد الكربون, الأملاح المسامية, امتصاص الغازات, الأطر المربوطة بروابط هيدروجينية, التحولات الطورية