Clear Sky Science · ar
الأساس البنيوي والجزيئي للتنظيم اللاالستيري والاقتران التحفيزي لإنزيم الفسفورايبوزيلفورميلغليسينأميدينس البشري
لماذا هذا الإنزيم مهم للصحة
تعتمد كل خلية في جسمك على البورينات، وهي جزيئات صغيرة تُمكّن التفاعلات، وتخزن الطاقة، وتحمل المعلومات الوراثية. خلايا السرطان، التي تنقسم بسرعة، تكون جائعة بشكل خاص للبورينات وغالبًا ما تعيد توصيل طرق تصنيعها. تركز هذه الدراسة على إنزيم بشري يُدعى FGAMS، وهو لاعب أساسي في بناء البورينات من الصفر. من خلال الكشف عن البنية ثلاثية الأبعاد لـ FGAMS وكيف تتحرك أجزاؤه وتتواصل، يكشف المؤلفون كيف يُشغّل ويُطفأ الإنزيم وكيف يمكن استهدافه لإبطاء نمو الأورام.
كتل الحياة تحت الرقابة
تكوّن الخلايا البورينات عبر خط تجميع متطلب يُعرف بمسار de novo، الذي يستهلك الطاقة ويتضمن عدة إنزيمات لربط حلقة معقدة معًا. يؤدي FGAMS الخطوة الرابعة في هذه السلسلة ويقع في قلب عنقود إنزيمي أكبر يُسمى البورينوسوم، الذي يساعد على توجيه المكونات بكفاءة. لأن خلايا السرطان سريعة النمو غالبًا ما تعزز هذا المسار، تصبح إنزيمات مثل FGAMS أهدافًا دوائية جذابة: فحجبها يمكن أن يجوع الأورام من النوكليوتيدات التي تحتاجها بينما تلجأ الخلايا السليمة إلى طرق إعادة التدوير.
آلة جزيئية قابلة لتغيير الشكل
يتكوّن FGAMS من ثلاثة أجزاء متصلة، أو مجالات، يؤدي كل منها وظيفة مختلفة ويجب أن تتعاون بترتيب دقيق. يزيل أحد المجالات الأمونيا من الحمض الأميني غلوتامين، ويستخدم مجال آخر تلك الأمونيا لتعديل جزيء سكري صغير، بينما يعمل المجال الثالث كمحور تنظيمي. باستخدام المجهر الإلكتروني بالتبريد عالي الدقة، التقط الباحثون FGAMS في ثلاث حالات تشغيلية مميزة: مرتبط بجزيء ناقل للطاقة، مع احتجاز وسط تفاعلي قصير العمر، ومع وجود عدة ركائز ووسطيات في آن واحد. كشف مقارنة هذه الحالات أن الحلقات المرنة و"الذراع" الطرفي N تتحرك بشكل دراماتيكي، معيدة تكوين الإنزيم مع تقدم الكيمياء.
نفق مخفي وبوابات جزيئية
كان لغز رئيسي هو كيف تنتقل الأمونيا المُحررة في مجال واحد بأمان إلى الموقع البعيد حيث تُستخدم، دون أن تتشتت وتسبب ضررًا. تكشف البنى الجديدة عن نفق داخلي لم يُرَ من قبل يربط الموقعين، إلى جانب سلسلة من "البوابات" التي تشكلها أحماض أمينية محددة. عندما ترتبط الركائز المناسبة ويتكون الوسط التفاعلي، يندفع حلقة مركزية إلى وضع منظم، ساعِرة المجال الطرفي N ومعيدة ترتيب الحلقات القريبة في المجال التحفيزي. تفتح هذه الرقصة بوابتين دخول حتى يُعالَج الغلوتامين وتُعيد تشكيل منطقة مؤقتًا لتثبيت الوسط عالي الطاقة المطلوب لكسر الروابط.
اقتران الكيمياء بالحركة
مع تقدم التفاعل، لا ينتظر الإنزيم ببساطة؛ بل يستخدم كل خطوة كيميائية كإشارة. بمجرد تكوّن وسط ثيوإستري تساهمي في المجال المنتج للأمونيا، تنعكس الحركات السابقة جزئيًا. هذا يريح الحلقة المركزية ويعيد وضع البوابات لإغلاق مسارات الهروب، بينما تندلق بوابتان إضافيتان عند كل طرف من النفق. تؤدي التحولات الطفيفة في بقايا قليلة تشكّل "عنق الزجاجة" إلى توسيع الممر الداخلي، مما يسمح لجزيء أمونيا بالمرور عبر النفق مباشرة إلى الموقع النشط الثاني، حيث يتفاعل مع الوسط المحتجز لإنتاج المنتج النهائي. التغيرات في بقايا البوابات تؤدي إلى تسرب الأمونيا أو فصل نصفي التفاعل، مؤكدة أن نظام البوابات والقناة هذا أساسي لتحفيز فعال.
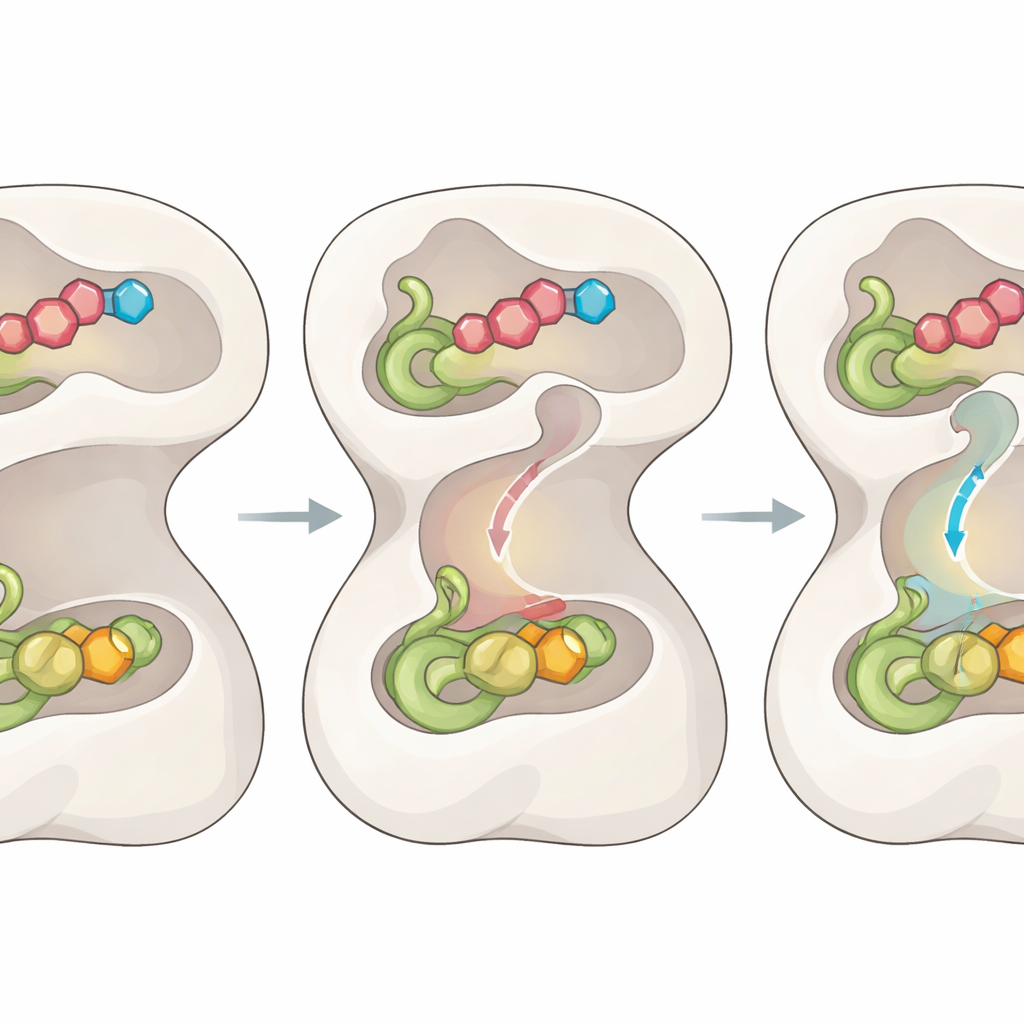
من الرؤية البنائية إلى مسارات علاجية
من خلال تتبع FGAMS خلال دورة نشاطه التحفيزي، تعرض الدراسة صورة مفصلة لكيفية توصيل حركات المجالات والحلقات المرنة والبوابات الداخلية والنفق العابر معًا لتنسيق الكيمياء. للقراء غير المختصين، الخلاصة أن الإنزيم يعمل كمصنع صغير قابل للبرمجة: لا يفتح أبوابه وحزامه الناقل الداخلي إلا عندما تكون كل القطع الصحيحة في مكانها، مما يضمن السرعة والسلامة. وبما أن FGAMS يدعم إنتاج البورينات في خلايا السرطان ومرتبَط بسوء البقاء في أورام الكبد، فإن المخططات البنائية ونقاط التحكم المكتشفة حديثًا توفر نقاط ارتكاز متعددة لتصميم أدوية تسد النفق، أو تجمّد البوابات، أو تحتجز الوسطيات الأساسية، مما قد يؤدي إلى فئة جديدة من العلاجات المضادة للسرطان الموجهة.
الاستشهاد: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
الكلمات المفتاحية: تخليق الأدينين والغاوانين, التنظيم اللاالستيري, قناة الأمونيا, استقلاب السرطان, بنية بالتبريد الإلكتروني المجهري