Clear Sky Science · ar
بروتين الإنفلامماسوم ASC داخل خلایا السرطان يربط المناعة الفطرية بتمثيل الطاقة الميتوكوندريا في دفع سرطان البنكرياس
لماذا هذا البحث مهم
يُعد سرطان البنكرياس من أخطر أنواع السرطان، وغالبًا ما يُكتشف متأخرًا بحيث تقل فرص العلاج الفعّال. يكشف هذا العمل عن «أسلاك» خفيّة داخل خلايا أورام البنكرياس تربط دفاعات الجسم الخط الأول مع طرق صنع واستخدام الطاقة في هذه الخلايا. من خلال إظهار أن بروتينًا واحدًا رابطًا للمناعة يسمى ASC يساهم في نمو الورم عبر إعادة برمجة استقلاب الخلية، يشير البحث إلى هدف جديد ودقيق للعلاجات المستقبلية في سرطان يحتاج بشدة إلى خيارات أفضل. 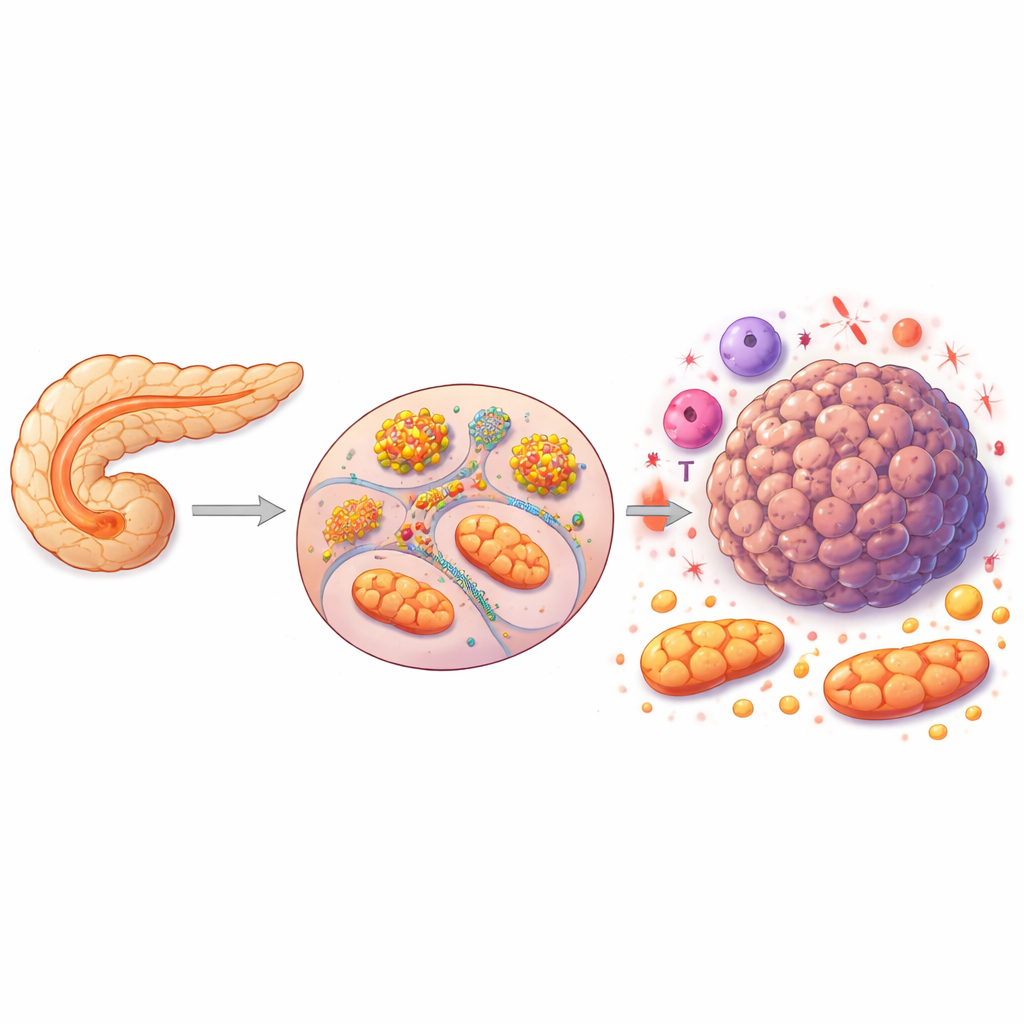
سرطان قاتل مع خيارات قليلة جيدة
معظم سرطانات البنكرياس هي من نوع غدّي قنوي البنكرياس، الذي ينشأ من الخلايا المبطنة للأنابيب الدقيقة في البنكرياس. عادةً ما تكون هذه الأورام متقدمة عند اكتشافها، والعلاجات الكيميائية والمناعية الحالية توفر فوائد محدودة. يعرف العلماء أن الالتهاب المزمن وبيئة الورم المعيقة للمناعة تساعد على نمو سرطان البنكرياس، لكن الجزيئات الدقيقة التي تربط اضطراب المناعة بسلوك الورم بقيت غير واضحة. يمكن أن يفتح تحديد مثل هذه الجزيئات الباب لعلاجات تبطئ المرض عن طريق قطع «خطوط دعم» حاسمة داخل السرطان نفسه.
مُوَصِّل مناعي يختبئ في خلايا الورم
ركز الباحثون على ASC، بروتين هيكلي عادةً ما يساعد في تجميع الإنفلامماسومات—آلات جزيئية تستشعر الخطر وتفعّل إشارات الالتهاب. عبر تحليل عدة مجموعات بيانات مرضى، وجدوا أن الجين المشفر لـ ASC (PYCARD) مرتفع باستمرار في أورام البنكرياس مقارنةً بالبنكرياس السليم، عبر الأنماط الجزيئية المختلفة للمرض. ارتبطت مستويات ASC العالية، ومستويات مرتفعة من إنزيمه الشريك كاسبيز-1 والسيتوكين IL-18، ببقاء أسوأ للمرضى. باستخدام تقنيات تلوين متقدمة على خزعات الأورام، أظهر الفريق أن ASC وكاسبيز-1 المنشط يوجدان بشكل أساسي داخل خلايا القنوات السرطانية نفسها، مكوّنين «بقع» متوهجة نقطية داخل الخلايا وفي النسيج المحيط—دليل على وجود مجمعات إنفلامماسوم نشطة. 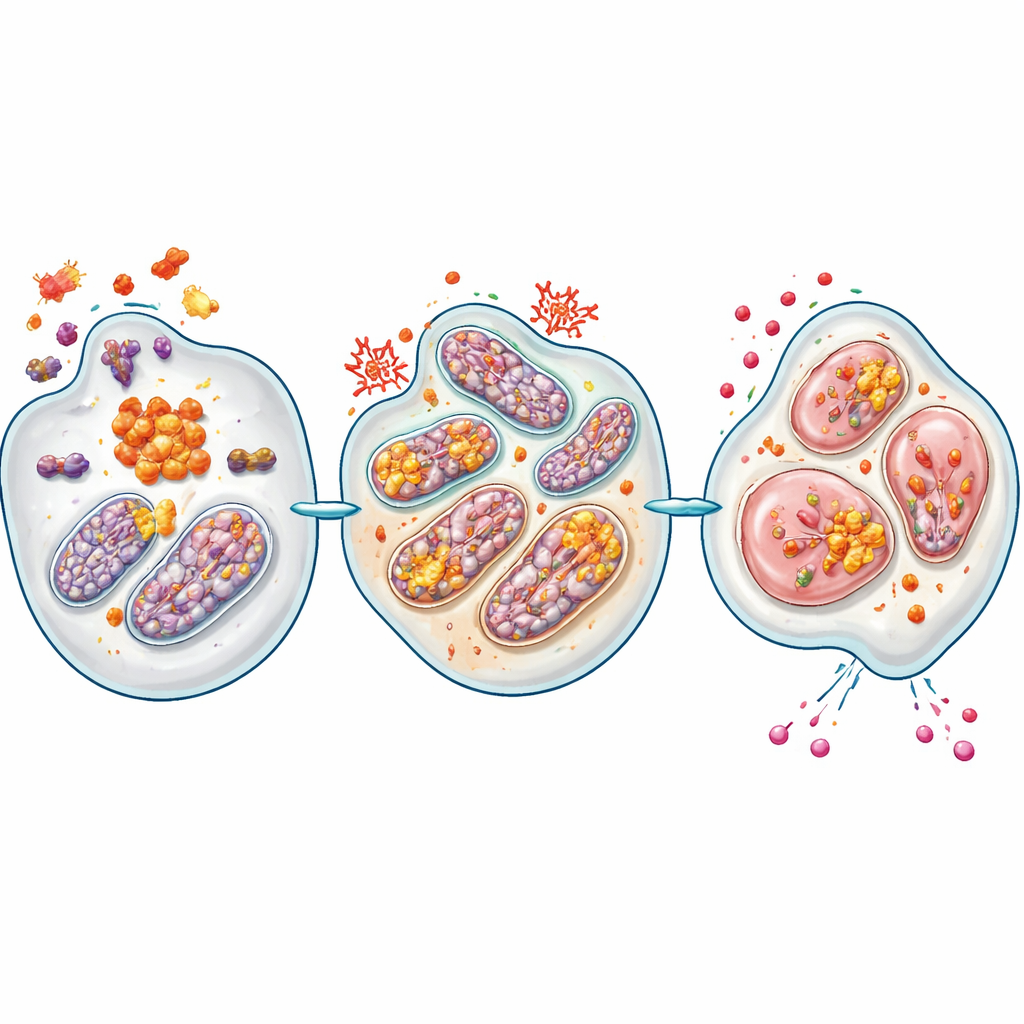
إيقاف ASC يبطئ نمو الورم
لاختبار ما إذا كان ASC يساعد فعلاً في التسبب بسرطان البنكرياس بدلًا من كونه مرافقًا فقط، استخدم الباحثون نموذجًا فأريًا راسخًا يقوده طفرات في جينات Kras وTrp53، يواكب المرض البشري عن قرب. في هذه الفئران، كانت مستويات ASC وكاسبيز-1 وIL-18 مرتفعة في البنكرياس، وارتفع IL-18 الدوري مع تقدم الآفات. عندما تم حذف ASC في جميع أنحاء الجسم، طوّرت الفئران بنكرياسات أصغر بكثير، وكانت لديها أورام أقل وعدوانية بدرجة كبيرة، ولم تُظهر نقائل كبدية. أدى الحذف الانتقائي لـ ASC فقط في эпителия قنوات البنكرياس إلى تأثير وقائي قوي، وإن كان أضعف بعض الشيء، مما يؤكد أن ASC داخل خلايا الورم هو محرك رئيسي. ومن المهم أن حجب «بقع» ASC خارج الخلايا بواسطة دواء نانوبودي متخصص قلل أيضًا من عبء الورم وتكاثر الخلايا، مما يشير إلى أن ASC يعمل داخل وخارج الخلايا لتعزيز المرض.
إعادة توجيه محطات طاقة الخلية
بتعمق أكثر، استخدم الفريق ملف التعبير الجيني الكامل لمقارنة نشاط الجينات في بنكرياسات طبيعية وحاملة للأورام وبدون ASC. في الفئران الحاملة للأورام، كانت الجينات المرتبطة بتنشيط المناعة مفعّلة، بينما تراجعت تلك المرتبطة بالتنفس الميتوكوندري والفسفرة التأكسدية—المسار الرئيسي لإنتاج الطاقة في الخلية. عكس فقدان ASC هذا النمط إلى حد كبير. أكدت الاختبارات الكيميائية الحيوية أن بروتينات السلسلة التنفسية الميتوكوندرية الأساسية كانت منخفضة في الأورام ولكن استعادت مستواها عند غياب ASC. كان لدى الفئران المصابة بالأورام نسخ أقل من DNA الميتوكوندريا، وضرر أكسدي أعلى، ومستويات لاكتات مرتفعة، وهي كلها علامات تحول من إنتاج الطاقة المعتمد على الأكسجين إلى تحلل السكر الهوائي الشبيه بواربورغ. أدى إزالة ASC إلى زيادة عدد نسخ DNA الميتوكوندريا وخفض كل من الأكسدة الضارة وإنتاج اللاكتات.
من نماذج الفئران إلى خلايا سرطان بشرية
للتحقق مما إذا كانت هذه النتائج تنطبق مباشرة على أورام بشرية، خفض المؤلفون مستويات ASC في خطين خلويين بشريين لسرطان البنكرياس باستخدام RNA متداخل صغير. أظهرت الخلايا ذات ASC المنخفض نشاط كاسبيز-1 أقل، ونمَت ببطء أكبر، شكلت مستعمرات أقل، وأنتجت لاكتات وأوكسيد فائق ميتوكوندري أقل. تعافت جينات الميتوكوندريا وعدد نسخ DNA الميتوكوندريا، وزاد استهلاك الأكسجين والقدرة التنفسية الاحتياطية، مما يدل على تحول عكسي نحو تنفس ميتوكوندري أكثر صحة. ومن اللافت أن هذه الخلايا الناقصة ASC أصبحت أقل حساسية للأدوية التي تحجب تحلل الغلوكوز، متسقة مع اعتماد أقل على هذا الطريق الطاقي المناسب للسرطان. مجتمعة، تُظهر هذه النتائج أن ASC يوجّه بنشاط خلايا سرطان البنكرياس نحو حالة عالية التحلل السكري والإجهاد التأكسدي التي تدعم النمو السريع.
ماذا يعني هذا للعلاج المستقبلي
يكشف هذا البحث أن ASC عبارة عن «جسر» مركزي بين المناعة الفطرية والالتهاب المزمن واستقلاب الطاقة المعطوب الذي يغذي سرطان البنكرياس. بدلاً من العمل فقط في خلايا المناعة التقليدية، يساعد ASC داخل خلايا القنوات السرطانية في تجميع إنفلامماسومات تُفضّل إنتاج IL-18، وتعرقل بناء الميتوكوندريا، وتدفع الخلايا نحو التحلل السكري والنمو العدواني. في الفئران، يؤدي إزالة ASC وراثيًا أو تحييد بقعها خارج الخلايا إلى إبطاء تقدم المرض، مما يشير إلى أن الأدوية التي تستهدف ASC أو مجمعات الإنفلامماسوم الخاصة به قد تكمل العلاجات الحالية. وبينما تبقى أسئلة—مثل أي مستشعرات عليا تغذي ASC في هذا السرطان وكيفية حجب IL-18 بأمان—يوفر هذا العمل مسوّغًا مقنعًا لمتابعة ASC كهدف علاجي جديد قائم على الآلية في سرطان غدّي قنوي البنكرياس.
الاستشهاد: Chey, Y.C.J., Kashgari, B., McLeod, L. et al. Cancer cell-intrinsic inflammasome protein ASC links innate immunity with mitochondrial metabolism in driving pancreatic cancer. Nat Commun 17, 2477 (2026). https://doi.org/10.1038/s41467-026-69398-w
الكلمات المفتاحية: سرطان البنكرياس, الإنفلامماسوم, تمثيل الطاقة الميتوكوندري, IL-18, مناعة السرطان