Clear Sky Science · ar
اللاكتات المشتق من البلعميات يحفّز إعادة تشكيل النمط الظاهري للخلايا الليفية الجلدية عبر لاكتيلاسيون لايسين 23 في الهستون H3 المهيأ بواسطة MCT1 في الندبة المتضخمة
لماذا تنمو بعض الندوب كثيفة وبارزة
معظم القطوع والحروق تتلاشى في النهاية لتصبح ندوباً رقيقة ومسطحة. لكن بعض الجروح تلتئم بأشرطة نسيجية سميكة وبارزة تُسمى ندوباً متضخمة يمكن أن تحكّ أو تؤلم وتقيّد الحركة. تكشف هذه الدراسة عن محرك غير متوقع لتلك الندوب العنيدة: ناتج أيضي شائع يسمى اللاكتات، تنتجه خلايا الجهاز المناعي في الجلد الصلب أثناء الالتئام، ويعيد برمجة خلايا الإصلاح المجاورة لتتصرف بطريقة أكثر عدوانية وتشكّل نسيجاً ندبيّاً.
من الإصلاح الطبيعي إلى الندبة المشكلة
في شفاء الجروح الصحي، تتعاون خلايا الجلد لإغلاق الإصابة وإعادة بناء النسيج. تتحول الخلايا الليفية، وهي خلايا الإصلاح الرئيسية في الطبقة العميقة من الجلد، مؤقتاً إلى حالة أقوى تُنتج الكولاجين، البروتين البنيوي للجلد. بمجرد إغلاق الجرح، تهدأ هذه الخلايا مجدداً. في الندوب المتضخمة، ومع ذلك، تبقى الخلايا الليفية عالقة في هذه الحالة المفرطة الإنتاج، وتودع كمية زائدة من الكولاجين في حزم سميكة ومشوشة. بدأ المؤلفون بمقارنة الجلد الطبيعي بنسيج الندبة المتضخمة ووجدوا تحولاً أيضياً واضحاً: بيئة الندبة تفضّل الكيمياء السريعة لحرق السكر التي تولّد كميات كبيرة من اللاكتات، إلى جانب مستويات مرتفعة من بروتين ناقل يُدعى MCT1 الذي ينقل اللاكتات إلى داخل الخلايا. 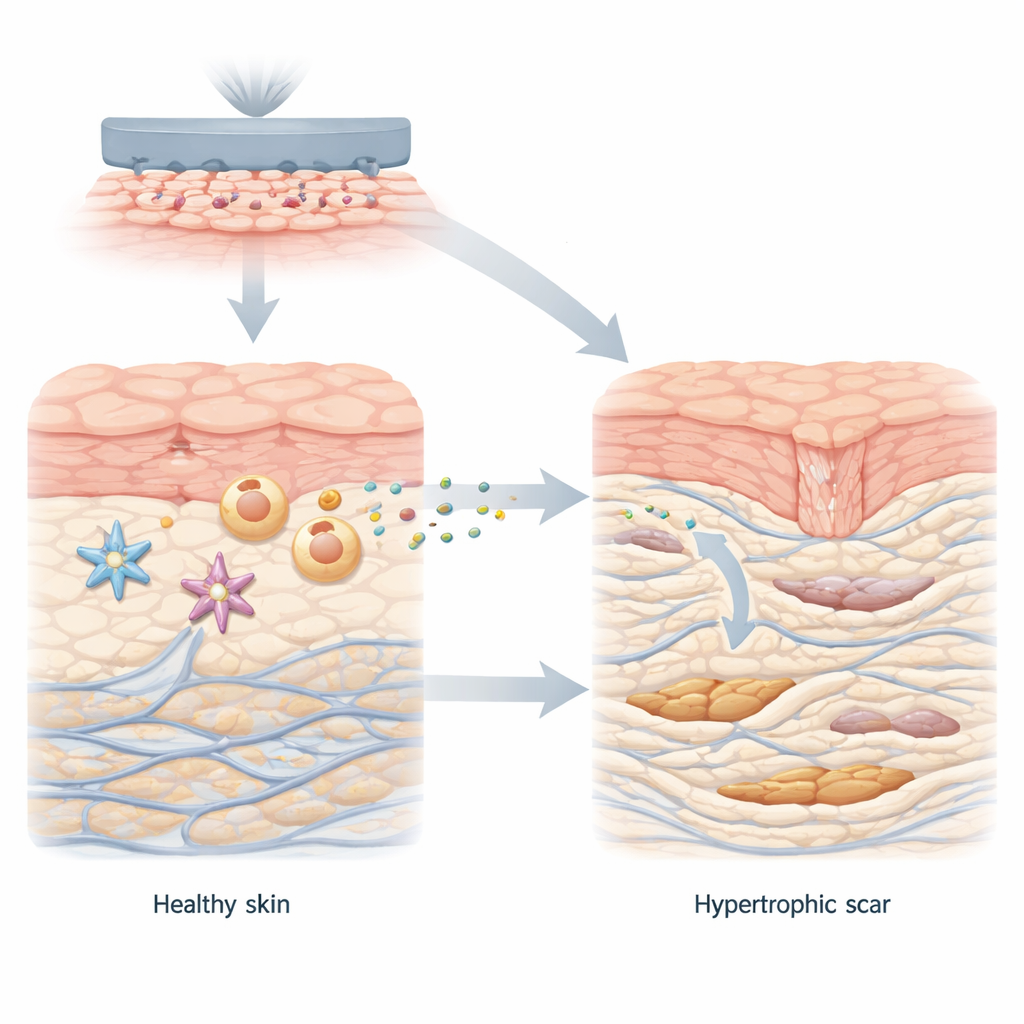
الخلايا المناعية كمصانع غير متوقعة للاكتات
لاكتشاف مصدر كل هذه اللاكتات، فحص الفريق أنواعا مختلفة من الخلايا من جلد الإنسان ونماذج الفأر: البلعميات (خلايا مناعية تزيل الحطام وتنسق الشفاء)، وخلايا الأوعية الدموية، والخلايا الليفية. زرعوا هذه الخلايا على مواد لينة أو صلبة تحاكي الجلد الطبيعي والمندوب. على الأسطح الصلبة، تحوّلت البلعميات فقط إلى نمط أيضي عالي الجلوكوليز، أي عاطشة للسكر، وطرحت كميات كبيرة من اللاكتات، سواء في أطباق المختبر أو في نسيج الندبة الفعلي. عندما أُزيلت البلعميات من جروح الفأر الملتئمة، انخفضت مستويات اللاكتات في النسيج وتراجع تكوّن الندبة. تشير هذه النتائج إلى أن البلعميات، خصوصاً تلك التي تستشعر بيئة صلبة، هي المصانع الرئيسية للاكتات التي تشكل بيئة الندبة الدقيقة.
اللاكتات كإشارة تعيد توصيل الخلايا الليفية
بعد ذلك، سأل الباحثون كيف يؤثر هذا الفائض من اللاكتات على الخلايا الليفية. عندما تعرضت الخلايا الليفية لسوائل غنية باللاكتات من بلعميات مزروعة على وسط صلب، تكاثرت بسرعة أكبر، وتحركت أكثر، وأنتجت المزيد من الكولاجين، وهي جميعها علامات حالة المايوفايبروبلاست العدوانية. حجب ناقل MCT1 على الخلايا الليفية، أو تقليل إنتاج اللاكتات في البلعميات، خفّف هذه التغيرات بشكل كبير. داخل الخلايا الليفية، لم يعمل اللاكتات الداخل كمصدر طاقة فحسب: بل حفّز وسمًا كيميائيًا محددًا على بروتينات الهستون التي تعبّأ الحمض النووي في نواة الخلية. هذا الوسم، المسمى لاكتيلاسيون H3K23، كان أعلى بكثير في الخلايا الليفية المكوّنة للندبة منه في الخلايا الطبيعية، وعمل كمفتاح يُشغّل اثنين من الجينات الأساسية، HEY2 وCOL11A1، التي معاً تضخم إشارات التندّب.
حلقة ندبية معززة ذاتياً
تشكل البروتينات التي يحفزها هذا الوسم الهستوني حلقة تغذية راجعة قوية. يعزز HEY2 نشاط مسار يتضمّن YAP1 وSMAD2، المعروف بدفع الخلايا الليفية نحو حالة أكثر تقلصًا وإنتاجًا للكولاجين. يتفاعل COL11A1، وهو بروتين بنيوي مرتبط بالكولاجين، فعلياً مع ناقل MCT1 على الخلايا الليفية، مما يساعد على استقراره وجعل امتصاص اللاكتات أكثر كفاءة. بعبارة أخرى، دخول اللاكتات إلى الخلية يغيّر تنظيم الجينات بطريقة تزيد من دخول اللاكتات وإنتاج الكولاجين، مما يقفل الخلايا الليفية في هوية مؤيدة للتندّب. 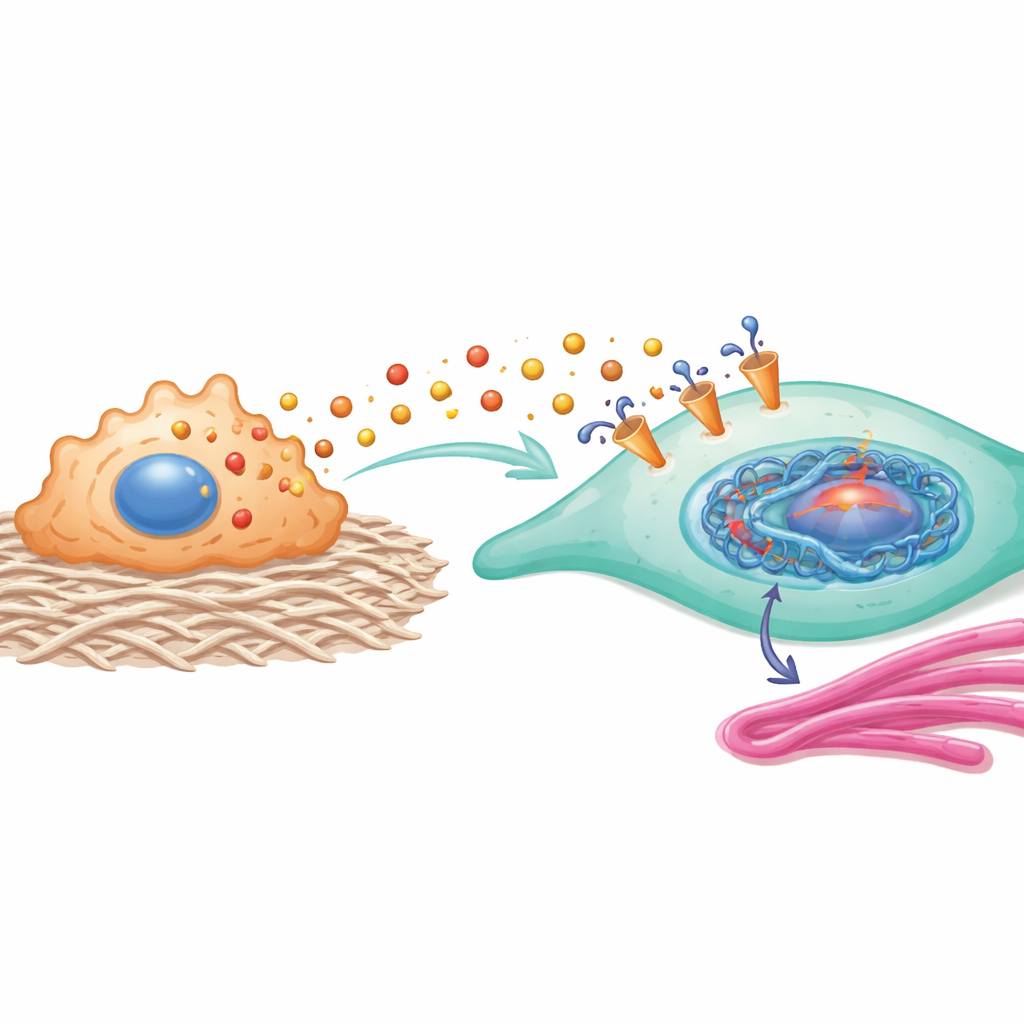
إضعاف الحلقة لتحسين الشفاء
لاختبار ما إذا كان قطع هذه الحلقة يمكن أن يحسّن الشفاء، استخدم الفريق فئرانًا يمكن إسقاط MCT1 انتقائياً من خلاياها الليفية، وكذلك دواءً يثبط MCT1. في كلتا الحالتين، أُغلقت الجروح أسرع، وبدا الجلد المتكوّن أكثر تنظيماً، وكانت ألياف الكولاجين أنحف وأكثر انتظامًا، مع سمات أقل للندبة المتضخمة. كما انخفض الوسم الهستوني المحدد وجيناته المتبوعة. كان لنفاد البلعميات، المصدر الرئيسي للاكتات، أو خفض اللاكتات كيميائياً تأثيرات مضادة للندبة مماثلة. تُظهر هذه التجارب أن سلسلة الجرح الصلب–البلعميات–اللاكتات–الخلايا الليفية ليست مجرد ارتباط بل محرك رئيسي للتندّب المرضي.
ما يعنيه هذا لعلاجات الندوب المستقبلية
تعيد هذه النتائج تصور اللاكتات من نفاية أيضية بسيطة إلى رسول قوي يربط الميكانيكا والأيض وتنظيم الجينات في شفاء الجروح. من خلال إظهار كيف يغيّر اللاكتات المشتق من البلعميات، والمحمّل عبر MCT1، الهستونات ويشغّل برنامج تندّب معزّز ذاتياً في الخلايا الليفية، تبرز الدراسة عدة أهداف علاجية واعدة. قد تساعد الأدوية التي تعدّل إنتاج اللاكتات، أو تحجب MCT1، أو تتدخل في الوسم الهستوني المحدد يومًا ما الجروح على الالتئام أسرع وبندوب أكثر تسطحًا وأقل وضوحًا.
الاستشهاد: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
الكلمات المفتاحية: ندبة متضخمة, إشارة اللاكتات, حوار البلعميات–الخلايا الليفية, لاكتيلة الهستون, علاج شفاء الجروح