Clear Sky Science · ar
مايوفيرلين مكوّن من حويصلات نقل vRNP في المراحل المتأخرة للفيروسات المغلفة ذات الحمض النووي الريبي
لماذا هذا مهم للصحة اليومية
قد تبدو الإنفلونزا الموسمية والالتهابات التنفسية الأخرى أمرًا روتينيًا، لكنها معًا تقتل ملايين الأشخاص في جميع أنحاء العالم كل عام. العديد من هذه الفيروسات، بما في ذلك فيروس الإنفلونزا A وفيروس المخلوي التنفسي (RSV)، تتفلت بالفعل من اللقاحات والأدوية المضادة للفيروسات عبر الطفرات السريعة. تبحث هذه الدراسة بدلاً من ذلك في شيء لا تستطيع الفيروسات تغييره بسهولة: آلية الخلية البشرية التي تنتزعها للخروج من الخلايا المصابة. من خلال كشف نقطة ضعف مشتركة في تلك الآلية، يشير العمل إلى أدوية مستقبلية قد تقلص مجموعة واسعة من الفيروسات التنفسية دفعة واحدة.
مسار خلوي للتوصيل تستغله الفيروسات
تُعيد خلايا مجرى الهواء باستمرار استخدام أجزاء من غشاءها الخارجي عبر عملية تُسمى إعادة التدوير. فقاعات غشائية صغيرة، أو حويصلات، تنقل الحمولة من داخل الخلية إلى السطح، موجهة بواسطة عائلة بروتينات تُعرف مجتمعة باسم Rab11. يستغل فيروس الإنفلونزا A وRSV وفيروس تابع له يُسمى فيروس سنداي هذا المسار في المراحل المتأخرة من العدوى. يحمّلون حمولتهم الجينية، المغلفة كمجمعات ريبونو-بروتينية، على حويصلات تحتوي Rab11 التي تحملها إلى الجانب العلوي (المواجه للمجرى الهوائي) من الخلية، حيث تنبثق جُسيمات فيروسية جديدة وتنتشر. حتى الآن، كان Rab11 هو العامل الوحيد للمضيف المعروف بوضوح على هذه الحويصلات الناقلة، مما ترك فجوة كبيرة في فهمنا لكيفية تكوّنها وعملها.
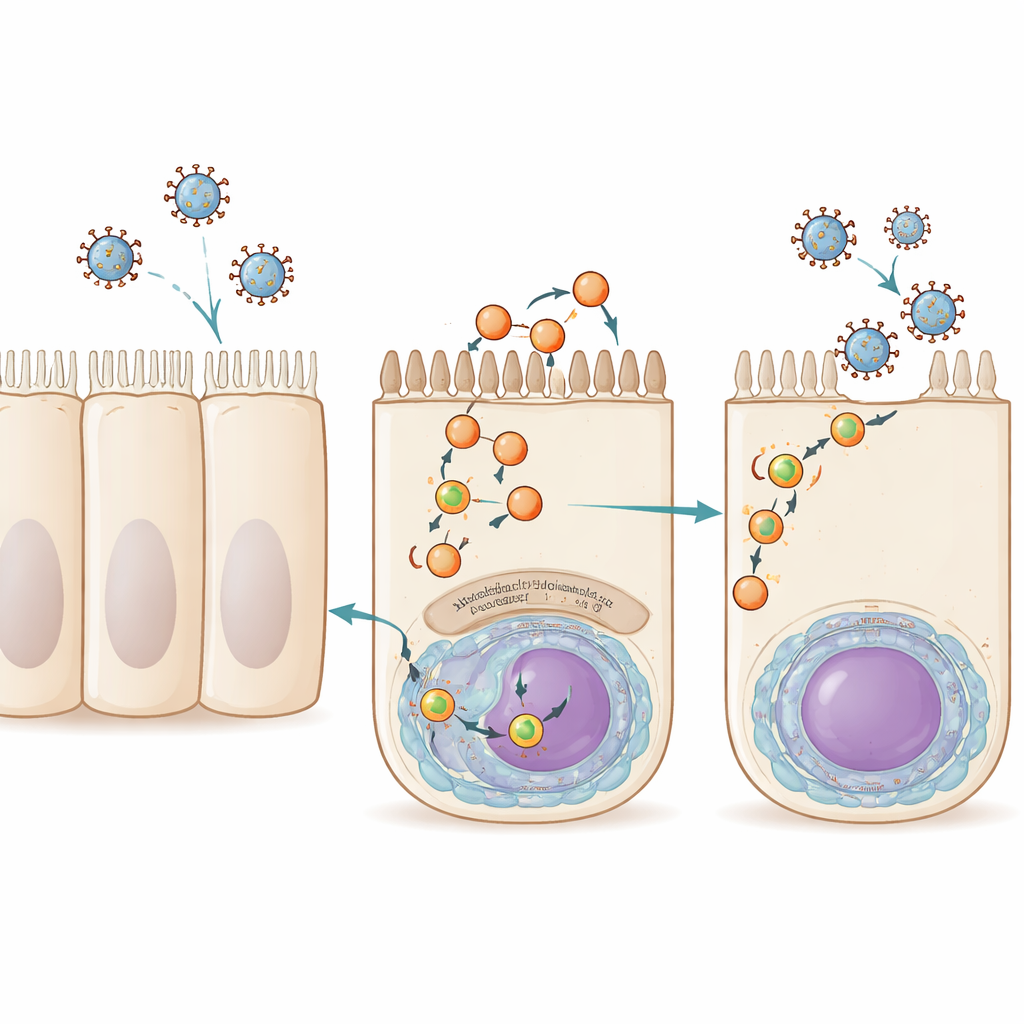
اكتشاف لاعب جديد: مايوفيرلين
بدأ الباحثون بالسؤال عن البروتينات البشرية التي ترتبط جسديًا بآلية تغليف جينوم الإنفلونزا في أوقات مختلفة خلال العدوى. صنعوا فيروس إنفلونزا A مهندسًا بحيث يحمل بوليميرازه وسمًا جزيئيًا، ثم استخدموا مطيافية الكتلة لجرد البروتينات البشرية المرتبطة بهذا المُركب مبكرًا ومتأخرًا خلال العدوى. من بين مئات المرشحين، برز واحد في النقاط الزمنية المتأخرة: مايوفيرلين، بروتين كبير مرتبط بالغشاء سبق ربطه بتطور العضلات، والابتلاع الخلوي وإصلاح الغشاء. عندما خفض الفريق مستويات مايوفيرلين في خلايا مشتقة من الرئة باستخدام حمضيات نووية متداخلة صغيرة أو قاموا بحظره بمثبط جزيئي صغير، استمرت الخلايا في صنع الحمض النووي الريبي والمواد البروتينية الفيروسية بشكل طبيعي، لكنها أطلقت عددًا أقل بكثير من الجسيمات الإنفلونزية المُعدية. أشارت هذه النتيجة إلى أن مايوفيرلين ليس ضروريًا لنسخ الجينوم الفيروسي، لكنه حاسم للمراحل اللاحقة عندما تُجمع الفيروسات الجديدة وتخرج من الخلية.
مايوفيرلين يسافر مع الحمولة الفيروسية
كشفت التصويرات عالية الدقة عن مكان مايوفيرلين أثناء العدوى. في الخلايا غير المصابة، يتداخل مايوفيرلين إلى حد كبير مع الحويصلات المعاد تدويرها الموجبة لـRab11، سواء بالقرب من النواة أو نحو حافة الخلية، وفقدان أي من البروتينين يُعطل التوزيع الطبيعي للآخر. أثناء عدوى الإنفلونزا، يُعاد تشكيل شبكة Rab11 بشكل كبير إلى حويصلات متضخمة وغير منتظمة تحمل مجمعات ريبونو-بروتينية فيروسية. يحتفظ بهذه الحويصلات المعاد تشكيلها مايوفيرلين ويُظهر توطينًا قويًا مشتركًا مع الجينوم الفيروسي وRab11. عندما استخدم الفريق دواءً يجبر مجمعات الجينوم الفيروسي وحويصلاتها الحاملة على التكتل معًا، سُحب مايوفيرلين إلى نفس التكتلات، مما يؤكد أنه مكوّن مدمج في هذه الهياكل الناقلة المتأخرة وليس مجرد موجود بالصدفة بالجوار.
محور مشترك لعدة فيروسات تنفسية
سأل الباحثون بعد ذلك ما إذا كان الاعتماد على مايوفيرلين فريدًا بالنسبة للإنفلونزا أم أنه مشترك على نطاق أوسع. أدى خفض مايوفيرلين في خلايا الرئة المصابة بـRSV أو فيروس سنداي مرة أخرى إلى انخفاض قوي في الفيروس المعدي المُطلق، دون خفض مستويات الحمض النووي الريبي الفيروسي. أظهر التصوير أحادي الجزيء تجمع جينومات كلا الفيروسين معًا مع مايوفيرلين وRab11 في بقع سيتوبلازمية يُحتمل أن تمثل محاور نقل بدلاً من معامل نسخ. يدعم هذا النمط صورة موحدة: فيروسات RNA التنفسية المغلفة المختلفة، رغم أنماطها الحياتية المتنوعة، تتقارب على نفس نظام الحويصلات Rab11–مايوفيرلين عندما يحين وقت نقل جينوماتها المكتملة نحو سطح الخلية للتغليف والخروج.
كيف يشكل مايوفيرلين الحويصلات الناقلة للفيروس
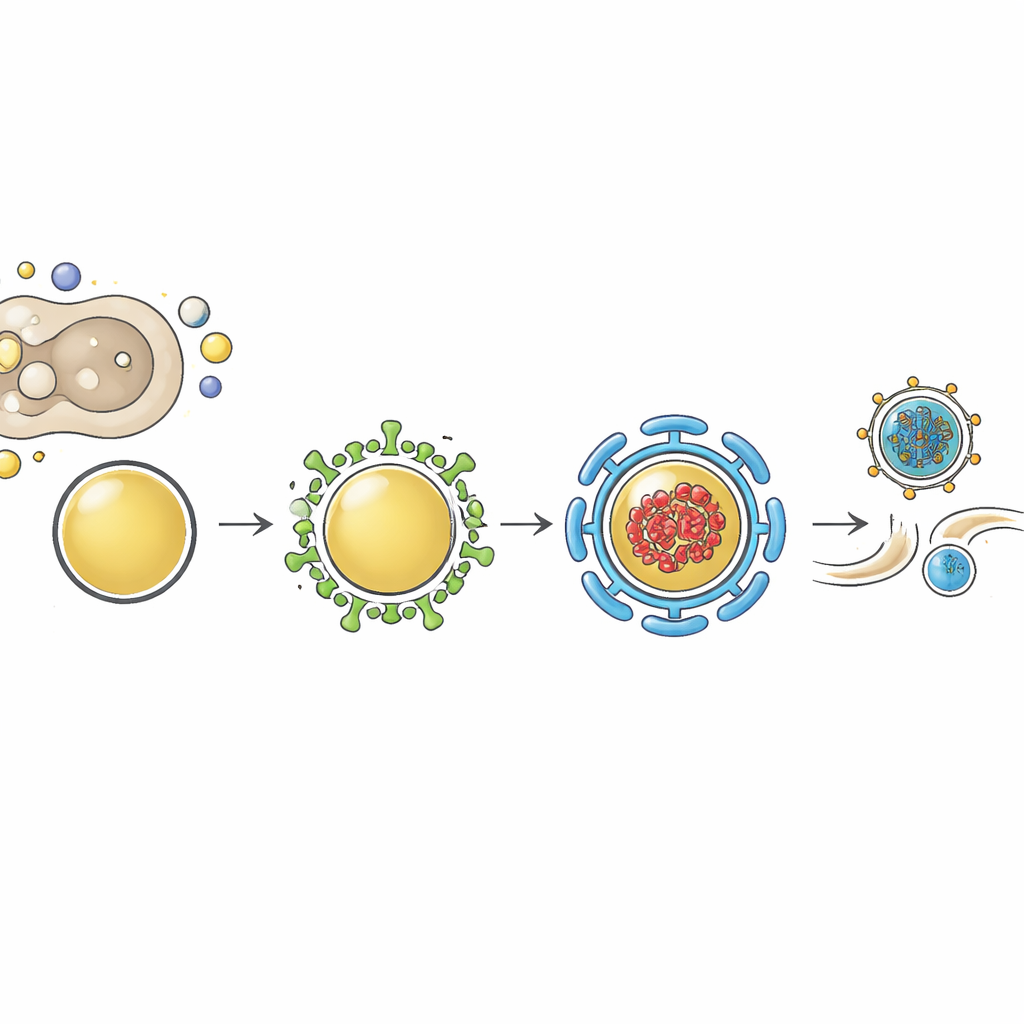
يتكوّن مايوفيرلين من عدة مجالات "C2" يمكنها ربط الأغشية وبروتينات الشريك. أظهرت أعمال سابقة أن أحد هذه المجالات يتفاعل مع عائلة من بروتينات تشكيل الغشاء تُدعى EHDs. في هذه الدراسة، وُجد كل من EHD1 وEHD2 الموسوم فلورسينياً داخل نفس الحويصلات المعاد تشكيلها التي تحمل جينومات الإنفلونزا وRab11، خاصة عندما تم تجميع هذه الحويصلات تجريبيًا. خفض مستويات EHD2، كما خفض مايوفيرلين، خفّض محصلات الإنفلونزا دون أن يؤثر على نسخ الجينوم. علاوة على ذلك، أدى إزالة مايوفيرلين إلى انخفاض مستويات بروتين EHD2، مما يوحي بأن مايوفيرلين يساعد في استقرار EHD2 أو وضعه بشكل صحيح على الأغشية. يقترح المؤلفون أن مايوفيرلين يجلس على الحويصلات الموجبة لـRab11 ويستقطب بروتينات EHD لنحت أغشيتها، مكملاً تكوين "حويصلات مغطاة بشكل غير منتظم" متخصصة ومحسّنة لنقل الحمولة الفيروسية إلى مواقع النبْت.
ماذا يعني هذا لاستراتيجيات مضادة للفيروسات مستقبلية
معًا، تضع النتائج مايوفيرلين كمنظّم مركزي لمسار إعادة تدوير في المضيف تعتمد عليه العديد من الفيروسات التنفسية المغلفة في خطوة حرجة متأخرة. وبما أن استهداف البروتينات الفيروسية وحدها يؤدي غالبًا إلى مقاومة سريعة، فإن عوامل المضيف المشتركة بين فيروسات متعددة تُعد أهدافًا دوائية جذابة. قد يؤثر تعطيل وظيفة مايوفيرلين، أو شراكته مع Rab11 وبروتينات EHD، مبدئيًا في إبطاء أو منع انتشار مسببات مرضية متنوعة، من الإنفلونزا وRSV إلى فيروسات أخرى معتمدة على Rab11 مثل بعض الفيروسات التاجية. لا يزال العمل كثيرًا قبل ترجمة هذا المفهوم إلى علاجات آمنة، لكن الدراسة تقدم خريطة مفصلة لمسار هرب فيروسي مشترك — وتسلط الضوء على مايوفيرلين كنقطة اختناق واعدة على طول ذلك الطريق.
الاستشهاد: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
الكلمات المفتاحية: الأنفلونزا, الفيروسات التنفسية, نقل الحويصلات, عوامل المضيف, مايوفيرلين