Clear Sky Science · ar
محفزات فضية معدلّة بواسطة ربيطات الكبريت الأريلية ذات تقارب ربط مصمّم لتحويل النترات انتقائياً إلى أمونيا
تحويل التلوث إلى سماد ذي قيمة
تعتمد الزراعة الحديثة اعتماداً كبيراً على الأسمدة المحتوية على الأمونيا، لكن إنتاج الأمونيا بالطرق التقليدية يستهلك كثيراً من الوقود الأحفوري ويطلق كميات كبيرة من ثاني أكسيد الكربون. في الوقت نفسه، يؤدي فائض النترات من الأسمدة والنفايات الصناعية إلى تلوث الأنهار والمياه الجوفية. تستعرض هذه الدراسة طريقة لمعالجة المشكلتين معاً: استخدام محفزات فضية مصممة بعناية لتحويل النترات غير المرغوب فيها في الماء مباشرة إلى أمونيا نافعة تحت ظروف لطيفة مدفوعة بالكهرباء.
لماذا تهم النترات والأمونيا
الأمونيا هي العمود الفقري لإنتاج الأسمدة، والطلب العالمي دفع إنتاجها إلى نحو 190 مليون طن سنوياً، غالبيته عبر عملية هابر–بوش التي تعود لعقود. تعمل هذه العملية عند درجات حرارة وضغوط عالية وتمثل جزءاً ملحوظاً من استهلاك الطاقة والانبعاثات الكربونية العالمية. في الوقت نفسه، تحمل مياه الجريان من المزارع والمصانع كميات كبيرة من النترات التي تضر بالأنظمة البيئية ومصادر مياه الشرب. قد تُمكّن تقنية تحول تلوث النترات إلى أمونيا في درجة حرارة الغرفة بواسطة الكهرباء من تنظيف المياه وتوفير سماد بطريقة أكثر صداقة للمناخ.
تشكيل سطح الفضة
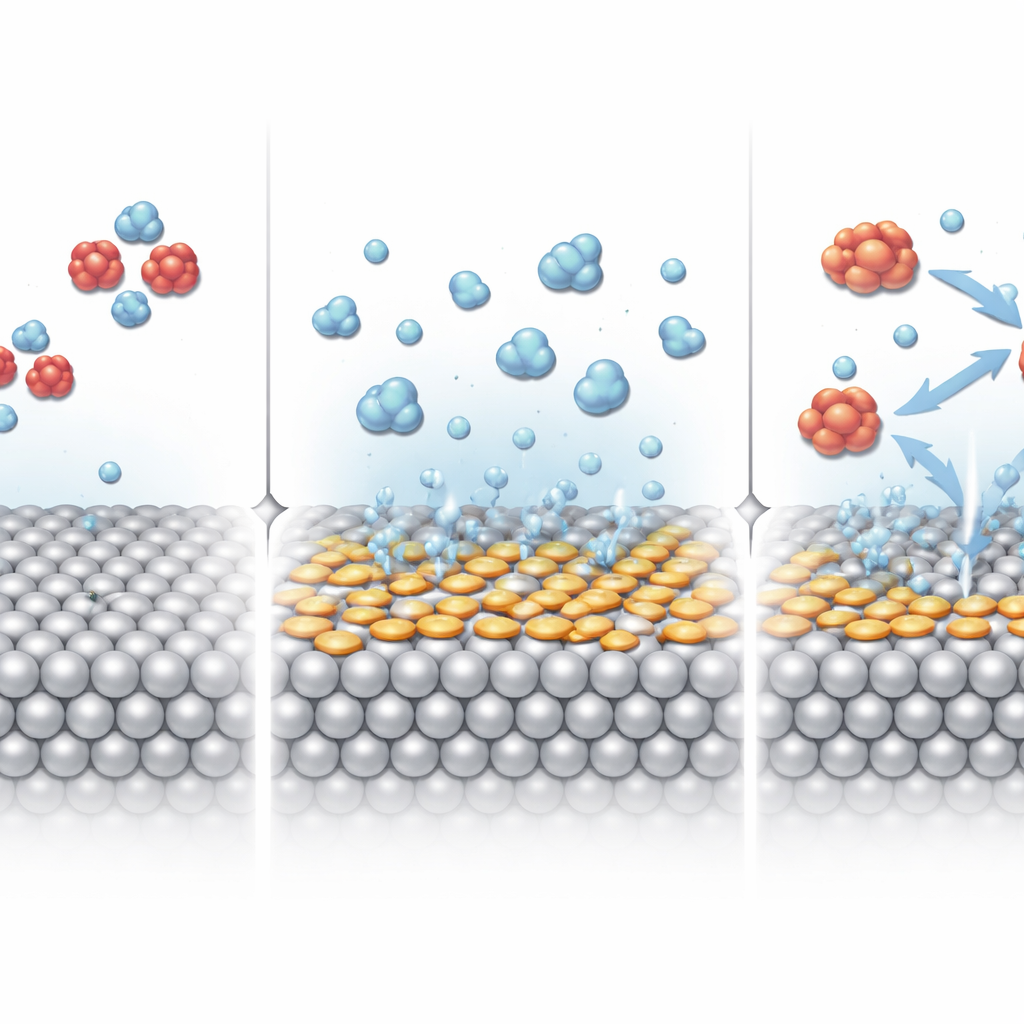
تُعرف الفضة بقدرتها على التقاط النترات وبدء تحللها الكيميائي، لكنها تواجه صعوبة في دفع التفاعل إلى نهاية المسار نحو الأمونيا. تكمن المشكلة الرئيسية في مدى قوة ارتباط سطح الفضة ببقايا النيتروجين خلال المراحل المتوسطة. تعامل الباحثون مع هذا عبر «تزيين» مكعبات فضية نانوية صغيرة بعائلة من الجزيئات العضوية الحاوية على الكبريت التي ترتبط بثبات بالمعدن. من خلال تعديل الطابع الإلكتروني لهذه الربيطات الأريلية الكبرية، استطاعوا إعادة تشكيل تفاعل سطح الفضة مع الوسائط المتوسطة للتفاعل بشكل دقيق دون تغيير الحجم أو الشكل العام للجسيمات النانوية.

البحث عن الإضافة الجزيئية الأمثل
باستخدام مزيج من المحاكاة الحاسوبية والاختبارات الكهروكيميائية، قام الفريق بفحص خمسة ربيطات مختلفة إما مانحة أو سالبة لكثافة الإلكترون على سطح الفضة. أظهرت الحسابات أن هذه الجزيئات تغير الشحنة على ذرات الفضة السطحية وتعدّل سهولة التصاق النترات، وتفتتها، وتفاعلها مع الهيدروجين المشتق من الماء. برزت ربيطة واحدة، 4-(ميثيلثيو)بنزالدهيد (MTBA)، كأفضل مرشح: إذ رفعت الحالة الظاهرية لأكسدة ذرات الفضة السطحية وخلقت مواقع تربط الوسائط الأساسية بقوة كافية لتسريع التفاعل دون أن تُحبَس فيها هذه الوسائط. أكدت التجارب هذا التنبؤ: مكعبات الفضة النانوية المعدلة بـMTBA ضاعفت تقريباً نسبة الشحنة الكهربائية التي تتحول إلى أمونيا، فزادت كفاءة إنتاج الأمونيا من نحو 51% إلى ما يقارب 99%، وزادت معدل الإنتاج بحوالي مرتين ونصف.
كيف يعمل الماء والوسطوات معاً
لفهم سبب فاعلية MTBA، فحص الباحثون الواجهة حيث يلتقي المحفز الصلب والماء والنترات. كشفت طيفية رامان المتقدمة أنه، في ظروف العمل، يجتذب السطح المزين بـMTBA مجموعة من جزيئات الماء ذات روابط هيدروجينية أضعف، وهي أسهل انقساماً إلى أنواع هيدروجينية تفاعلية. أظهرت قياسات عزم الدوران الإلكتروني أن هذه الذرات الهيدروجينية التفاعلية تتولد بسهولة أكبر على السطح المعدل وتستهلك بسرعة في خطوات الهدرجة بدلاً من تكوين غاز الهيدروجين. كما كشفت طيفيات موقعية أخرى عن وجود وسيطات مثل HNO تتكوّن عند جهود أقل وبكميات أكبر على الفضة المعالجة بـMTBA، مما يدل على أن الجزيئات المضافة تساعد في توجيه شظايا النترات والهيدروجين معاً بكفاءة، خطوة بخطوة، نحو الأمونيا بدلاً من نواتج جانبية.
من خلية مخبرية إلى جهاز عملي
انتقالاً إلى ما هو أبعد من الخلايا الاختبارية الصغيرة، بنى الفريق خلية تحلل كهربائية قائمة على غشاء تستخدم مكعبات الفضة النانوية المعدلة بـMTBA ككاثود. في ماء قلوي يحتوي على نترات، قدم هذا الجهاز تيارات كهربائية عالية مع الحفاظ على انتقائيات للأمونيا تتجاوز 90% لأكثر من 100 ساعة، وخفض تركيزات النترات والنتريت في مياه النموذج إلى ما دون حدود مياه الشرب في أقل من ساعة ونصف. تشير تحليلية اقتصادية بسيطة إلى أنه، إذا تم تشغيل هذه الأنظمة بكهرباء منخفضة التكلفة، فقد تنتج أمونيا من مياه الصرف الغنية بالنترات بتكاليف منافِسة للإنتاج الصناعي الحالي—مع تقديم خدمة تنظيف التلوث في آن واحد.
ما الذي يعنيه هذا للمستقبل
تُظهر هذه العمل أن الجزيئات العضوية المختارة بعناية على سطح معدني يمكن أن تعمل كمقابض ضبط دقيقة توجّه تفاعلاً كهروكيميائياً معقداً نحو منتج واحد مرغوب. باستخدام ربيطات الكبريت الأريلية مثل MTBA لضبط قوة ارتباط الوسائط الأساسية ولتحفيز الماء بشكل أفضل، حوّل المؤلفون مكعبات الفضة النانوية إلى آلات انتقائية عالية لتحويل النترات إلى أمونيا. يمكن توسيع مفهوم هندسة الواجهة الجزيئية المعروض هنا إلى معادن وتفاعلات أخرى، مقدّماً مخططاً لإنتاج أسمدة أنظف ومعالجة أكثر استدامة للجداول الملوّثة بالنتروجين.
الاستشهاد: Zhang, L., Liu, Y., Li, L. et al. Aryl sulfur ligand-modulated silver catalysts with tailored binding affinity for selective nitrate-to-ammonia conversion. Nat Commun 17, 2553 (2026). https://doi.org/10.1038/s41467-026-69385-1
الكلمات المفتاحية: الاختزال النمطي الكهربائي للنترات, تخليق الأمونيا, محفزات فضية نانوية, تحويل مياه الصرف إلى قيمة, هندسة الواجهة