Clear Sky Science · ar
حويصلات نانوية مُهندَسة من الإكسوسومات لتوصيل الأجسام المضادة لعلاج التهاب الأمعاء الالتهابي
أمل جديد لمرض معوي عنيد
يمكن أن يحوّل التهاب الأمعاء الالتهابي (IBD) الحياة اليومية إلى معركة مستمرة مع الألم والإسهال والإرهاق، كما يزيد من خطر الإصابة بسرطان القولون على المدى الطويل. العديد من الأدوية الحالية تهدئ التوهّجات لكنها لا تعيد فعلياً توازن الاستجابات المناعية المعيبة التي تقود المرض، لذلك تعود الأعراض غالباً. تقدم هذه الدراسة جسماً نانويًا «ذكيًا» مُهندَسًا يسافر عبر مجرى الدم، ويجد المناطق الملتهبة في الأمعاء، ويوصل علاجًا ذا شقين مصمَّمًا لتقليل الالتهاب الضار وإعادة بناء توازن مناعي دائم.
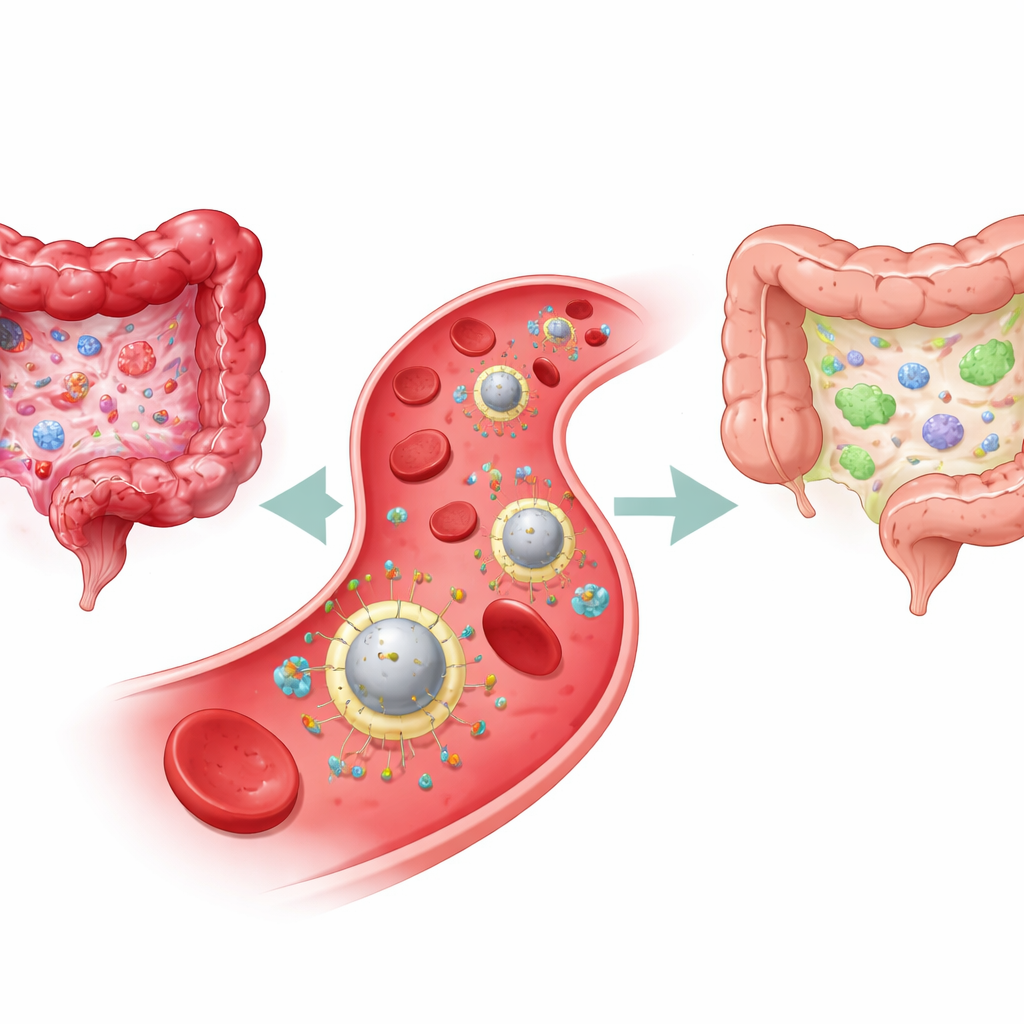
لماذا العلاج الحالي غير كافٍ
ينجم التهاب الأمعاء الالتهابي، الذي يشمل داء كرون والتهاب القولون التقرحي، عن صراع مزمن في جهاز المناعة المعوي. ففي جهة توجد خلايا مناعية نشطة وجزيئات التهابية تضرّ بطبقة الأمعاء؛ وفي الجهة الأخرى خلايا تنظيمية عادةً ما تكبح هذه الاستجابة. تحاول العلاجات القياسية—مثل الستيرويدات، والمثبّتات المناعية، والأدوية البيولوجية—تقليل الالتهاب في جميع أنحاء الجسم. قد تُخفف الأعراض، لكنها غالبًا ما تفشل في استعادة التوازن المناعي الأساسي، وكبح المناعة على نطاق واسع قد يزيد من مخاطر العدوى. حتى الأجسام المضادة الحديثة التي تعيق إشارة التهابية رئيسية تسمى الإنترلوكين‑23 (IL‑23) تفيد جزءًا فقط من المرضى وتبقى متداولة على نطاق واسع في الجسم بدلاً من التركيز حيث الحاجة.
بناء دواء موجه يتغير حسب الشكل
سعى الباحثون لتصميم علاج يتصرف أشبه بخلية حية بدلاً من دواء بسيط. بدأوا وفقاعات صغيرة تُفرَز طبيعياً من خلايا تي التنظيمية—وهي خلايا مناعية تعزز التحمل والحفاظ على السلم. تحمل هذه الفقاعات، المسماة إكسوسومات، بروتينات ومادة وراثية يمكنها دفع خلايا مناعية أخرى نحو حالة تهدئة. دمج الفريق هذه الإكسوسومات مع أجزاء من غشاء الصفيحات الدموية، مستعيرين قدرة الصفيحات على الالتصاق بالأوعية الدموية المتضررة في الأنسجة الملتهبة. وعلى سطح هذا الغشاء الهجين ربطوا أجسامًا مضادةً تعيق IL‑23 باستخدام «خيط» جزيئي يمكن قطعه بواسطة إنزيمات (معدّيات البروتينات المصفوفية) التي تتواجد بكثرة فقط في نسيج الأمعاء الملتهب. النتيجة، المسمّاة PrEXO‑a23، هي حويصلة نانوية تدور في الدم، وتلتصق بالأوعية المعوية المتضررة، ثم تفرّغ حمولة الأجسام المضادة فقط حيثما يكون المرض نشطًا.
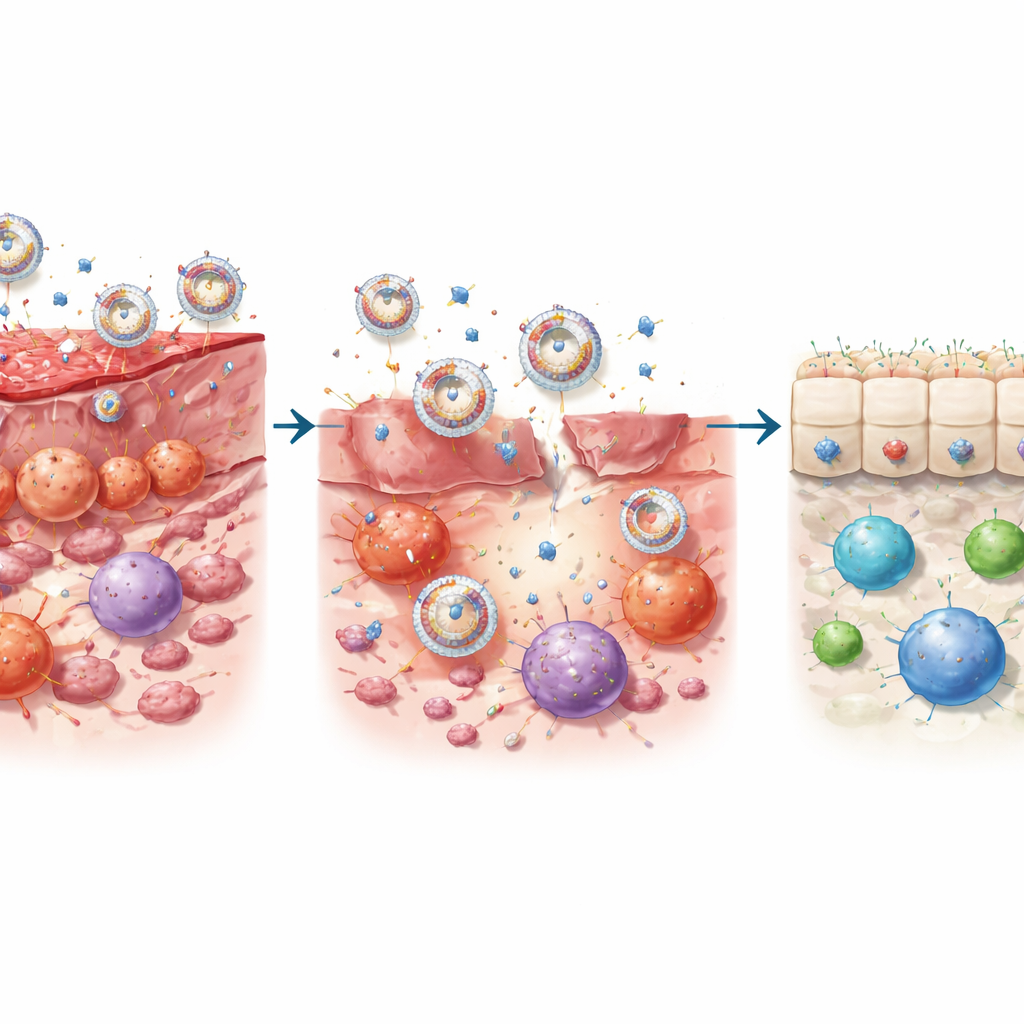
إعادة تعليم الحي المناعي في الأمعاء
في دراسات خلوية، تفوقت PrEXO‑a23 على كل من الجسم المضاد أو الإكسوسومات بمفردهما. قلّلت بشكل كبير من تشكل خلايا T‑helper 17 (Th17) الالتهابية وإفراز السيتوكينات الضارة التي تهاجم بطانة الأمعاء، بينما حمت خلايا الظهارة المعوية البشرية من الموت. وفي الوقت نفسه، دفعت الخلايا الشجرية—بوّابات الجهاز المناعي التي توجه خلايا تي—بعيدًا عن حالة تنشيط عدائية نحو حالة «تحمل» تشجع نمو خلايا تي التنظيمية. في نماذج الفأر لالتهاب القولون، توجّهت الحويصلات النانوية بكفاءة إلى نسيج القولون الملتهب، وابتلعها أنواع متعددة من الخلايا المناعية، وأطلقت الأجسام المضادة استجابةً للنشاط الإنزيمي المحلي. هذا العمل المزدوج—حجب الالتهاب المدفوع بـ IL‑23 وتعزيز إشارات تحفز التحمل—قرب مؤشرات الالتهاب من المستويات الطبيعية وأعاد توازنًا صحيًا لأنواع خلايا تي.
إصلاح الأنسجة ومنع الضرر طويل الأمد
الفئران المصابة بالتهاب القولون الكيميائي التي تلقت PrEXO‑a23 فقدت وزنًا أقل، كان لديها أمعاء أكبر وأصح، وظهرت لديها تضخّم أقل للطحال، وهو علامة على الالتهاب الجهازِي. أظهر الفحص المجهري حفظ بنية الأمعاء ووجود وصلات أحكم بين خلايا الظهارة، مما يدل على إصلاح الحاجز. وساعد العلاج أيضًا على إعادة توازن بكتيريا الأمعاء، بزيادة العائلات المرتبطة بصحة الأمعاء وتقليل تلك المرتبطة بالمرض. في نموذج أكثر شدة يحاكي الانتقال من التهاب قولون مزمن إلى سرطان القولون، لم يخفف PrEXO‑a23 الالتهاب الجاري فحسب، بل منع تمامًا تطور الأورام وكبح سماكة وتندّب جدار الأمعاء المميزة للتليف. أشارت التحليلات الجزيئية إلى استعادة إشارة الحماية المرتبطة بـ p53—الحارس المركزي ضد السرطان—التي ثبت أنها مهمة لتأثير مكافحة السرطان.
نحو رعاية أذكى وأكثر دوامًا لالتهاب الأمعاء
لغير المتخصص، الرسالة الأساسية هي أن هذا العمل يتجاوز مجرد «تخفيف» الالتهاب. بجمع إيصال مستهدف، وإطلاق أجسام مضادة في الموقع، وحمولة إكسوسومية مهدِّئة للمناعة في حزمة واحدة دقيقة، تهدئ PrEXO‑a23 المرض النشط وتساعد على إعادة تدريب الجهاز المناعي نحو تحمل دائم. في الفئران، أدى ذلك ليس فقط إلى تخفيف الأعراض بل أيضًا إلى الحماية من التندّب وسرطان القولون، وهما من أخطر مضاعفات التهاب الأمعاء الطويل الأمد. وعلى الرغم من أن مزيدًا من الاختبارات اللازمة قبل وصول مثل هذا العلاج إلى المرضى، تُظهر الدراسة كيف قد تقدّم الأدوية النانوية المستوحاة من الأحياء يومًا ما تحكمًا أكثر دقة وديمومة في الاضطرابات المناعية المعقدة مثل IBD.
الاستشهاد: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
الكلمات المفتاحية: التهاب الأمعاء الالتهابي, الطب النانوي, تحمل المناعة, الإكسوسومات, الوقاية من سرطان القولون والمستقيم