Clear Sky Science · ar
العيوب البنائية في لُفَائف الأميلويد-β تُحفّز النواة الثانوية
لماذا تهم الشوائب الصغيرة في بروتينات الدماغ
في مرض الزهايمر والأمراض الدماغية المرتبطة، تتجمع بروتينات معينة لتشكيل هياكل طويلة تشبه الخيوط تُسمى لُفَائف الأميلويد. هذه اللفائف لا تميّز المرض فحسب؛ بل تساعد أيضًا في إنتاج جزيئات بروتينية جديدة شديدة السمية يمكن أن تضر الخلايا الدماغية. تطرح هذه الدراسة سؤالًا بسيطًا لكنه قويًا: هل تعمل "العيوب" البنائية النادرة داخل لفائف الأميلويد كنقاط ساخنة أساسية تُشعل نموًا ضارًا جديدًا؟ قد تشير الإجابة إلى طرق جديدة لإبطاء هذه الاضطرابات أو إيقافها عن طريق استهداف عدد قليل من المواقع الحاسمة بدلًا من سطح البروتين بأكمله. 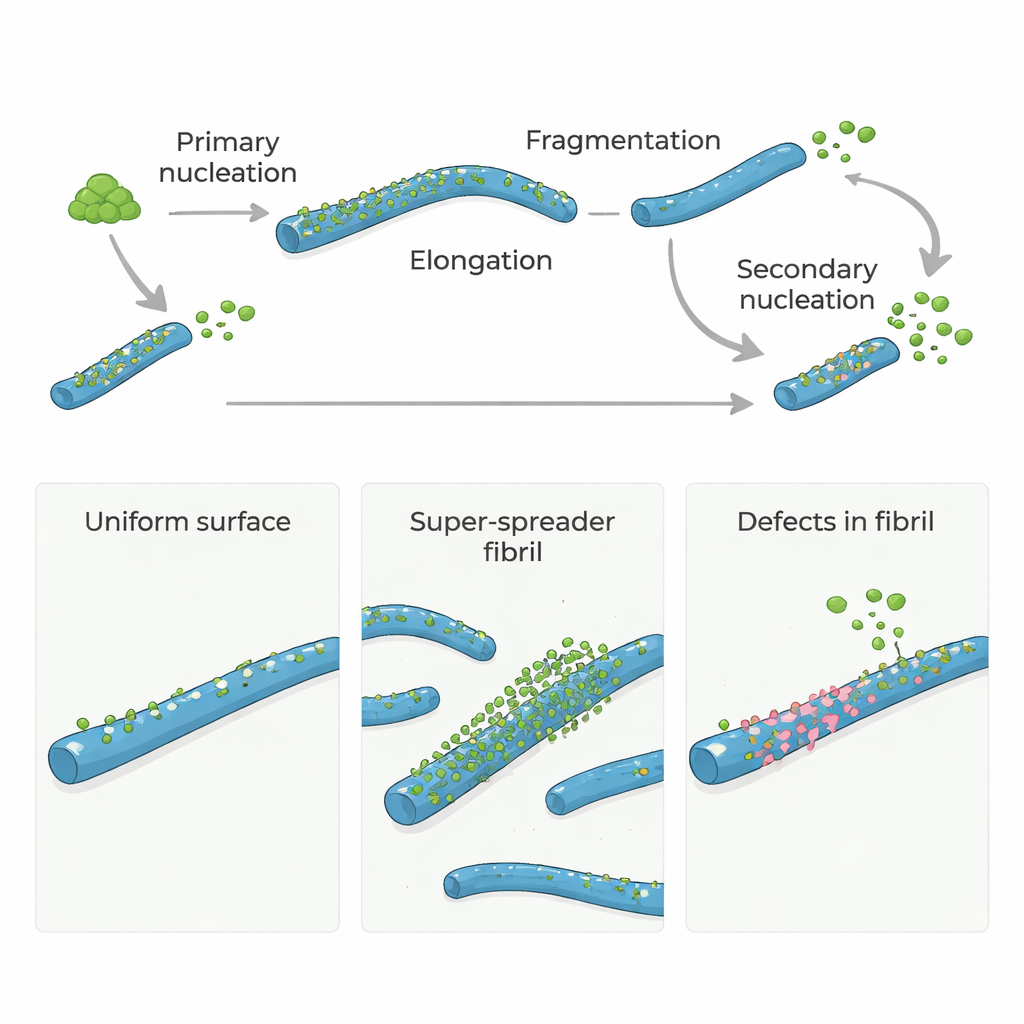
من بروتين هادئ إلى تفاعل سلسلة خارق
بروتينات أميلويد-β (Aβ)، المحورية في مرض الزهايمر، لا تشكّل عادة تجمعات بسرعة من تلقاء نفسها. للشروع في ذلك، يجب أن تتجمع بعض المونومرات ببطء لتكوّن اللفائف الصغيرة الأولى، وهي خطوة تُدعى التكوّن البدئي (النواة الأولية). بعد ظهور هذه اللفائف الأولية، تنمو بسرعة مع إضافة مونومرات إضافية إلى نهاياتها. والأهم من ذلك أن اللفائف الموجودة يمكن أن تحفّز ظهور لفائف جديدة على أسطحها في عملية تُعرف بالنواة الثانوية. هذه الخطوة التي يقودها السطح يمكن أن تُغمر النظام بلفائف جديدة وأوليغومرات سامة صغيرة، فتحوّل تدفقًا بطيئًا إلى تفاعل سلسلة خارج السيطرة.
هل كل أسطح اللفائف خطرة بالمثل؟
افترضت العديد من النماذج أن سطح ليف أميلويد كله فعّال بالتساوي في تحفيز النواة الثانوية. ومع ذلك، ألمحت تجارب حديثة إلى أن جزءًا صغيرًا فقط من السطح هو النشط فعليًا. للاستقصاء، استخدم الباحثون جزيئًا طبيعيًا يعمل كـ"شابرون" يُدعى Brichos، المعروف بقدرته على حجب النواة الثانوية لـ Aβ40 وAβ42 (صورتان رئيسيتان من أميلويد-β). بقياس دقيق لمقدار Brichos الموسوم بالفلوريسنس الذي يلتصق باللفائف، وجدوا أنه يرتبط بقوة لكن بعدد ضئيل جدًا: تقريبًا جزيء Brichos واحد لكل 100–150 جزيء Aβ في اللفيفة. ومع ذلك، كانت هذه التغطية المتباعدة كافية لقمع أكثر من 90% من النواة الثانوية، ما يعني أن مواقع نادرة ومُحلية — لا السطح بأكمله — هي التي تهيمن على إنتاج التجمعات السامة الجديدة.
استكشاف دور العيوب الخفية
اقترحت هذه النتائج أن مواقع النواة الحاسمة قد تكون عيوبًا بنائية — شوائب صغيرة تتكون أثناء نمو اللفائف، مثل طبقات غير مصطفة أو حديثة التعرض للنواة الداخلية. لاختبار هذه الفكرة مباشرة، نما الباحثون لفائف Aβ40 تحت شرطين مختلفين. تكونت مجموعة واحدة، "اللفائف الضابطة"، تحت ظروف تشبع قوية نموذجية تُفضل النمو السريع والاحتجاز الحركي للعيوب. أما المجموعة الأخرى فتم إنشاؤها باستخدام بروتوكول تنعيم بطيء ومتحكم في درجة الحرارة: نما اللفائف عند قوة دافعة فعّالة منخفضة جدًا، قريبة من حد ذوبانها، حيث يمكن للهياكل غير الصحيحة أن تذوب أو تُصلَح قبل أن تُقفل. أظهرت الميكروسكوبية الإلكترونية بالتبريد عالية الدقة أن مجموعتي اللفائف بدتا متطابقتين أساسًا في الشكل العام والالتواء، مما يشير إلى أن عملية التنعيم لم تغيّر المورفولوجيا الأساسية. 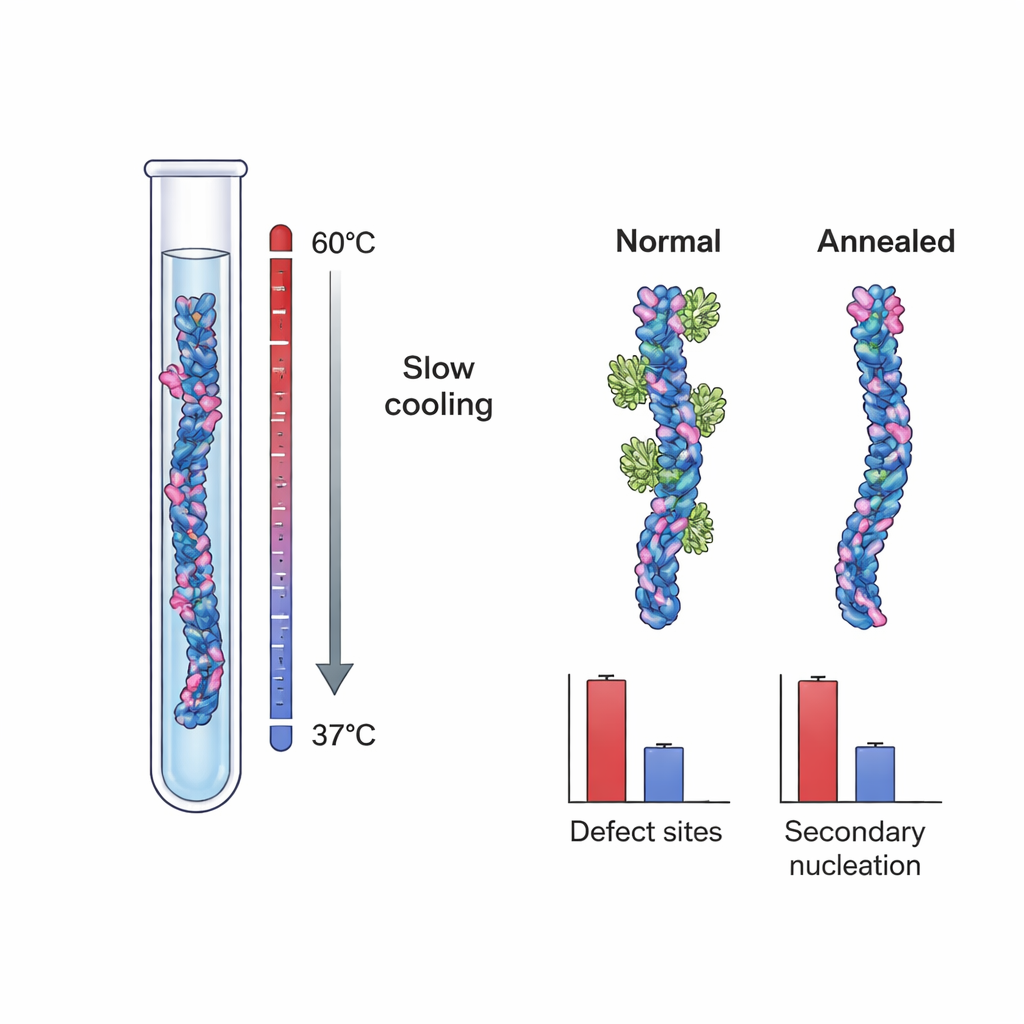
عيوب أقل، مواقع نمو خطيرة أقل
عندما قاس الفريق ارتباط Brichos بهذين النوعين من اللفائف، اكتشفوا فرقًا لافتًا. كان لدى لفائف Aβ40 الضابطة نحو موقع ارتباط واحد لـ Brichos لكل ~100 مونومير، مما يشير مرة أخرى إلى مواقع نادرة لكنها مهمة. أما اللفائف المملَّنة فكان لديها نحو موقع واحد لكل ~800 مونومير — انخفاض يقارب 90% في تكرار المواقع. في اختبارات منفصلة حيث أُضيفت هذه اللفائف كبذور إلى محاليل Aβ40 جديدة، كانت اللفائف المملَّنة أقل فعالية بكثير في تحفيز التجمع الجديد، حتى عندما تم مطابقة كتلتها الإجمالية مع كتلة اللفائف الضابطة. أظهر نمذجة حركية مفصلة أن هذا الانخفاض في القدرة على الإحداث لا يمكن تفسيره ببساطة بفروق في طول اللفائف. بل تماشى كميًا مع انخفاض عدد مواقع ارتباط Brichos، مما يدعم بقوة فكرة أن عيوب النمو تعمل كمحركات رئيسية للنواة الثانوية.
مبدأ عام ذو وعد علاجي
من خلال مزج الحجج الثرموديناميكية، وإعادة تحليل الأعمال السابقة، والمقارنات عبر عدة بروتينات مكوِّنة للأميلويد، يجادل المؤلفون بأن العيوب النادرة في النمو من المرجح أن تكون مركزية للنواة الثانوية في أنظمة عديدة، وليس فقط في Aβ المرتبط بالزهايمر. تعرّض هذه العيوب جزئيًا لبنية اللب الداخلي المكدّس بإحكام لللفيفة، مقدّمةً سقالات جاهزة حيث يمكن أن تتكوّن الأوليغومرات واللفائف الجديدة بسهولة أكبر بكثير من السطح الأملس. إن الاعتراف بهذه العيوب كالمذنبين الرئيسيين يفتح طرقًا جديدة لتصميم الأدوية. بدل محاولة حجب كل تفاعل ممكن على سطح اللفيفة، يمكن أن تهدف العلاجات إلى درء أو إصلاح هذه المواقع النادرة فقط، أو تقليل الظروف التي تُنشئها في المقام الأول. عمليًا، قد يعني ذلك خفض التركيز الفعّال للبروتينات المكوِّنة للأميلويد في الدماغ أو تصميم جزيئات مستوحاة من Brichos تتعرف على بقع النواة المدفوعة بالعيوب وتحيّدها. إذا نجحت، قد تقطع مثل هذه الاستراتيجيات المصدر الرئيسي للأوليغومرات السامة وتبطئ تقدم الأمراض المرتبطة بالأميلويد.
الاستشهاد: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
الكلمات المفتاحية: ليف أميلويد, مرض الزهايمر, النواة الثانوية, تجمّع البروتينات, الشابرون Brichos